Trebuie obţinute cel puţin două seturi de hemoculturi înainte de a începe terapia antimicrobiană la pacienţii cu suspiciune de infecţie de dispozitiv cardiac implantabil.
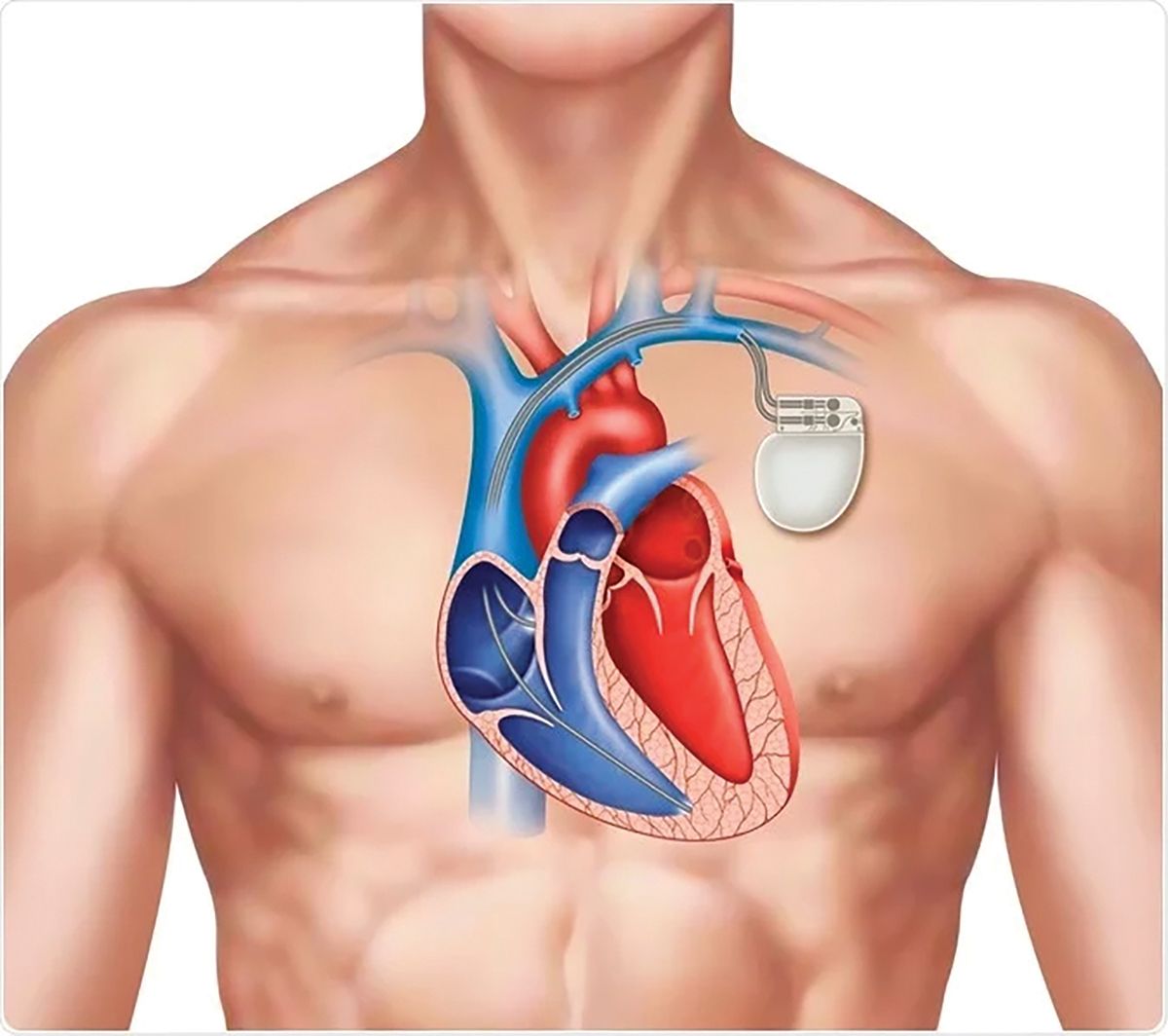
Dispozitivele cardiace implantabile (DCI) includ stimulatoarele cardiace, defibrilatorul implantabil și dispozitivele de resincronizare cardiacă. Din punct de vedere clinic, avem mai multe caracteristici ale infecţiilor asociate DCI. Acestea se pot referi la locul infecţiei, dar și la agentul patologic responsabil (4).

Infecţiile asociate dispozitivelor cardiace implantabile se pot produce prin două mecanisme majore: pe de o parte, contaminarea sondelor și/sau a generatorului de puls în timpul implantării sau manipulării ulterioare, iar pe de alta, consecinţa unei inoculări în cazul bacteriemiei secundare unei infecţii la distanţă. Aceste mecanisme nu se exclud reciproc, ci chiar pot coexista.
O infecţie a buzunarului DCI, fie primară, fie secundară, se manifestă prin modificări inflamatorii locale. Acestea pot include eritem de buzunar (41%), tumefiere (38%), durere și sensibilitate (28%), căldură (18%), exteriorizare (38%) și expunerea dispozitivului (21%) (4).
Eroziunea cutanată și expunerea dispozitivului pot apărea prin necroza grăsimilor și migrarea din straturile profunde prin piele. De obicei, acest lucru se întâmplă la distanţă faţă de procedura de implantare a dispozitivului cardiac, prin migrarea progresivă și pierderea de ţesut.
În unele cazuri, atunci când buzunarul nu este închis corespunzător din cauza suturilor slăbite sau a spaţiilor mari dintre punctele de sutură, incizia poate deveni dehiscentă. Odată ce dispozitivul implantat este expus, acesta este considerat infectat, deoarece este în contact direct sau comunică cu pielea și agenţii patogeni bacterieni locali (4).
Semnele iniţiale de eritem, sensibilitate și tumefacţie după o procedură de implantare a unui dispozitiv cardiac pot reprezenta o infecţie superficială sau o adevărată infecţie a buzunarului.
Infecţia de buzunar poate urma de-a lungul porţiunii intravasculare și intracardiace a dispozitivului cardiac. Prin urmare, pacienţii pot prezenta simptome sistemice, cum ar fi febră, frisoane, stare de rău, oboseală sau anorexie. Cu toate acestea, unii pacienţi cu vegetaţii de sonde nu prezintă semne și simptome sistemice.
Infecţia precoce a dispozitivului cardiac implantat este definită ca infecţie care apare în mai puţin de șase luni de la implantare și este mai probabil să se prezinte cu infecţie de buzunar. Infecţia tardivă este mai mult atribuită bacteriemiei și/sau endocarditei. Totuși, momentul debutului infecţiei după plasarea dispozitivului cardiac nu poate indica în mod sigur dacă infecţia este de tip localizat sau sistemic (4).
Severitatea și debutul simptomelor și semnelor fizice sunt legate atât de factorii microbieni, cât și de gazdă. Speciile de stafilococ sunt responsabile pentru 60-80% din infecţiile dispozitivelor cardiace implantabile. Staphylococcus aureus este o bacterie deosebit de virulentă, reprezentând 25% din infecţiile DCI, ducând adesea la apariţia febrei și a frisonului.
Stafilococul coagulazo-negativ este cea mai frecventă cauză a infecţiei legate de buzunarul dispozitivului, dar este mai puţin virulent și are mai puţine simptome sistemice. Stafilococii pot fi rezistenţi la terapia antimicrobiană și la sistemul de apărare al gazdei, deoarece formează un biofilm protector. Biofilmul împiedică eradicarea infecţiei dispozitivului numai prin administrarea de antibioterapie, fără îndepărtarea acestuia.
Infecţiile non-stafilococice legate de dispozitivul cardiac sunt prevalente și diverse, cu o virulenţă și o rată a mortalităţii relativ scăzute. Mai puţin de 10% din infecţiile asociate DCI sunt cauzate de bacili Gram-negativi, precum Klebsiella pneumoniae și Serratia marcescens.
Infecţia fungică este mai puţin frecventă. Bacteriemia Gram-negativă duce mai puţin frecvent la însămânţarea secundară a dispozitivului. Se recomandă o acoperire antimicrobiană empirică și extinsă împotriva bacteriilor Gram-pozitive și Gram-negative până când agentul patogen este identificat (4).
Pacienţii cu infecţii de dispozitive cardiace implantabile se pot prezenta cu embolie pulmonară sau cu osteomielită vertebrală și discită. Se recomandă recoltarea procalcitoninei (3).
Trebuie obţinute cel puţin două seturi de hemoculturi înainte de a începe terapia antimicrobiană la pacienţii cu suspiciune de infecţie de DCI. Creșterea germenului responsabil poate fi suprimată de antibioterapie, ceea ce poate induce în eroare sau poate masca diagnosticul clinic de infecţie a dispozitivului.
Hemoculturile ar trebui să includă atât culturi bacteriene aerobe, cât și anaerobe. Prelevarea de probe cu tampon de la nivelul buzunarului pentru culturi și coloraţie Gram, precum și cultura de ţesut la momentul îndepărtării dispozitivului sunt utile pentru identificarea microorganismului cauzator și pentru a susţine diagnosticul de infecţie asociată DCI.
Sensibilitatea culturii tisulare (69%) este mai mare decât cea a culturii cu tampon (31%). Când coloraţia Gram este negativă, trebuie efectuate culturi din ţesut pentru micobacterii și fungi. Întreaga sondă sau vârful acesteia ar trebui trimise pentru cultură, deși contaminarea sondelor se poate întâmpla în momentul extragerii acestora prin buzunarul generatorului (4).
Identificarea agentului patogen responsabil este foarte importantă. Culturile trebuie obţinute înaintea iniţierii terapiei antibiotice empirice. Acestea trebuie repetate la pacienţii cu DCI și febră, dar fără semne clare de infecţie sau de endocardită infecţioasă. La pacienţii instabili cu sepsis sau șoc septic, terapia antibiotică empirică precoce trebuie administrată după două seturi de hemoculturi (Figura).
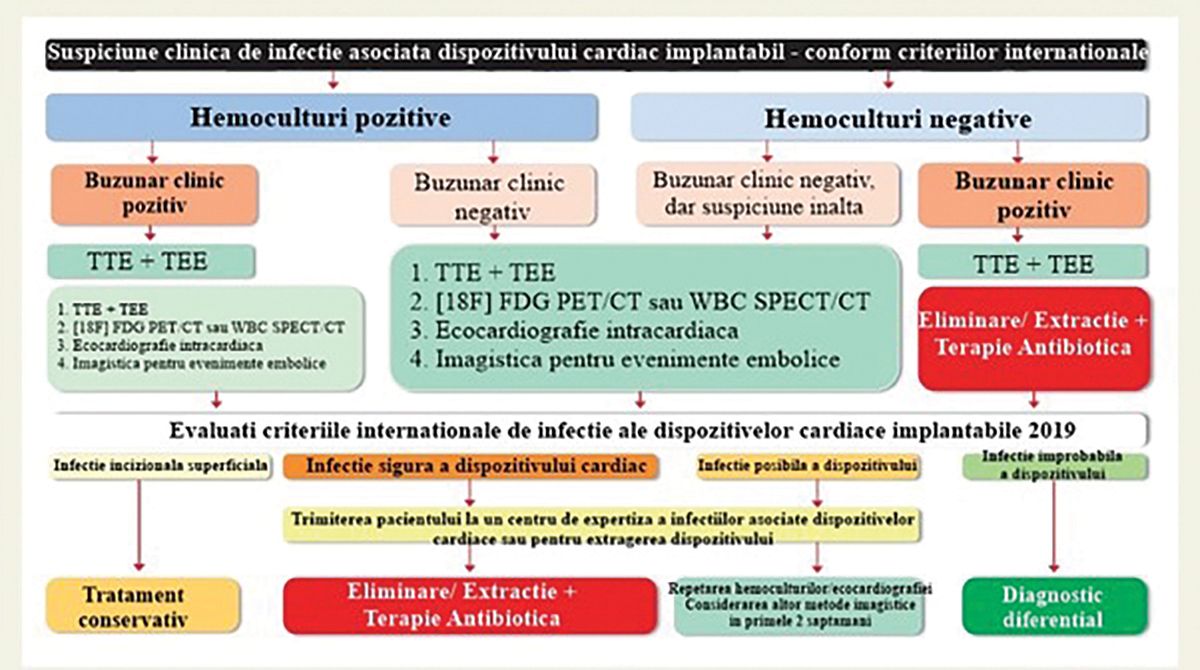
În cazul în care hemoculturile sunt negative, se poate lua în considerare utilizarea metodelor biomoleculare (amplificare ADN și/sau secvenţierea genelor) pentru a detecta agenţi microbieni atipici pentru endocardita asociată DCI. În timpul unei proceduri de extracţie, trebuie trimise pentru cultură fragmentele de sondă distale și proximale, vegetaţiile prezente pe sonde și ţesutul de la locul de implantare a generatorului.
Mediile de cultură sugerate sunt agar cu ciocolată în 5% CO2, agar MacConkey, agar cu sânge în condiţii anaerobe și agar Sabouraud. În caz de puroi, dar fără creștere după trei zile, trebuie luate în considerare microorganismele cu creștere lentă, precum Cutibacterium acnes (3).
Ecocardiografia transesofagiană este superioară atât în detectarea vegetaţiilor de la nivelul sondelor, cât și în măsurarea acestora. Aceasta permite vizualizarea sondelor în locuri atipice precum vena cavă superioară proximal sau în zone greu accesibile examenului transtoracic.
O serie de elemente cu valoare prognostică pot fi determinate mai ușor cu ajutorul ecografiei transtoracice, precum prezenţa lichidului pericardic, disfuncţia ventriculară și hipertensiunea pulmonară. Având în vedere complementaritatea investigaţiilor, se recomandă utilizarea ambelor metode în cazul suspiciunii endocarditei infecţioase asociate DCI.
Ecocardiografia intracardiacă are o sensibilitate crescută pentru detecţia vegetaţiilor pe dispozitivele cardiace. Astfel, o vegetaţie prezentă la ecocardiografia intracardiacă ar trebui considerată un criteriu major de diagnostic (3). O ecocardiografie normală nu exclude endocardita infecţioasă asociată DCI.
Scanarea cu fluor-18-fludeoxiglucoză ([18F]FDG), tomografia cu emisie de pozitroni/tomografia computerizată (PET/CT) și scintigrafia leucocitelor marcate radioactiv sunt instrumente complementare pentru diagnosticarea infecţiilor legate de DCI și a complicaţiilor asociate, putând distinge între infecţia superficială a inciziei chirurgicale cu debut precoce și o adevărată infecţie a generatorului localizat în buzunarul dispozitivului cardiac.
Când pacienţii se prezintă cu infecţie sistemică fără semne locale la nivelul implantului dispozitivului cardiac, PET/CT este folositor în diagnosticarea infecţiei locale, cu o specificitate și sensibilitate de aproximativ 93% și, respectiv, 98%. Această investigaţie este utilizată în mod particular pentru identificarea localizărilor embolice neașteptate și ale infecţiilor metastatice (3).
Citiți și: Infecţiile asociate dispozitivelor cardiace implantabile (1)
Material preluat din volumul „Boli infecţioase 2022 – Patologia infecţioasă în pandemie”, editat de Viaţa Medicală
Bibliografie
1. www.uptodate.com
2. E.PILLY 2020, Maladies Infectieuses et Tropicales 27ème édition
3. BLOMSTRÖM-LUNDQVIST, Carina, et al. European Heart Rhythm Association (EHRA) international consensus document on how to prevent, diagnose, and treat cardiac implantable electronic device infections—endorsed by the Heart Rhythm Society (HRS), the Asia Pacific Heart Rhythm Society (APHRS), the Latin American Heart Rhythm Society (LAHRS), International Society for Cardiovascular Infectious Diseases (ISCVID) and the European Society of Clinical Microbiology and Infectious Diseases (ESCMID) in collaboration with the European Association for EP Europace, 2020, 22.4: 515-549
4. KUSUMOTO, Fred M., et al. 2017 HRS expert consensus statement on cardiovascular implantable electronic device lead management and extraction. Heart rhythm, 2017, 14.12: e503-e551
5. BADDOUR Larry M, et al. Update on Cardiovascular Implantable Electronic Device; Infections and Their Management; A Scientific Statement From the American Heart Association, Endorsed by the Heart Rhythm Society
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe