
Boala Crohn (BC) este o boală cronică a intestinului, cu evoluţie ondulantă, cu perioade de activitate și de remisiune, dominată de inflamaţia intestinală.
Diagnosticul BC are la bază tabloul clinic, la care se adaugă examinările endoscopice, histopatologice, imagistice și biologice.
Nu există teste specifice de diagnostic. Explorările utilizate sunt destinate, în principal, precizării diagnosticului pozitiv al BC, a formei anatomoclinice de boală și a activităţii bolii, a complicaţiilor.  În același timp, investigaţiile servesc la diferenţierea BC de colita ulcerativă (CU), precum și la diferenţierea de alte entităţi anatomoclinice cu afectare intestinală (alte colite din afara spectrului bolilor inflamatorii intestinale de cauză neprecizată) și de sindromul de intestin iritabil. În ţările cu prevalenţă ridicată a tuberculozei, trebuie exclusă tuberculoza intestinală (1–4).
În același timp, investigaţiile servesc la diferenţierea BC de colita ulcerativă (CU), precum și la diferenţierea de alte entităţi anatomoclinice cu afectare intestinală (alte colite din afara spectrului bolilor inflamatorii intestinale de cauză neprecizată) și de sindromul de intestin iritabil. În ţările cu prevalenţă ridicată a tuberculozei, trebuie exclusă tuberculoza intestinală (1–4).
La primul diagnostic al BC, precum și la evaluările periodice, biomarkerii de activitate ai BC sunt utilizaţi ca semne de boală intestinală activă și sunt analizaţi în corelaţie cu constatările endoscopice și imagistice. Aceștia pot fi utilizaţi, ulterior, ca markeri noninvazivi de monitorizare a activităţii bolii (1–4).
Examinările biologice din sânge sunt destinate identificării unui sindrom inflamator, a unor carenţe secundare malabsorbţiei sau pierderilor digestive, a unor complicaţii și a unor markeri serologici care au fost asociaţi cu BC (ASCA/pANCA). Examenul de scaun poate identifica markeri de inflamaţie nespecifici (calprotectină, lactoferină) și trebuie să excludă infecţiile (tabelul 1) (1, 2).
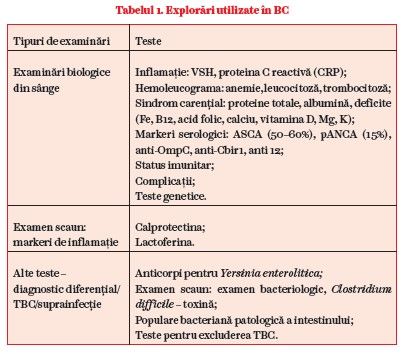
Calprotectina este un constituent al citosolului leucocitelor neutrofile. Calprotectina fecală a fost recunoscută ca marker de inflamaţie a mucoasei intestinale. Dozarea calprotectinei fecale pare să se impună ca test noninvaziv de monitorizare a evoluţiei bolilor intestinale inflamatorii, BC și CU, sub tratament și pentru selectarea pacienţilor care au nevoie de alte investigaţii.
Modificările calprotectinei fecale au fost asociate pozitiv cu variabilitatea evoluţiei bolii intestinale (BC și CU). Calprotectina fecală a fost corelată cu modificările endoscopice și histopatologice de inflamaţie, active. Mai mult, s-a constatat o creștere a calprotectinei fecale premergătoare unui puseu acut de activitate a bolii, clinic manifest, atât în BC, cât și în CU (1).
Utilizarea potenţială a testelor din scaun, noninvazive, de inflamaţie intestinală, are o importanţă particulară în contextul în care scopul tratamentului în BC a evoluat de la rezultatele tratamentului bazate pe simptom la rezultatele tratamentului asupra inflamaţiei la nivel tisular – vindecarea mucoasei (1). Deși asemenea teste de inflamaţie intestinală, efectuate din scaun, pot fi mai sensibile decât testele din sânge, ele rămân grevate de nespecificitate și necesită interpretare în context. Excluderea infecţiilor și a malignităţii este necesară în toate etapele de evaluare (1).
Markerii serologici ai bolilor inflamatorii de cauză neprecizată (BC și CU) s-au dovedit utili pentru diagnostic, clasificare (BC vs. CU), diferenţierea de alte colite, de sindromul de intestin iritabil și în aprecierea prognosticului.
Au fost descriși mai mulţi markeri serologici (1). Cei mai utilizaţi sunt reprezentaţi de ASCA și pANCA (tabelul 1). La primul diagnostic de boală inflamatorie intestinală de cauză neprecizată (BC sau CU), markerii serologici pot oferi informaţii suplimentare diagnostice, în contextul clinic și al constatărilor endoscopice și radiologice. În același timp, markerii serologici nu prezintă o acurateţe suficientă pentru diagnostic, cu valoare independentă și nu sunt utilizaţi în screening (1).
Profilul serologic al BC a fost asociat cu prognosticul BC, cu complicaţiile și cu evoluţia postchirurgicală. Un nivel crescut al markerilor serologici a fost asociat cu riscul de boală stenozantă și/sau fistulizantă și cu riscul de recidivă a BC după intervenţie chirurgicală (1). Profilul serologic al BC a fost asociat și cu genele de susceptibilitate specifice, precum mutaţiile NOD2. Markerii genetici au fost asociaţi cu severitatea bolii și cu un risc evolutiv spre forma fibrozantă/stenozantă a BC (1).
Proteina C reactivă (CRP) și viteza de sedimentare a hematiilor (VSH) pot să nu prezinte valori crescute la pacienţii cu BC. Creșterea CRP a fost asociată cu semnele clinice, endoscopice și histologice de activitate a BC. Alţi markeri de inflamaţie acută pot deriva din estimarea leucocitelor, feritinei (1).
Examenul anatomopatologic a contribuit esenţial la conturarea BC. Conform definiţiei, în BC, localizarea de elecţie este reprezentată de ileonul terminal. Alte localizări posibile sunt reprezentate de colon, rect, anus, jejun, duoden, stomac, esofag. Distribuţia leziunilor este segmentară, discontinuă. La examenul macroscopic, leziunile sunt polimorfe. La examenul histopatologic, inflamaţia este transmurală. Granulomul epiteloid, fără cazeificare, considerat o marcă a BC, poate fi identificat la 30–60% din cazuri.
Există diferenţe între rezultatele examenului anatomopatologic realizat pe un eșantion de biopsie endoscopică, faţă de examenul histopatologic al piesei de rezecţie chirurgicală. Examenul anatomopatologic realizat pe eșantionul de biopsie endoscopică oferă informaţii detaliate privitoare la inflamaţie: infiltrat inflamator limfoplasmocitar, hiperplazie limfoidă focală, abcese criptice, fibroză. Granulomul epiteloid fără cazeificare este rar constatat. Examenul anatomopatologic realizat pe piesa de rezecţie chirurgicală oferă informaţii mai complexe: caracterul transmural al inflamaţiei, prezenţa/absenţa granulomului epiteloid fără cazeificare, ulceraţii de tip aftoid, ulcere lineare profunde, fisuri profunde. Intestinul prezintă perete îngroșat, lumen îngustat, ganglionii sunt măriţi de volum, mezenterul este îngroșat/scurtat, prezenţa/absenţa de stenoze, fistule.
Pentru multe dintre aspectele morfologice care conturează cadrul anatomoclinic al BC există în prezent și alte examinări orientative, reprezentate de endoscopie și imagistică.
Scorurile sintetice de apreciere a activităţii BC au apărut ca o necesitate, pentru diagnosticul bolii active și monitorizarea rezultatului tratamentului (5). Aceste scoruri au evoluat de la cele bazate predominant pe parametri clinici (5) la cele bazate pe metodele de diagnostic morfologic dezvoltate în timp, endoscopice și imagistice (6–12). Capsula endoscopică oferă posibilitatea unui bilanţ lezional macroscopic la nivelul intestinului subţire (9, 11, 12). Noile metode imagistice aduc informaţii majore pentru diagnostic prin aprecieri privitoare la extinderea BC, caracterul transmural al leziunilor, confirmarea/excluderea complicaţiilor și a manifestărilor extraintestinale (7, 8). Dublate de tehnici suplimentare, metodele imagistice actuale oferă și date privitoare la activitatea inflamatorie la nivelul leziunii (1, 2, 7–9, 11, 12).
Pentru aprecierea sintetică a activităţii BC au fost create scoruri compozite. Scorul de activitate al bolii Crohn, CDAI (Crohn Disease Activity Index), este un asemenea scor, cu utilizare în studiile clinice, dar și în practica curentă, pentru evaluarea rezultatelor tratamentului. Scorul utilizează o sumă de simptome clinice subiective și derivate din examenul obiectiv al pacientului și un parametru derivat din explorările biologice, nivelul hemoglobinei (5).
Numărul de simptome prezente la pacient este multiplicat cu un factor de importanţă acordat fiecărei categorii dintre manifestările monitorizate. Un scor total până în 150 caracterizează o boală inactivă clinic. Un scor total de mai mare de 150 caracterizează o boală activă (tabelul 2) (1, 5).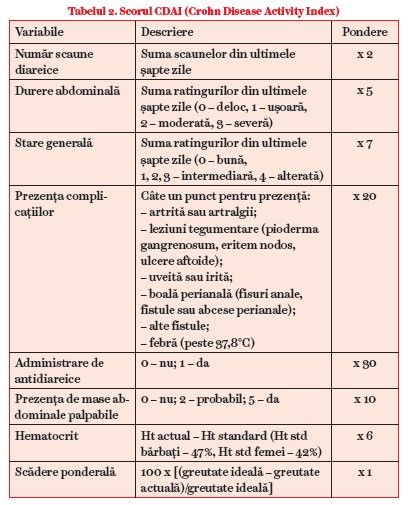
Scorul CDAI are limite deoarece nu încorporează biomarkeri de activitate inflamatorie/lezională serici și din scaun și nici activitatea endoscopică și tisulară, care reprezintă noile ţinte ale tratamentului.
Au fost propuse scoruri noi, care tind să încorporeze leziunile endoscopice, precum și inflamaţia de la nivel tisular evaluată imagistic (1, 6–12).
Biomarkerii fecali de inflamaţie pot prezenta o importanţă particulară, ca markeri noninvazivi de inflamaţie intestinală, cu utilitate în diagnosticul puseurilor acute ale BC, la selectarea pacienţilor pentru investigaţii complementare și la monitorizarea rezultatelor terapeutice (7, 9–11).
1.Melmed GY et al. Crohn’s disease: clinical manifestations and management. In: Yamada’s Tetbook of Gastroenterology. 5th ed. Podolski DK et al. (eds). Wiley-Blackwell, Oxford, 2016
2.Travis SPL et al. Gastroenterology. 3rd ed. Blackwell, Oxford, 2005
3. Gheorghe L, Gheorghe C. Bolile inflamatorii intestinale. In: Tratat de Gastroenterologie, vol. 2. Grigorescu M (ed.). Editura Medicală Naţional, București, 2001
4. Dejica D. Boli inflamatorii intestinale. In: Tratat de Gastronterologie Clinică, vol. 1. Grigorescu M, Pascu O (eds.). Editura Tehnică, București, 1996
5. Best WR et al. Development of a Crohn’sdisease activity index. National cooperative Crohn’s disease study. Gastroenterology. 1976;70:439-44
6. Mary JY et al. Development and validation of an endoscopic index of the severity for Crohn’s disease: a prospective multicenter study. Gut. 1989;30:983-9
7. D’Inca R et al. Measuring disease activity in Crohn’s disease: what is currently available to the clinician. Clin Exp Gastroenterol. 2014 May 20;7:151-61
8. Domachevsky L et al. Correlation of 18F-FDG PET/MRE metrics with inflammatory biomarkers in patients with Crohn’s disease: a pilot study. Contrast Media Mol Imaging. 2017 Sep 19;2017:7167292
9. Shitrit ABG et al. A prospective study of fecal calprotectin and lactoferrin as predictors of small bowel Crohn’s disease in patients undergoing capsule endoscopy. Scand J Gastroenterol. 2017 Mar;52(3):328-33
10. Ministro P et al. Fecal biomarkers in inflammatory bowel disease: how, when and why? Expert Rev Gastroenterol Hepatol. 2017 Apr;11(4):317-328
11. Kopylov U et al. Fecal calprotectin for the prediction of small-bowel Crohn’s disease by capsule endoscopy: a systematic review and meta-analysis. Eur J Gastroenterol Hepatol. 2016 Oct;28(10):1137-44
12. Niv Y et al. Capsule Endoscopy Crohn’s Disease Activity Index (CECDAIic or Niv Score) for the Small Bowel and Colon. J Clin Gastroenterol. 2018 Jan;52(1):45-9
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe