
Interviu cu prof. dr. Ion-Christian Chiricuţă
Continuăm serialul privind protonoterapia, în care profesorul Chiricuţă, expert de nivel internaţional în radioterapie, cu preocupări legate de protonoterapie, face un scurt istoric al acestei terapii, explicând etapele parcurse de la începuturile ei până astăzi, precum și avantajele acesteia comparativ cu alte metode de iradiere.
Demersul nostru a pornit de la faptul că, în urmă cu aproximativ două săptămâni, Gabriela Firea, primarul general al Capitalei, a anunţat că la București va fi construit un centru modern de terapie cu protoni pentru tratarea bolnavilor de cancer.
Cum s-a ajuns ca această iradiere cu fascicul de protoni să fie folosită și în medicină?
Totul a început în anul 1946, odată cu publicarea de către fizicianul Robert Rathbun Wilson, în revista Radiology (SUA), a unui articol cu referire la bazele fizice ale unei posibile terapii a cancerului cu ajutorul protonilor (Wilson RR. Radiological use a fast protons. Radiology. 1946;47:487–91). Robert R. Wilson a lucrat cu Robert Oppenheimer la conceptul bombelor atomice, în cadrul proiectului Manhattan, care a dus în final la lansarea atacurilor atomice la Nagasaki și Hiroshima, contribuind astfel la scurtarea și terminarea celui de-al Doilea Război Mondial. Fizicianul Wilson a lucrat în domeniul absorbţiei diferitelor radiaţii în materiale.

Cercetările sale au continuat, iar în acel an – 1946 – a publicat lucrarea care a stat la baza aplicării protonilor în terapia cancerului.
Când a fost tratat primul pacient prin această metodă?
În 1961, la centrul cu protoni de la Harvard. Nu trebuie uitat că primul copil tratat, cu ajutorul acceleratorului linear de data aceasta, este Gordon Isaak, în 1956. El avea 2 ani când a fost tratat la centrul de la Stanford, unde Henry Kaplan și fizicianul Mitchell Weisbluth au coordonat primele tratamente.

Patruzeci de ani mai tarziu, acest pacient era în viaţă, fără a avea vederea afectată de tratament.
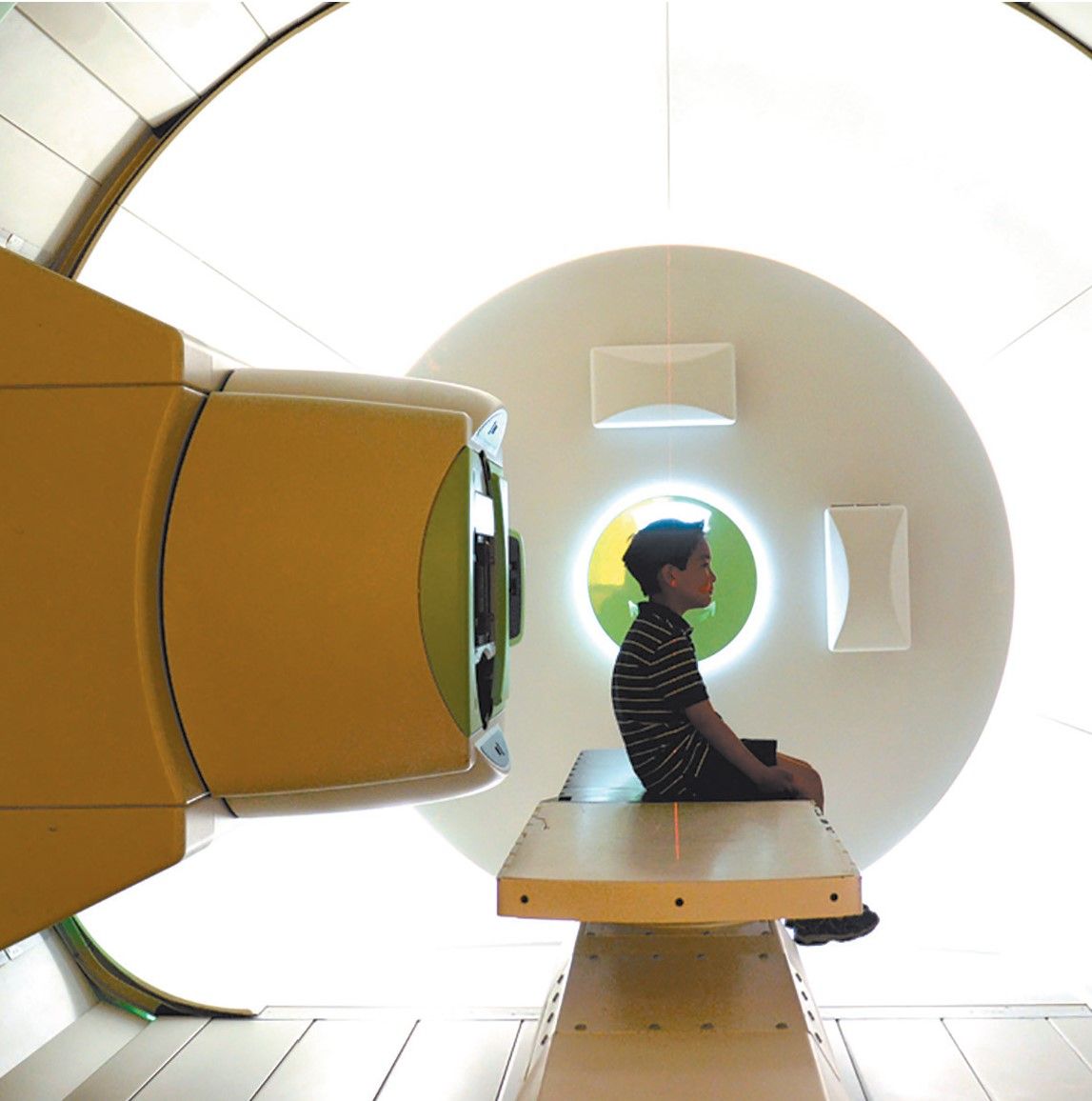
În imaginile alăturate sunt arătaţi cei doi copii aflaţi pe mesele de iradiere ale primului accelerator liniar și a capului de iradiere cu protoni.
Vorbiţi de copii. Copilul nu este un adult, care să înţeleagă ce se întâmplă cu el. Cum pot fi ei implicaţi în acest proces complicat al vindecării?
Este mai greu, dar se pot găsi soluţii. Am văzut, în urmă cu vreo 15 ani, la Centrul Cancerului MD Anderson, că s-a creat o cameră specială în care copiilor le sunt oferite jocuri în scop medical. Prin joc, ei înţeleg cum acţionează razele, cum se omoară celula tumorală. O idee interesantă mi s-a părut Proton Man, o creaţie a lui Bill Hansen și a graficianului Mike Jaszewski.

Este o poveste virtuală special creată pentru centrele în care copiii sunt trataţi cu ajutorul protonoterapiei. Copiii devin ei înșiși Proton Man, eroul care de fiecare dată omoară celulele tumorale; este un factor psihic de susţinere extraordinar, pentru că ei se culcă seara știind că au omorât mii de celule tumorale. Astfel, copiii sunt implicaţi în procesul vindecării, sunt pregătiţi pentru stările prin care vor trece: vărsături, diaree, pierdere în greutate. Și, cel mai important, au convingerea că tot timpul vor câștiga lupta cu celula tumorală.
Care a fost drumul parcurs în dezvoltarea acestor instalaţii?
Construirea unor instalaţii ce pot trata un număr mai mare de pacienţi a trecut prin trei etape distinctive. În prima etapă (1960–1990), aceste instalaţii aveau iniţial ca scop principal cercetarea, ulterior au fost adaptate, făcând posibilă și iradierea pacienţilor. Din 1990 până prin 2010 a fost parcursă etapa a doua, și anume conceperea și construcţia de centre de protoni, adaptate profilului investitorului, clinicii care finanţa proiectul. În ultimul deceniu au apărut și sisteme compacte de protonoterapie. Actualmente ne aflăm în cea de-a treia perioadă a dezvoltării protonoterapiei.
Ce definește această etapă în care ne aflăm?
În această etapă au apărut centrele de terapie cu protoni compacte, ca rezultat al cercetării și finanţării susţinute de firmele producătoare de aparatură cu tehnologie avansată. Dar tehnica de producere a unor fascicule omogene energetic este și rezultatul contribuţiei altor domenii, precum imagista medicală cu computer tomograf și rezonanţă magnetică nucleară, dar și al exactităţii cu care se poate calcula un plan de iradiere. Toate acestea fac posibilă calitatea terapiei cu ajutorul protonilor.
La care se adaugă o doză cât mai bine calculată.
Desigur. Doza aplicată la nivelul tumorii maligne, precis calculată, reduce mult efectele secundare, în comparaţie cu iradierea cu fotoni. Acest lucru se datorează proprietăţilor fasciculului cu protoni, acea energie care stă la baza fenomenului de destrucţie celulară tumorală, eliberată în profunzime (Bragg peak), ce nu afectează ţesuturile din faţa tumorii și nici pe cele din spatele ei. Inducerea de tumori secundare, care încă sunt o problemă în cazul radioterapiei cu fotoni, este și ea redusă prin utilizarea protonilor.
Care este tumora cu cea mai mare adresabilitate la această terapie?
În general, majoritatea copiilor diagnosticaţi cu o tumoră au vârsta până în zece ani și au o tumoră cerebrală sau un sarcom. Meduloblastomul este tumora cu cea mai mare frecvenţă la multe centre de tratament. În anul 2013, de exemplu, au fost trataţi 105.743 de pacienţi prin protonoterapie, din care 17.829 numai în Centrul de la Loma Linda (SUA). În acel an, în SUA au fost trataţi cu protonoterapie 736 de copii cu tumori maligne.
Statisticile arată un trend crescător al numărului copiilor și adolescenţilor care se adresează centrelor de protonoterapie.
Așa este. Într-o lucrare de sinteză publicată în Japonia (Proton beam therapy for pediatric malignancies: a retrospective observational multicenter study in Japan) – o analiză retrospectivă a situaţiei protonoterapiei în patru centre japoneze – sunt analizate multiplele aspecte ale acestei noi și promiţătoare terapii (Cancer Medicine, 2016). Din datele prezentate se remarcă creșterea numărului de cazuri tratate cu protonoterapie în oncopediatrie.
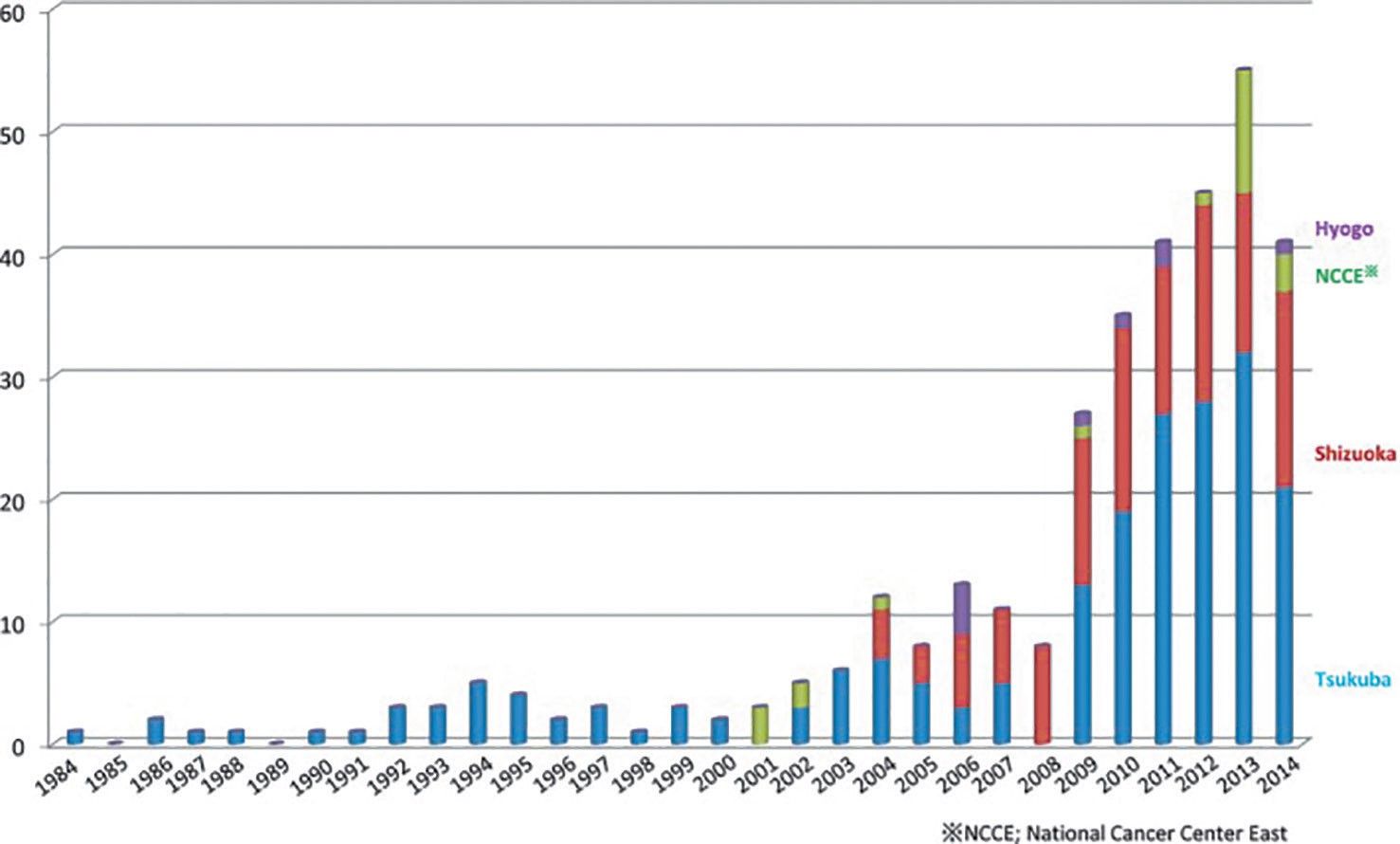
Este ușor de observat cum numărul copiilor și adolescenţilor ce se adresează unui asemenea centru este în continuă creștere. În Statele Unite chiar funcţionează o asociaţie, sub numele de Pediatric Proton Foundation, care coordonează multiplele activităţi necesare strângerii de date referitoare la succesul terapiei, dar și a datelor legate de efecte adverse. În anul 2014, numărul copiilor cu tumori cerebrale și tumori la nivelul măduvei spinării trataţi în centrele de protonoterapie a crescut cu 36%, comparativ cu anul 2010.
Exemplificarea celor relatate mai sus este aratată în figura de mai jos, unde se compară cele două tehnici de iradiere uzuale astăzi în oncopediatrie: protonoterapia și iradierea cu tehnica IMRT (intensitate modulată) cu acceleratorul liniar.
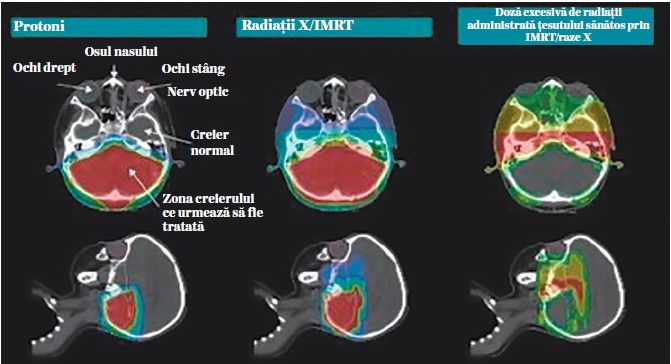
În coloana din stânga este reprezentată tehnica de iradiere cu protoni, în coloana din mijloc – iradierea cu fotoni –, iar în coloana din dreapta este reprezentată diferenţa în doza aplicată la nivelul ţesuturilor normale înconjurătoare. Avantajul radioterapiei cu protoni în aceste cazuri este evidentă. Regiunile colorate din coloana din dreapta sunt iradiate în plus dacă iradierea este efectuată cu fotoni.
În cazul meduloblastomului (tumoră frecventă la copii), radioterapia trebuie aplicată pe un volum mare, și anume la nivelul sistemului nervos central, inclusiv al întregului spaţiu ocupat de lichidul cefalorahidian din canalul medular, la nivelul măduvei spinale și cisternelor intracraniene, având ca scop și iradierea spaţiului în care s-ar afla celule tumorale.
În figura alăturată este exemplificată diferenţa de volum iradiat (zona colorată cu verde deschis), mai mult în cazul iradierii unui copil cu meduloblastom, prin cele două metode disponibile: protonoterapia și iradierea cu fotoni la accelaratorul liniar. 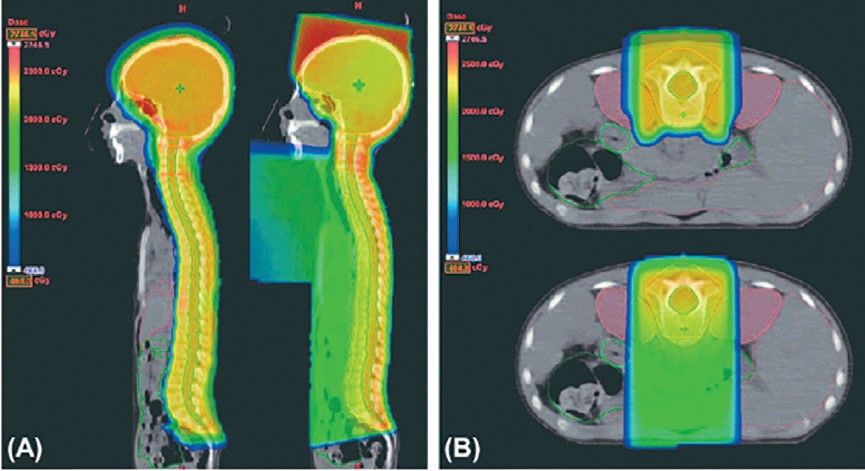
Planul de iradiere a fost calculat pentru iradierea cu protoni (prima din stânga în figura A și cea de sus în figura B) și un plan de iradiere ce ar fi efectuat cu fotoni (imaginea din dreapta în figura A și cea de jos în figura B).
Culoarea verde deschis arată volumul pacientului iradiat cu o doză suplimentară, care în cazul radioterapiei cu protoni nu este deloc iradiată.
Într-o lucrare publicată de grupul condus de Mizumoto Masashi în anul 2016 este raportată o reducere a dozei de radiaţii aplicate la nivelul creierului sănătos între 28% și 64% (în medie, 47%) prin protonoterapie faţă de doza aplicată prin fotonoterapie (accelerator liniar).
La pacienţii cu craniofaringiom este raportată de grupul condus de César Beltrán o reducere a dozei aplicate la nivelul întregului creier cu 22% și a dozei în întregul corp cu 43%.
Terapia cu protoni este preferată în numeroase tipuri de cancer pediatric, inclusiv în:
• Astrocitomul anaplazic
• Tumorile rhabdoide/teratoide atipice
• Cordom
• Craniofaringiom
• Tumori desmoide
• Ependimon
• Sarcom Ewing
• Glioame, inclusiv glioamele căilor vizuale/hipotalamice, oligodendroglioame, oligoastrocitoame
• Glioblastomul
• Tumori intracraniene provenind din celule germinative (germinoame)
• Angiofibroame juvenile
• Limfoame
• Meduloblastom
• Meningiom
• Carcinom nesofaringean
• Neuroblastom
• Osteosarcom
• Pineoblastom
• Retinoblastom
• Rhabdomiosarcom
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe