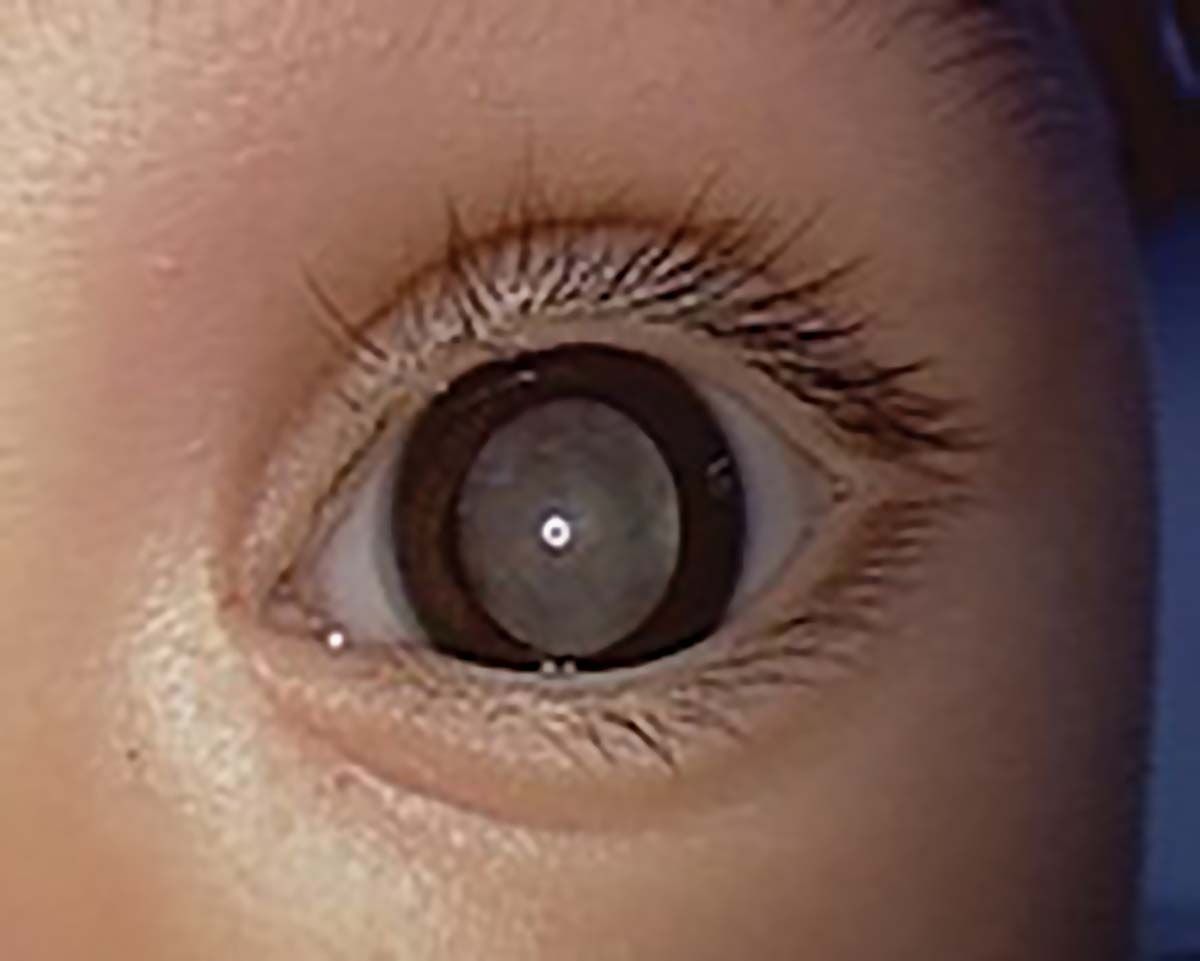
Formele severe de ROP pot afecta copiii născuţi prematur. Netratate, pot duce inclusiv la orbire. Astfel, toţi copiii din grupa de risc trebuie să beneficieze de screeningul ROP.
Retinopatia de prematuritate (ROP) este una dintre cele mai frecvente cauze de deficienţe de vedere la copilul mic, dar care poate fi prevenită și tratată (1-3). Majoritatea copiilor născuţi prematur dezvoltă un grad mediu sau minor de ROP, care se vindecă spontan (4). Însă unii prematuri pot dezvolta forme severe care, netratate, pot duce la deficienţe majore de vedere, inclusiv la orbire, motiv pentru care toţi copiii din grupa de risc trebuie să beneficieze de screeningul ROP (5-8). Pe lângă pierderea vederii, ROP poate determina și alte tulburări vizuale, respectiv reducerea sensibilităţii de contrast, afectarea câmpului vizual, defecte ale vederii cromatice, strabism, vicii de refracţie, ambliopie (9-11).
Vascularizarea retinei este indusă de factori de creștere vasculari, respectiv VEGF, stimulaţi de către „hipoxia fiziologică” intrauterină. Apariţia ROP este explicată prin succesiunea a două faze (12):
Se poate vorbi de trei „epidemii” ale ROP. Prima „epidemie” a apărut în perioada 1940-1950, odată cu utilizarea oxigenului (O2) nemonitorizat în tratamentul detresei respiratorii la prematuri, ROP fiind atunci cea mai importantă cauză de orbire la copii în ţările dezvoltate (14). Cel de-al doilea vârf a apărut în anii ’70, odată cu apariţia unităţilor de terapie intensivă neonatală, situaţie care a fost controlată prin îmbunătăţirea îngrijirilor neonatale și prin introducerea tratamentului prin crioterapie și ulterior laserterapie (15,16).
Îmbunătăţirea standardului îngrijirilor neonatale în ultimele două decenii în ţările mediu dezvoltate și creșterea ratei de supravieţuire a prematurilor a dus la apariţia celei de-a treia „epidemii” în aceste ţări (17). Ţările mediu dezvoltate au cea mai mare incidenţă a ROP din lume, 75% dintre cazurile de ROP provenind din aceste zone, întrucât doar 40% dintre unităţi au programe de screening pentru ROP implementate și funcţionale (3).
Copiii din ţările mediu dezvoltate care fac forme de ROP severe au vârsta gestaţională (VG) și greutatea la naștere (GN) mai mari comparativ cu cei din ţările dezvoltate. Din acest motiv, este obligatorie existenţa unui Ghid Naţional pentru screening și tratament al ROP pentru fiecare ţară, în funcţie de datele locale (23,24).
Factorul de risc cel mai important este prematuritatea, incidenţa ROP crescând odată cu scăderea VG și a GN (7). Multiple studii au asociat ROP severă cu tensiunea arterială ridicată a O2, fluctuaţiile gazelor sanguine, crizele de apnee, administrarea de surfactant, ventilaţia asistată, displazia bronhopulmonară (29), sepsisul, infecţia fungică, curba ponderală postnatală inadecvată, transfuziile multiple, hiperglicemia, hemoragia intraventriculară (27-33).
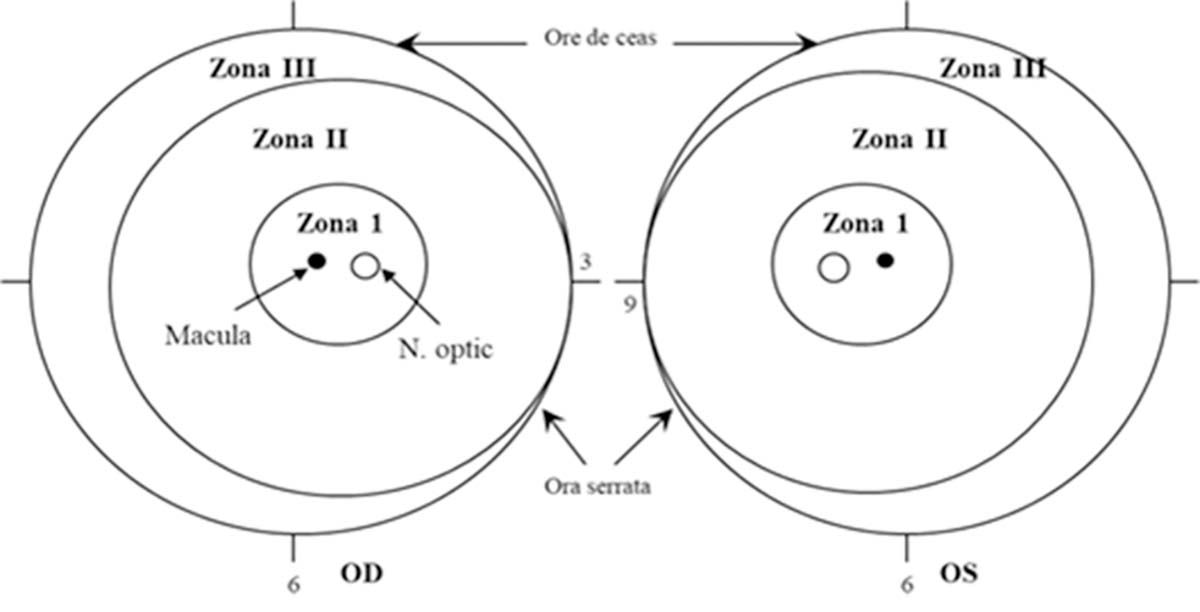
Conform Clasificării Internaţionale a ROP, aceasta este descrisă în funcţie de stadiu (5 stadii), de zonă, extindere, prezenţa factorului plus. Au fost descrise trei zone concentrice centrate pe discul optic (Figura 1) (1).
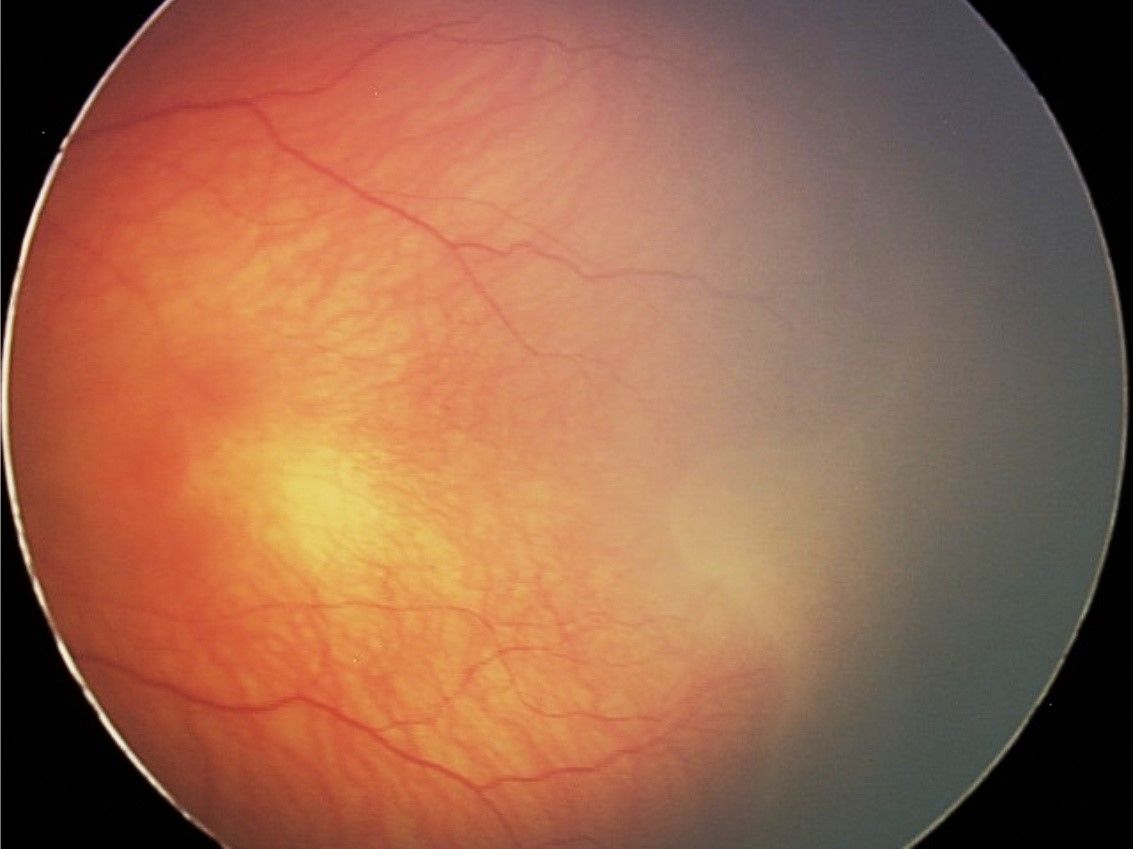
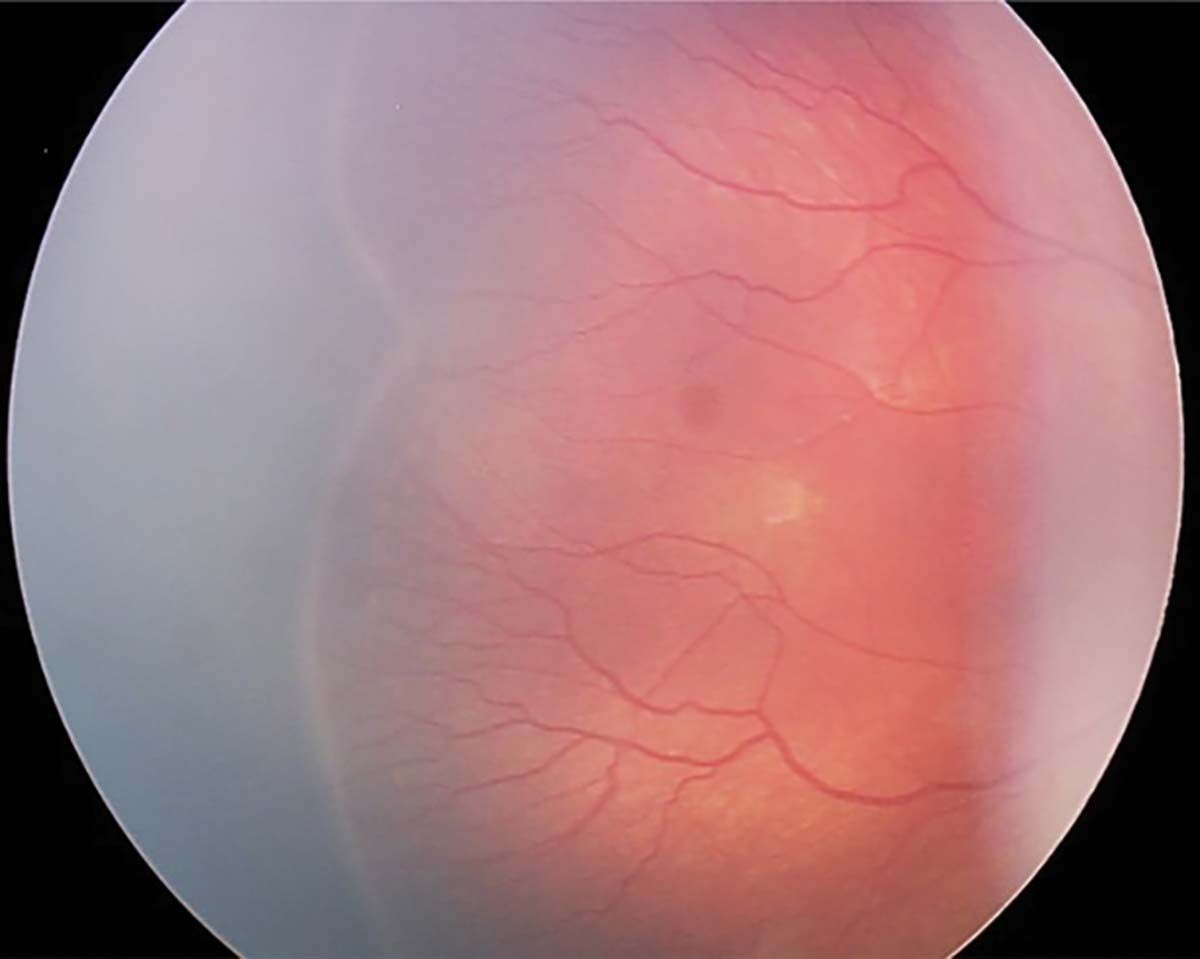
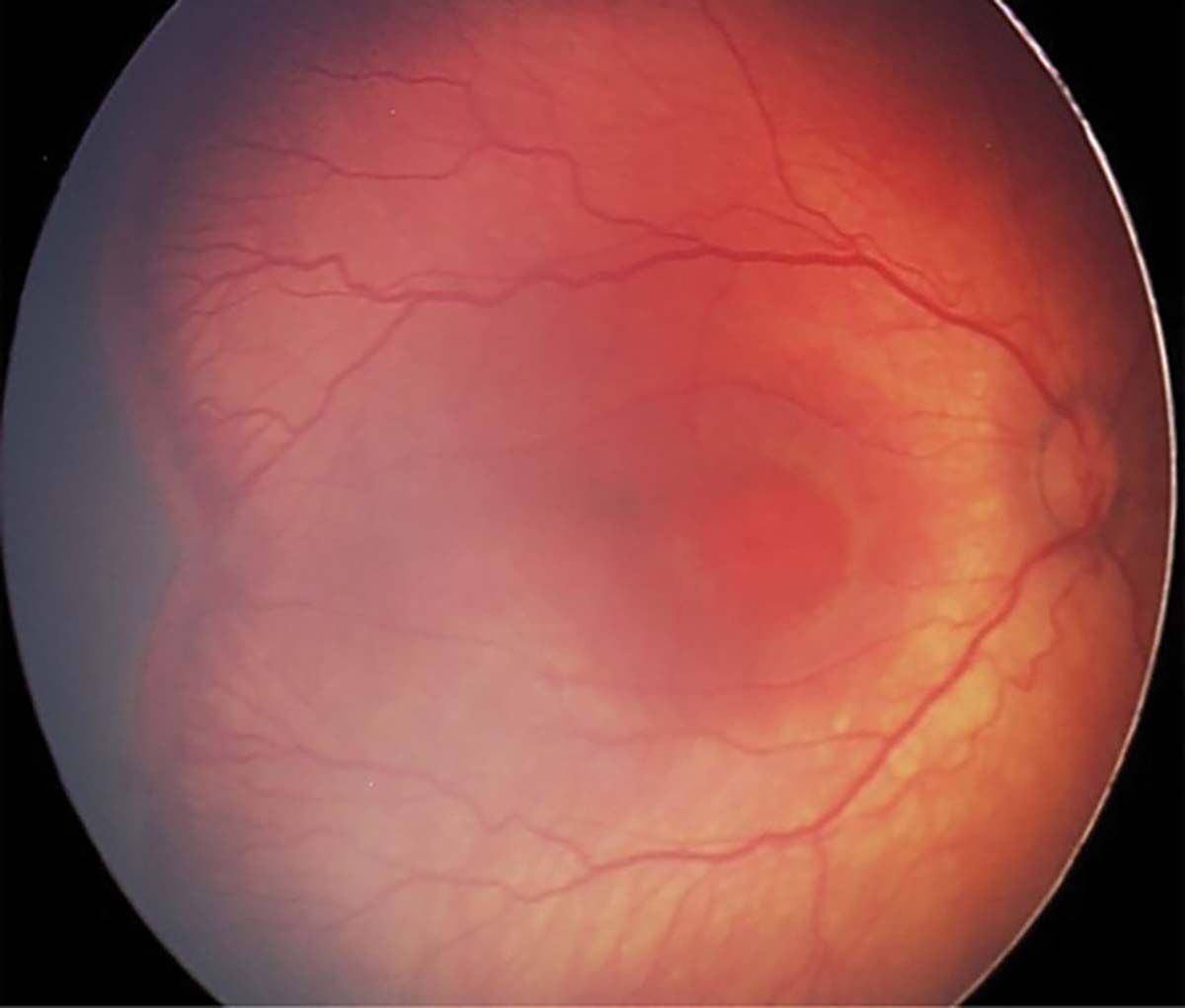
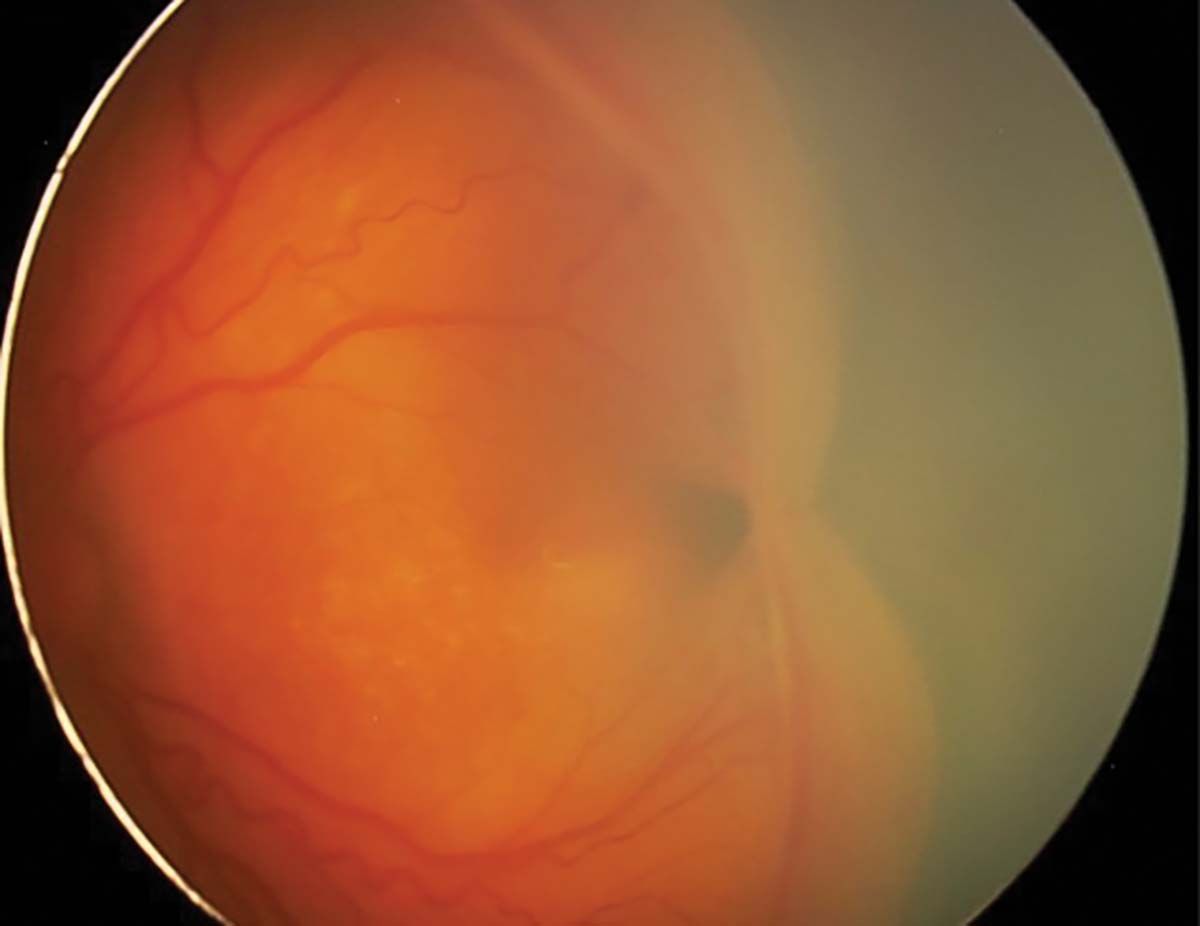
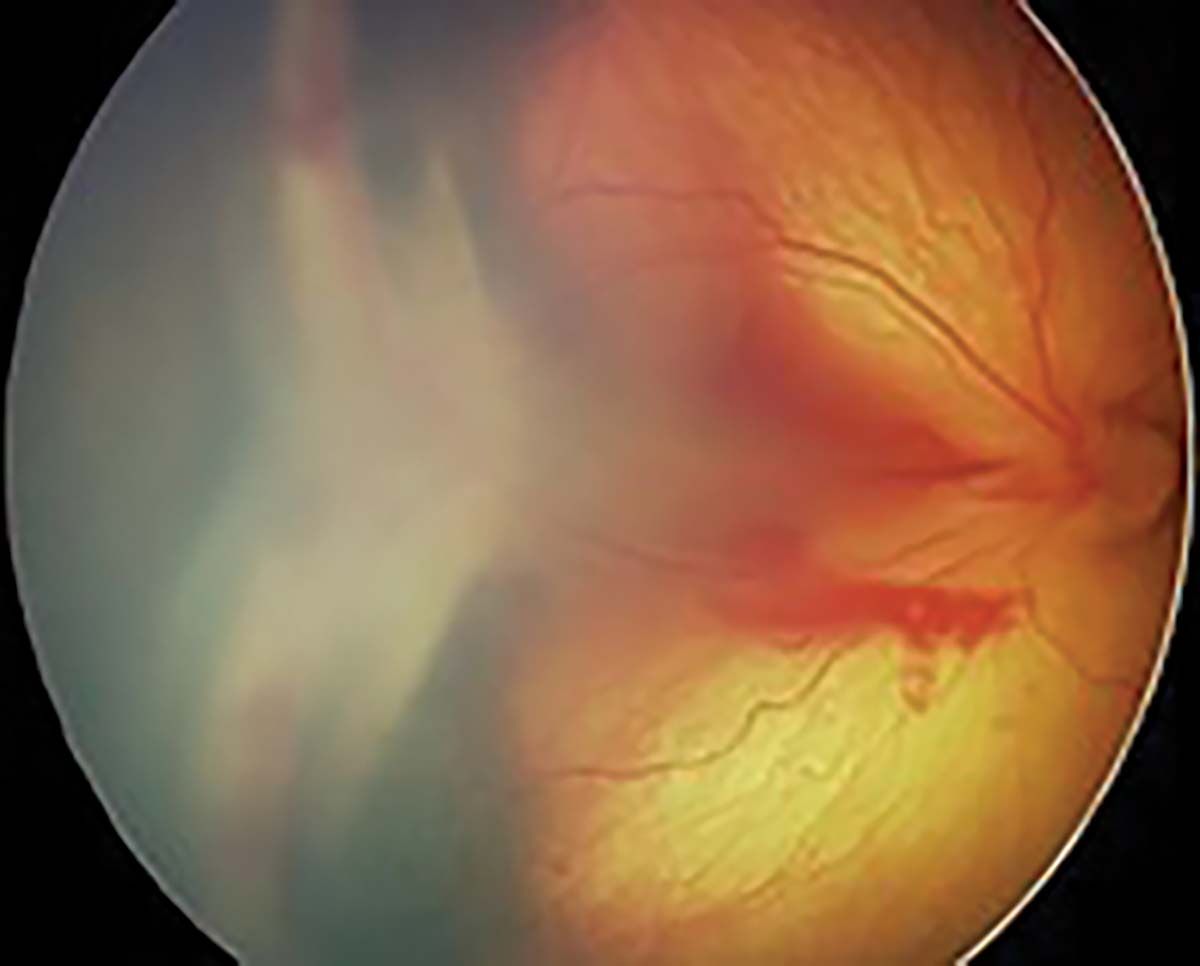
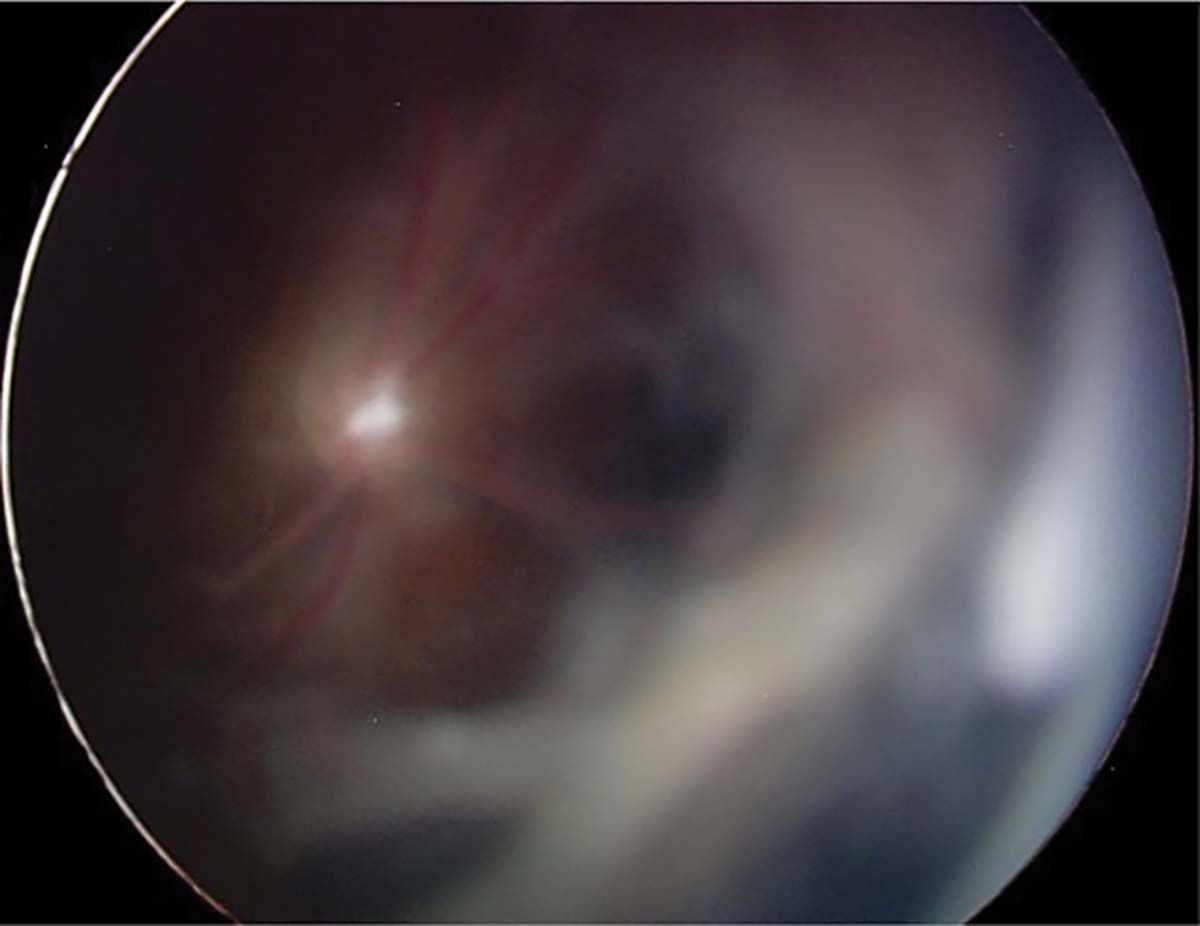
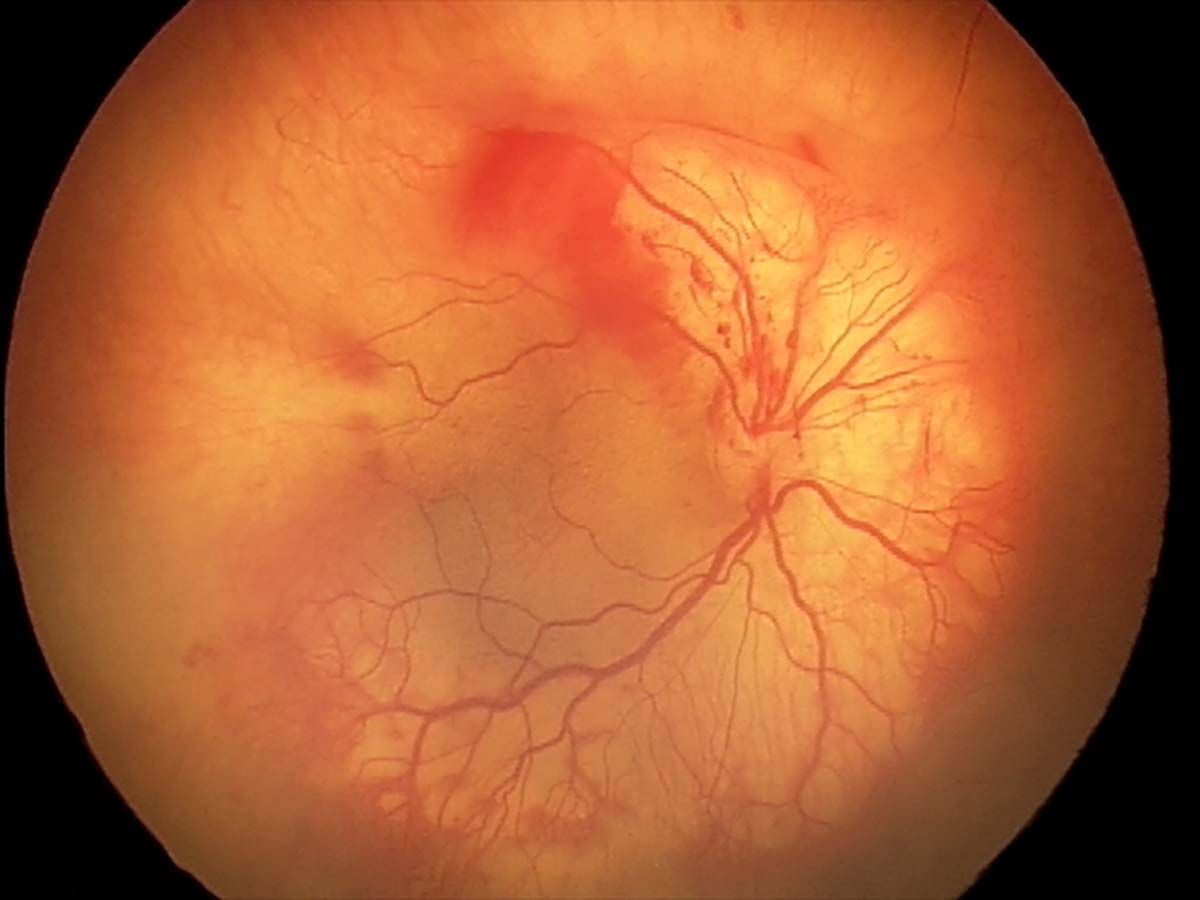
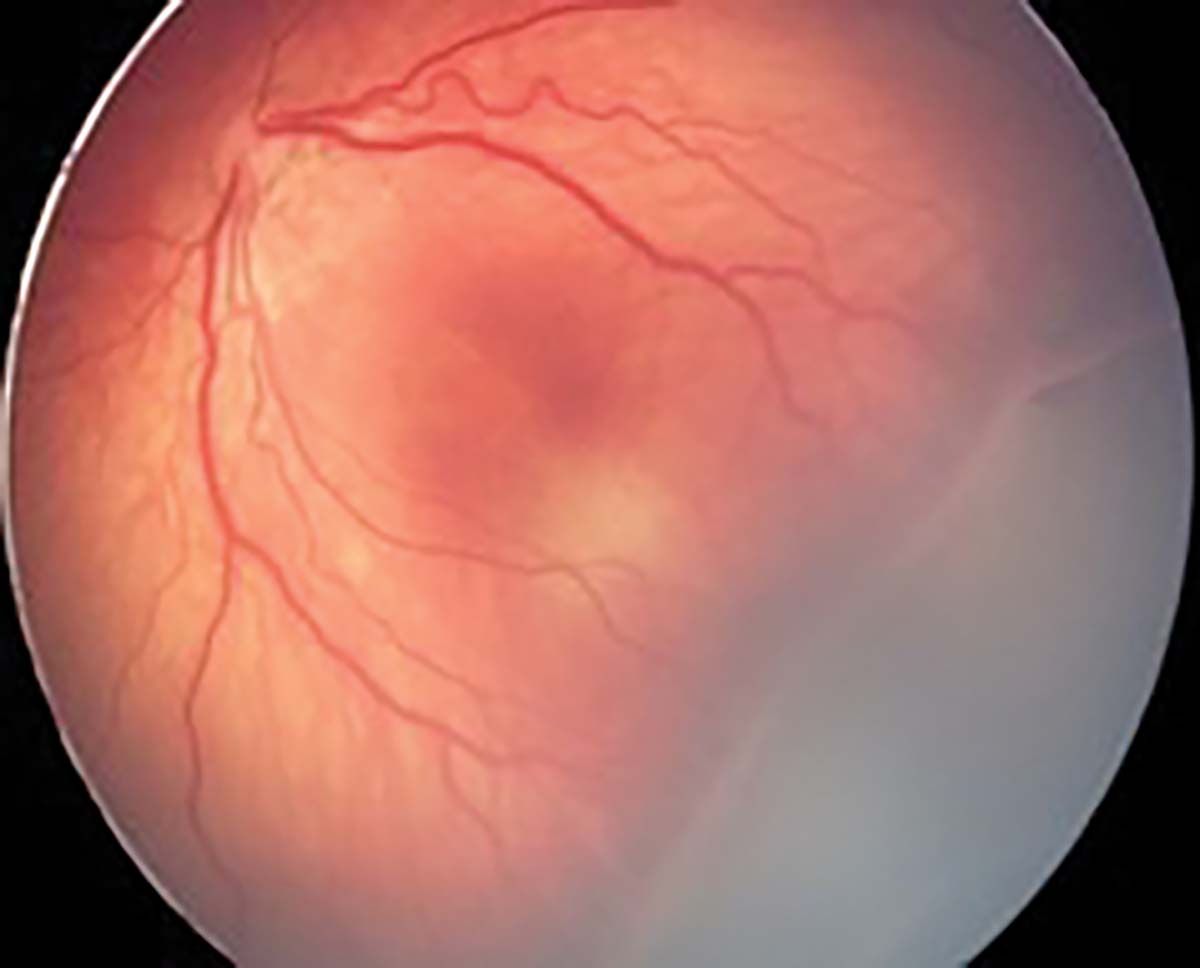
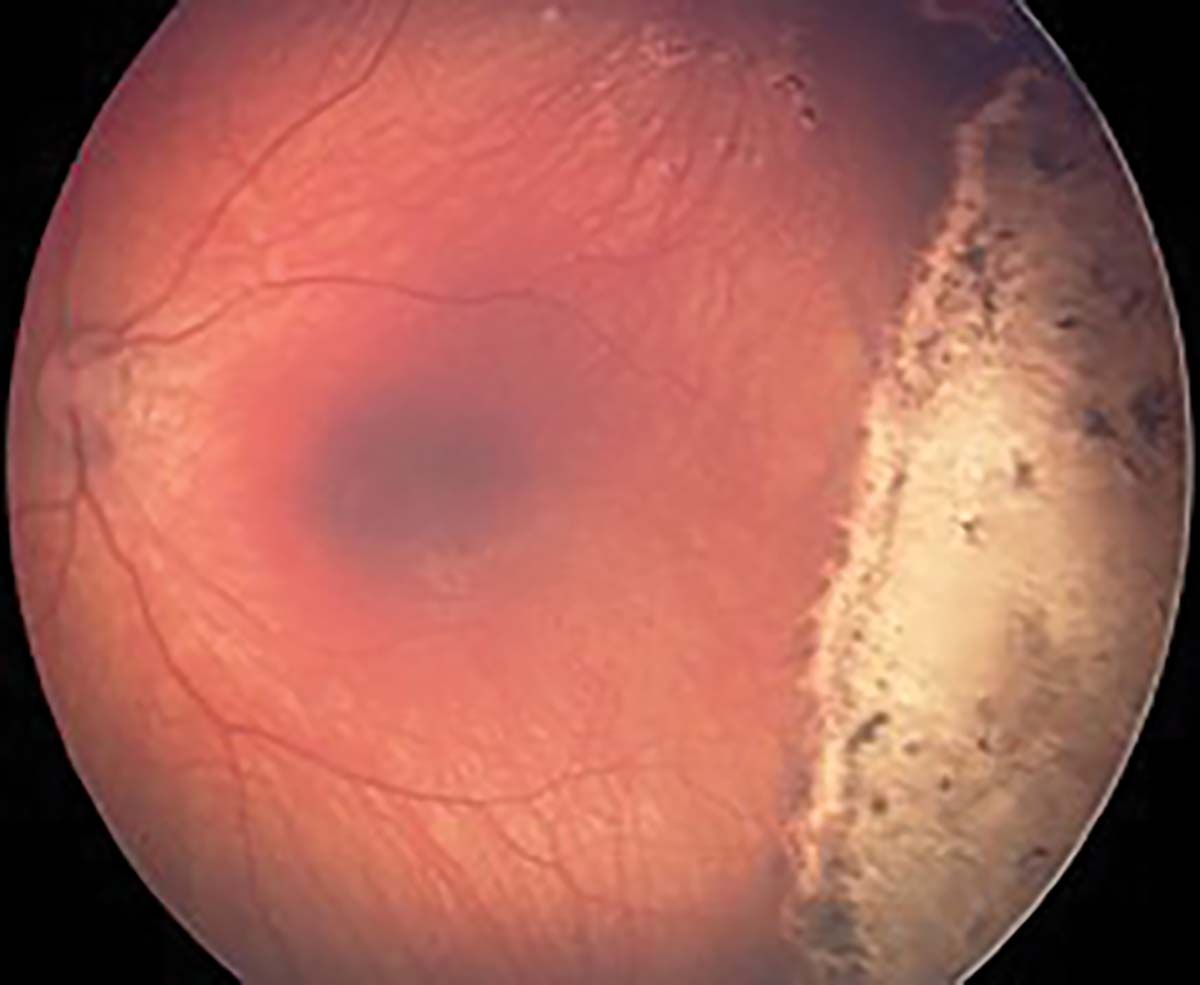
Stadiul 1 (Figura 2) este caracterizat de linia de demarcaţie ce separă retina avasculară de cea vasculară. În stadiul 2 (Figura 3), creasta înlocuiește linia de demarcaţie, iar în stadiul 3 (Figura 4) apare proliferarea extraretiniană sau neovascularizaţia, care proemină de la nivelul crestei în vitros. În lipsa tratamentului, evoluţia este către dezlipire de retină. Aceasta poate fi parţială – stadiul 4A, fără afectarea maculei, și 4B, cu afectarea maculei (Figurile 5 și 6) – sau totală (Figura 7), cu aspect de „pâlnie”. Aspectul final este de pupilă albă, respectiv leucocorie (Figura 8). În continuare, evoluţia este către cecitate absolută, respectiv pierderea percepţiei luminii.

Factorul plus („plus disease”) indică faptul că ROP este activă și severă. Include dilataţii venoase și tortuozităţi ale arterelor polului posterior în cel puţin două cadrane. Se poate însoţi de dilatare vasculară iriană, midriază insuficientă (rigiditate pupilară) și vitros tulbure (Figura 9).
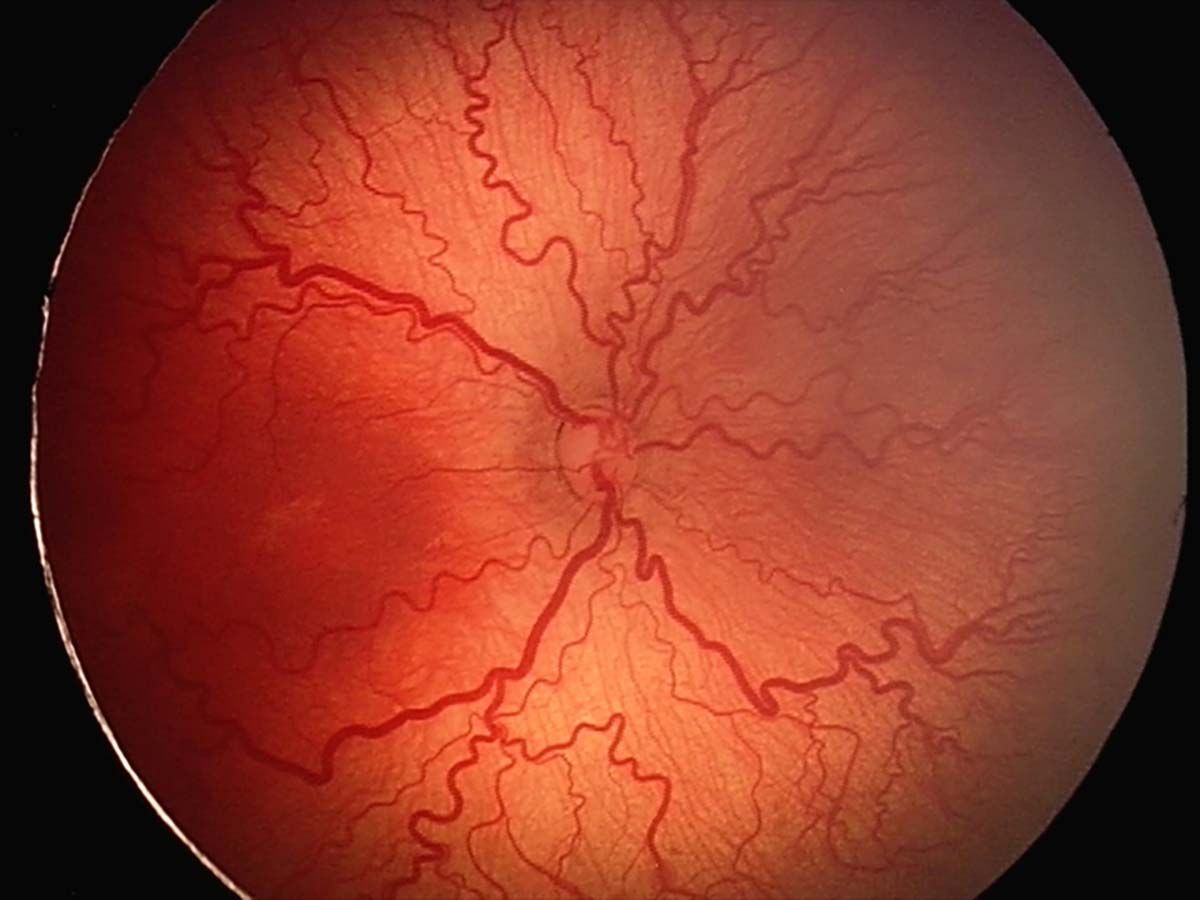
ROP forma agresivă este o formă severă, atipică, rapid progresivă, care fără tratament progresează rapid către stadiul 5 și care este asociată frecvent cu folosirea excesivă a O2 (34). De obicei, vascularizaţia este prezentă în zona I sau zona II posterior, cu factor plus important și șunturi vasculare. Caracterul atipic provine din faptul că evoluţia nu are loc de obicei prin stadiile 1-5 clasice și că neovascularizaţia retiniană este plată și dificil de vizualizat (1).
Intervenţia terapeutică are ca scop reducerea producţiei de VEGF de la nivelul retinei, care este responsabil de progresia bolii.
Tratamentul laser este în prezent, în toată lumea, tratamentul standard în ROP (5,8). Este indicat în ROP stadiul 3+ sau 2+ zona II, atunci când zona maculară este vascularizată. Aplicaţiile laser se fac la nivelul zonei avasculare, reducându-se astfel sursa VEGF (Figura 11). Laserterapia se face cu analgosedare sau în anestezie generală.
Anti-VEGF administrat intraocular (din anul 2010, în România se administrează bevacizumab) permite dezvoltarea vaselor retiniene către periferie și este un tratament salvator în formele de ROP agresive posterioare sau în ROP stadiul 3 în zona I, respectiv atunci când zona maculară nu este vascularizată, precum și pentru copiii instabili clinic, cu pupila rigidă, medii opace sau în caz de hemoragie retiniană extinsă (37-40) (Figura 12). Într-un studiu pe un lot de copii născuţi în perioada 2002-2009 în România, 9% dintre copii au avut evoluţie nefavorabilă postlaserterapie, întrucât la acea dată nu se practica injecţia intraoculară cu anti-VEGF pentru formele agresive (25).
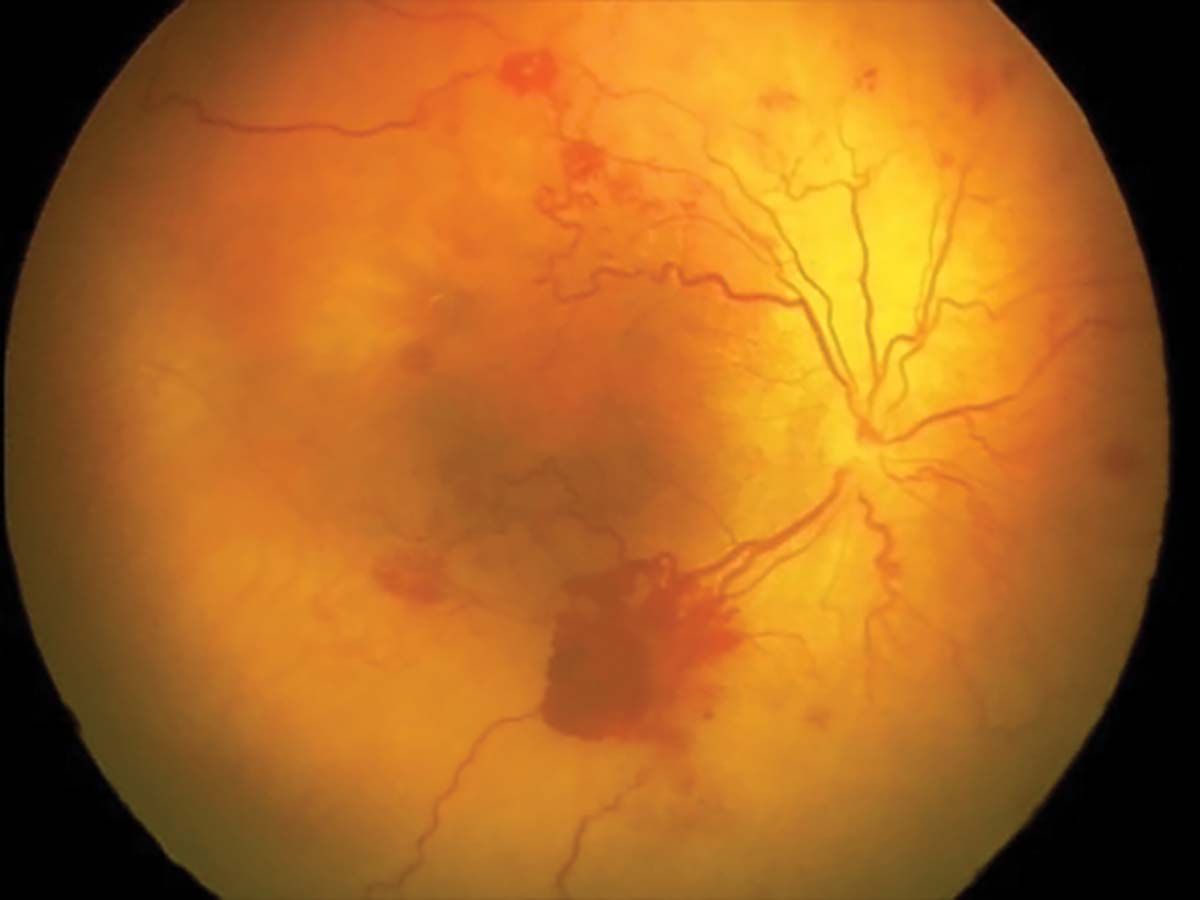
la 9 luni de viaţă (b)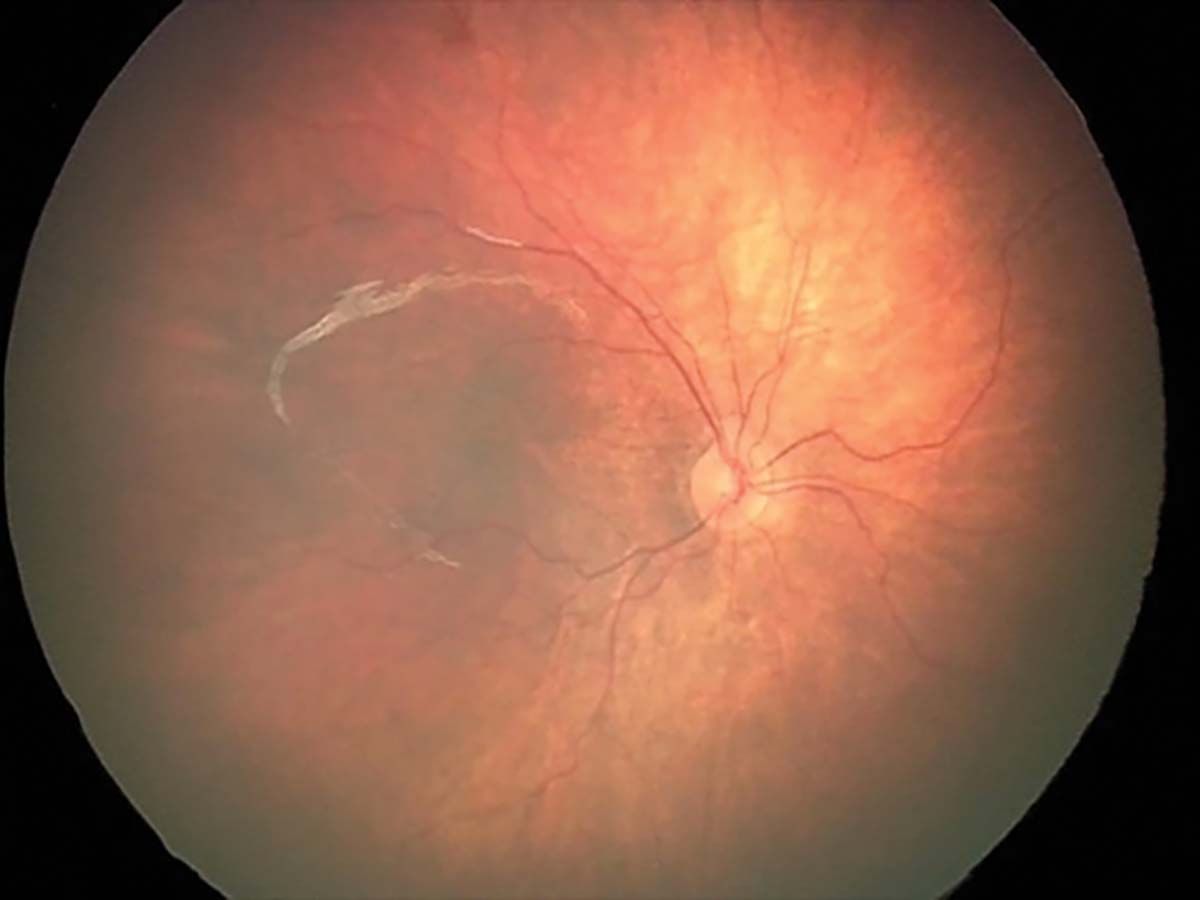
Acești copii trebuie examinaţi periodic, întrucât există cazuri când ROP se reactivează și necesită un tratament adiţional, fie o nouă injecţie, fie laserterapie (Figura 13).
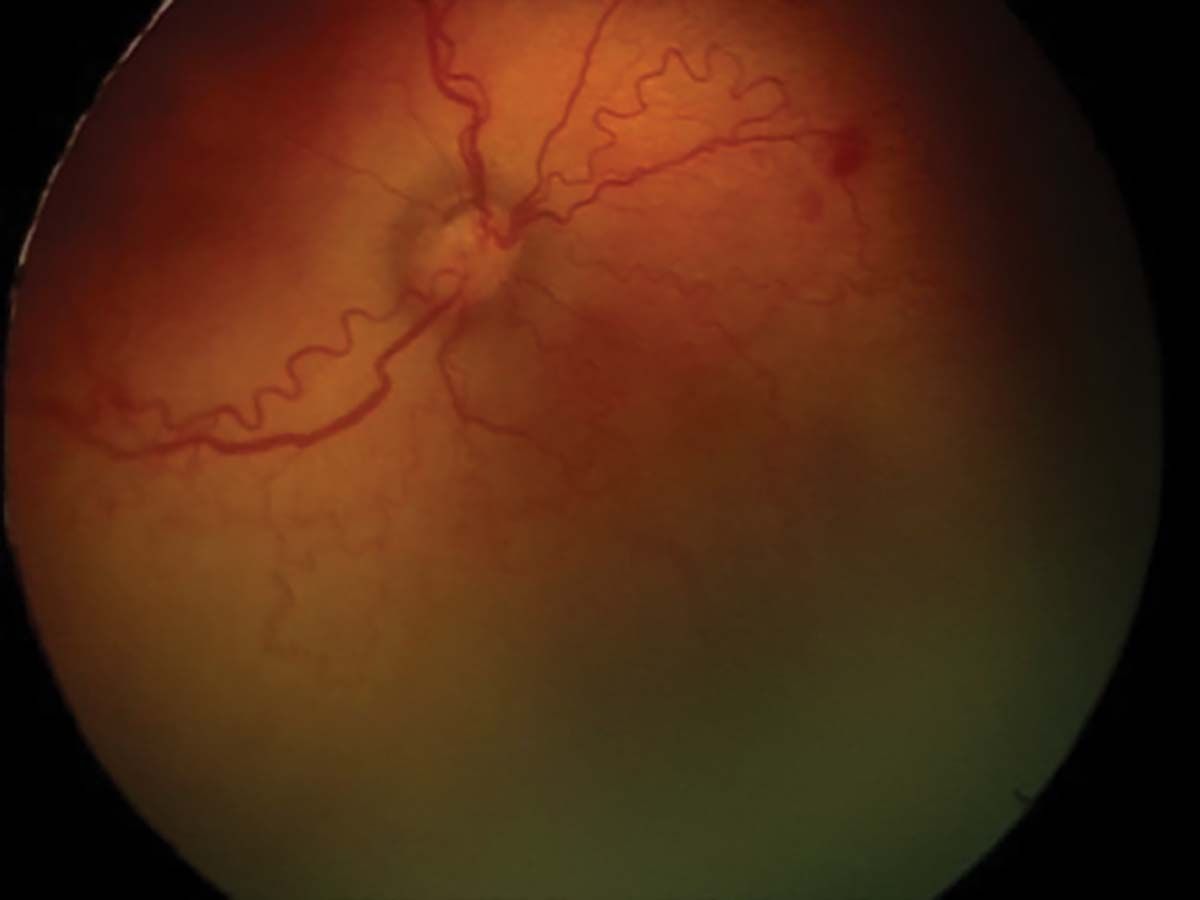
(b), la 16 săptămâni postinjecţie – ROP stadiul 3 (c) și aspectul postlaser
(d), întrucât nu au fost respectate datele de control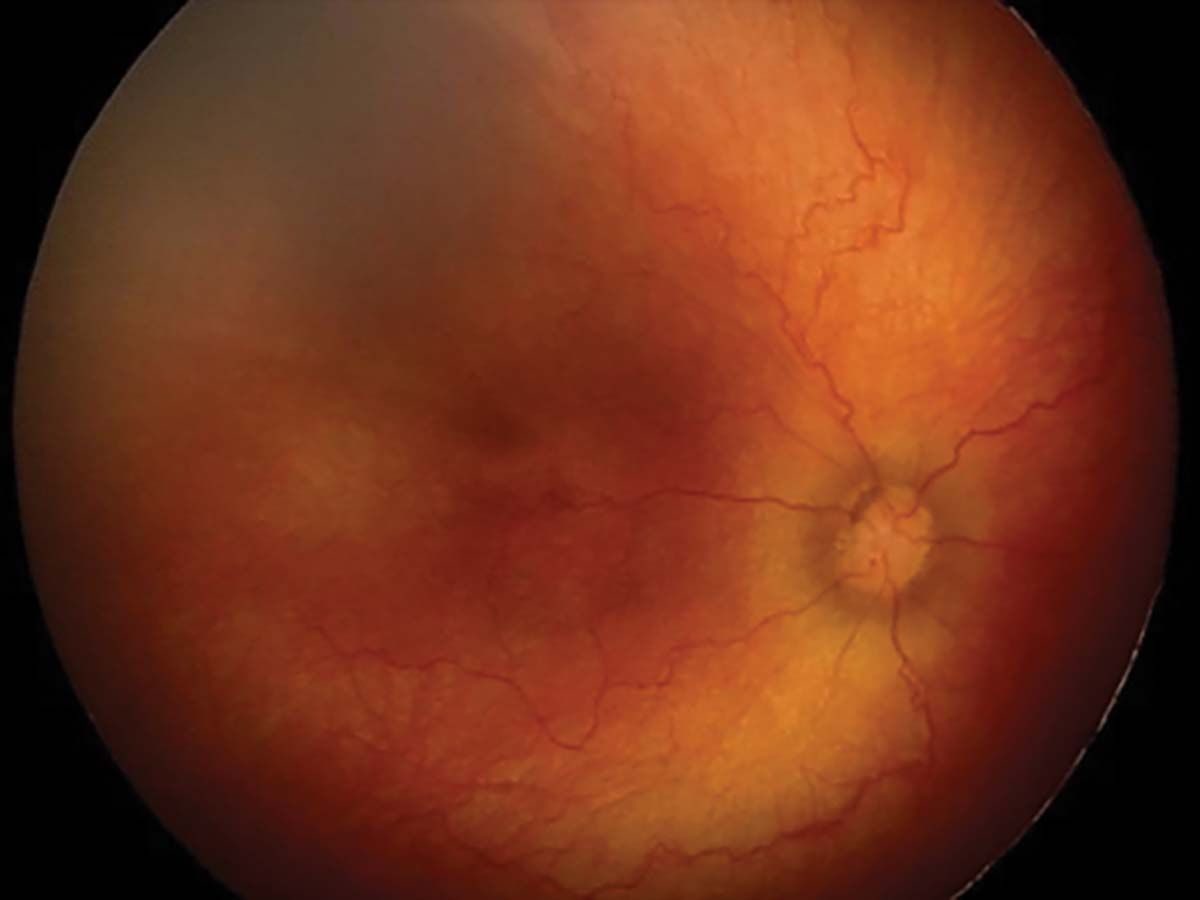
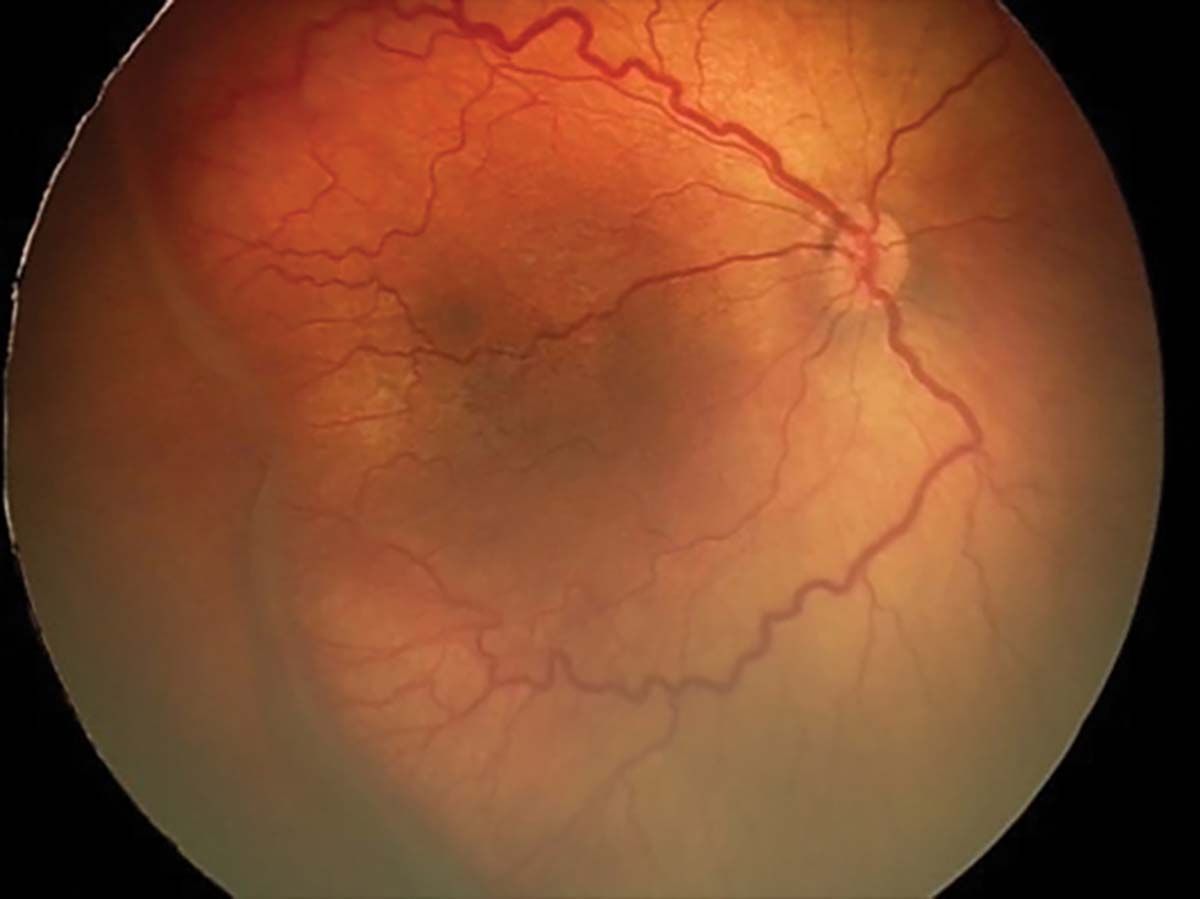
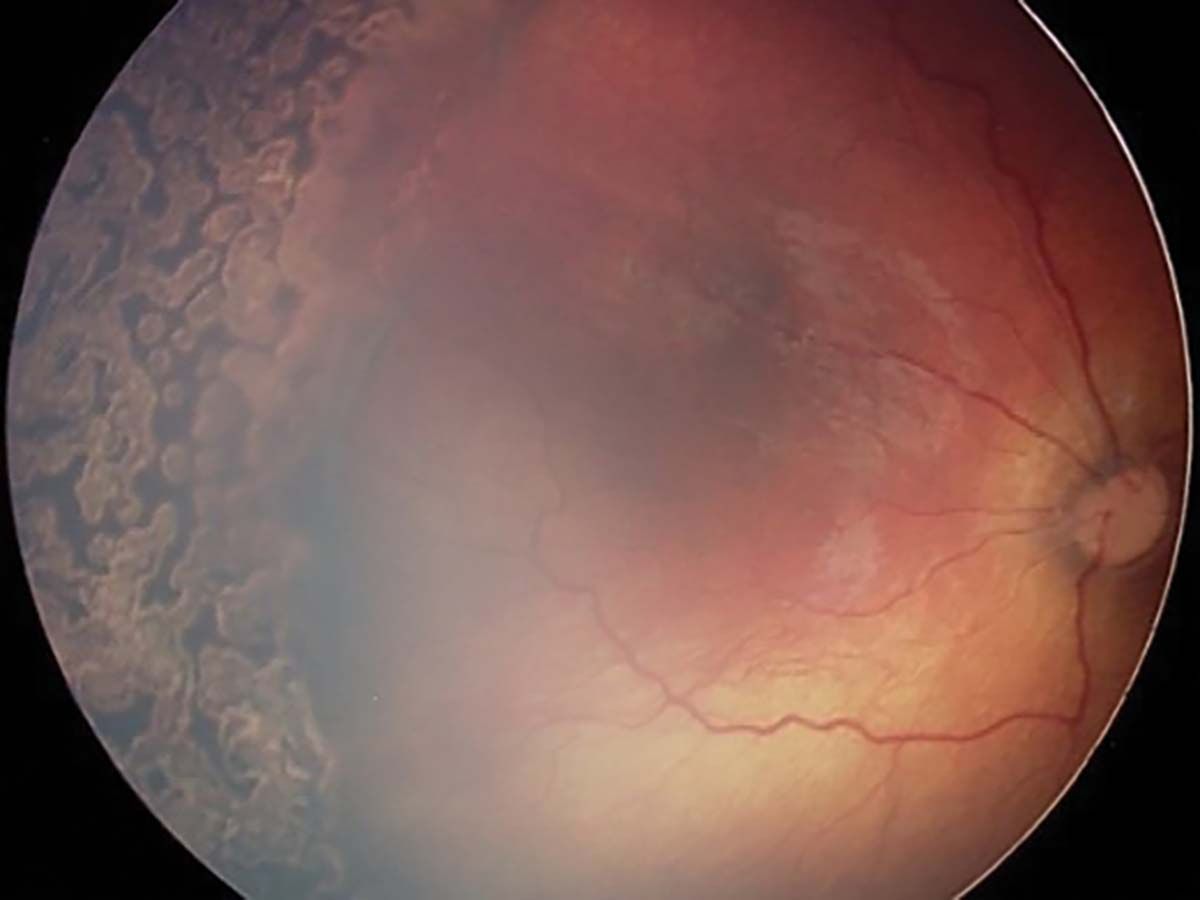
Se recomandă ca examinarea să se facă până la vascularizarea completă a retinei (se poate extinde până la 80 de săptămâni vârsta postmenstruală) sau se poate face laserterapie când vasele retiniene au trecut de zona II și macula este complet vascularizată (8,40-42).
Un aspect foarte important în tratamentul cu anti-VEGF este momentul aplicării acestuia. În ROP stadiul 4 sau în formele agresive, unde a apărut fibroza retiniană, acest tratament nu este indicat în monoterapie, ci asociat cu vitrectomia, pentru că altfel se poate produce o fibroză retiniană progresivă cu dezlipirea totală a retinei (43) (Figura 14).
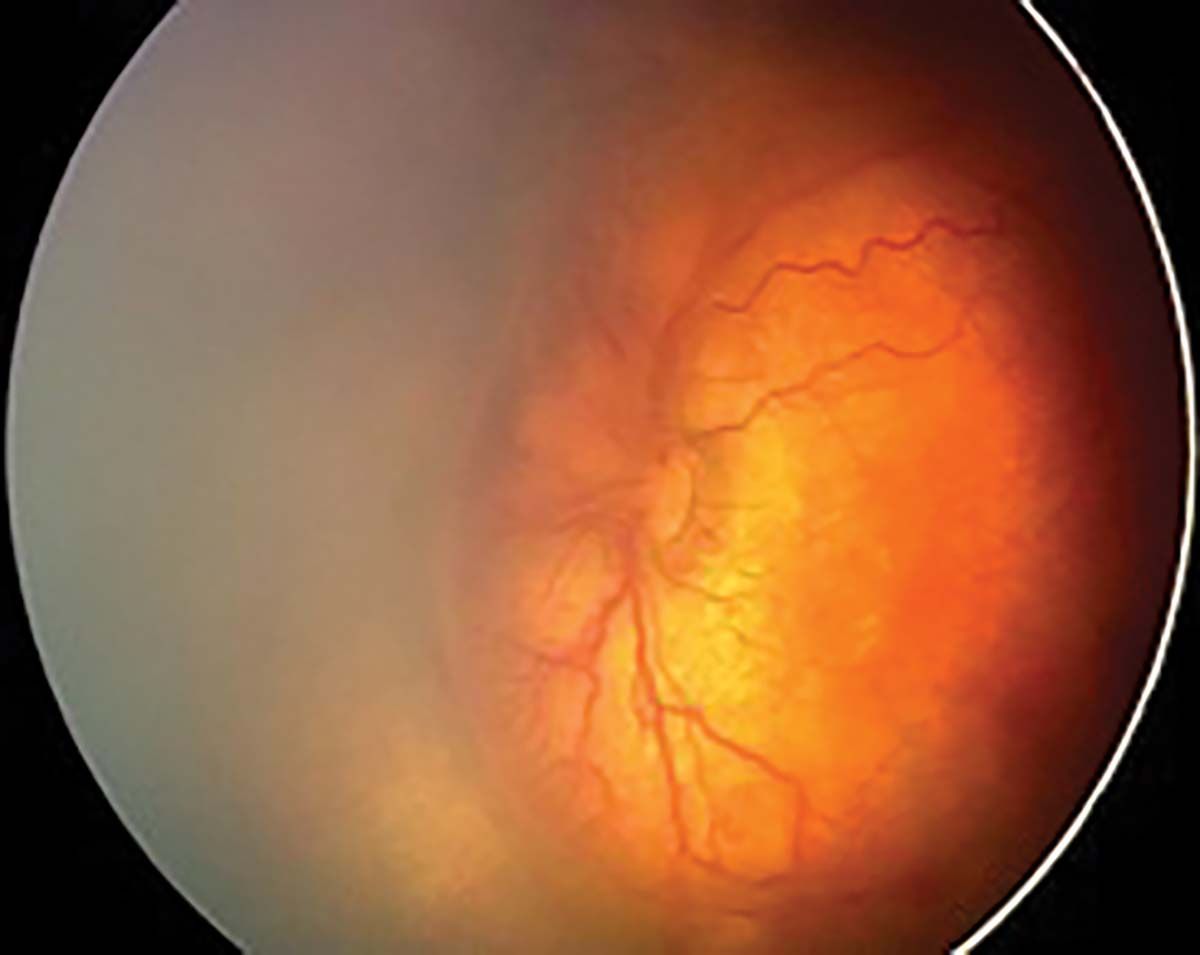
anti-VEGF (b)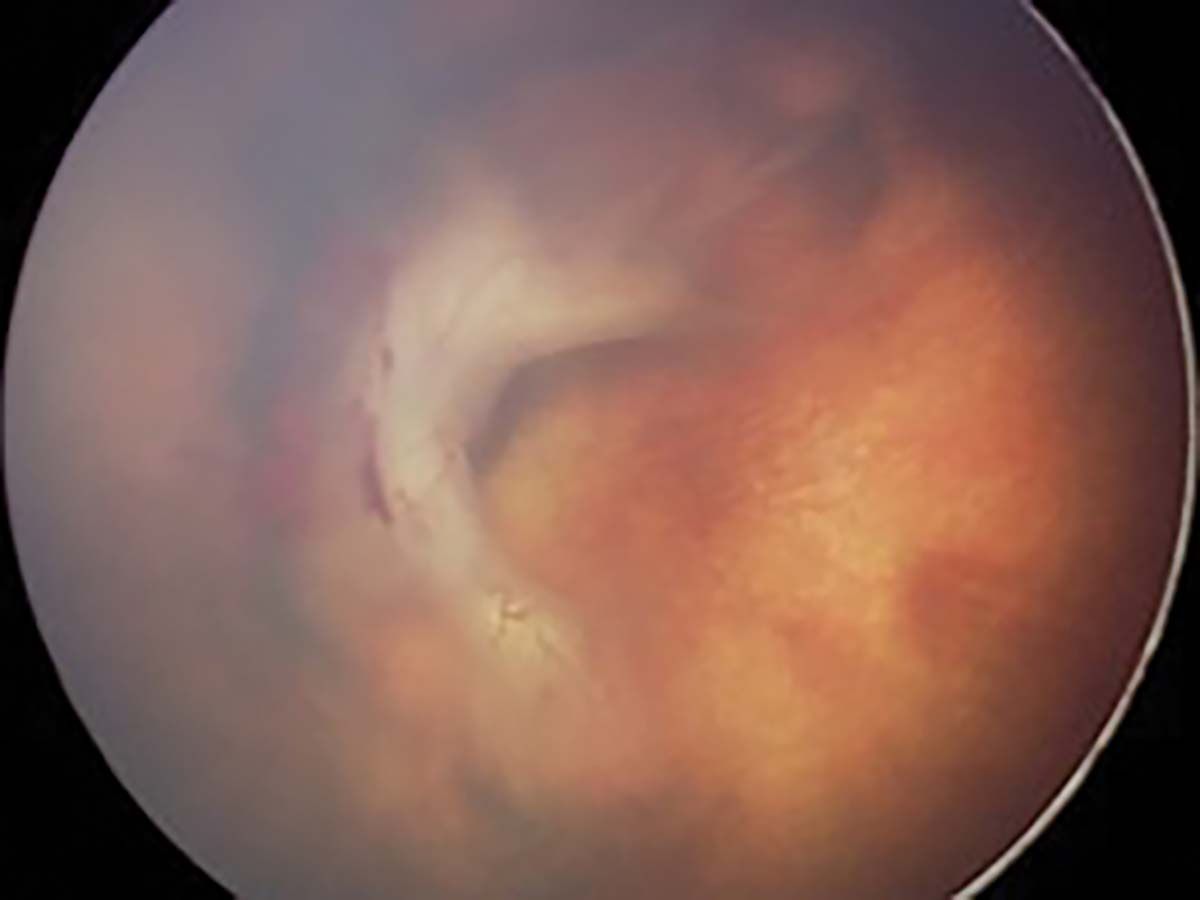
Chiar dacă anti-VEGF se administrează off-label și nu este încă un tratament bine standardizat, de cele mai multe ori este unica soluţie pentru acești copii. Se discută despre posibilele efecte adverse pe termen lung, dar nu au fost puse în evidenţă de niciun studiu clinic până în prezent (38). Din păcate, în acest moment, în România, acest tratament nu este acceptat de Ministerul Sănătăţii, fiind o medicaţie off-label, dar sute de copii au fost salvaţi de la orbire cu ajutorul lui la nivel mondial. Fiind unul dintre medicii care folosesc acest tratament, niciodată nu voi refuza să îl aplic doar pentru că nu este aprobat, întrucât doar noi, medicii care ne ocupăm de acești copii, cunoaștem dezastrul care urmează în cazul în care apare dezlipirea de retină și trebuie să privim părinţii în ochi, spunându-le că nu se mai poate face nimic niciodată și că vor avea un copil orb.
Chirurgia vitreoretiniană se practică în ROP stadiile 4 și 5, cu rezultate funcţionale bune în stadiul 4A (44) (Figura 15). În România, în acest moment, nu se practică la copiii prematuri acest tip de intervenţie. Din experienţa personală, precizez că în aproape 100% dintre cazurile de ROP stadiile 4 sau 5 pe care le-am întâlnit, cauza a fost lipsa screeningului și, implicit, a folosirii tratamentului în timp util (45).
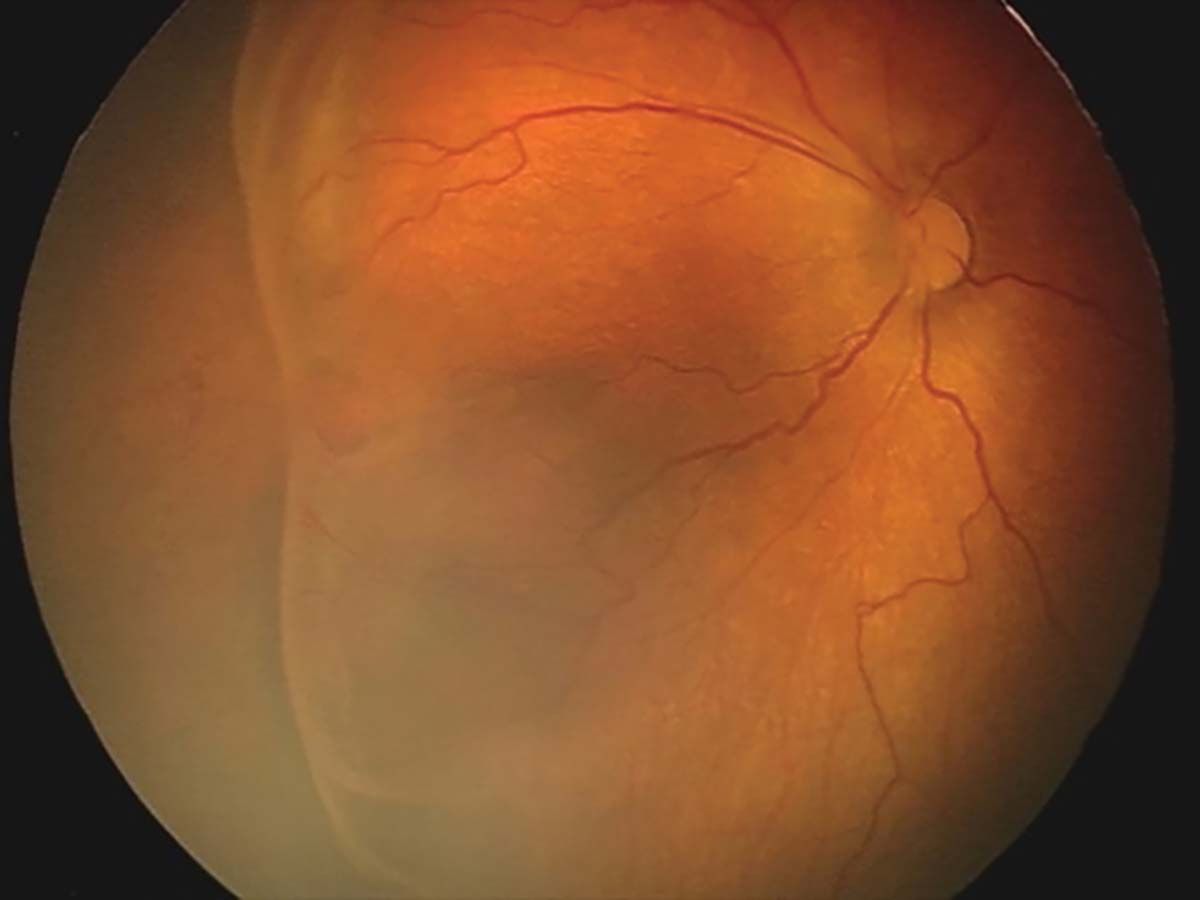
vitrectomie efectuată în Germania (b)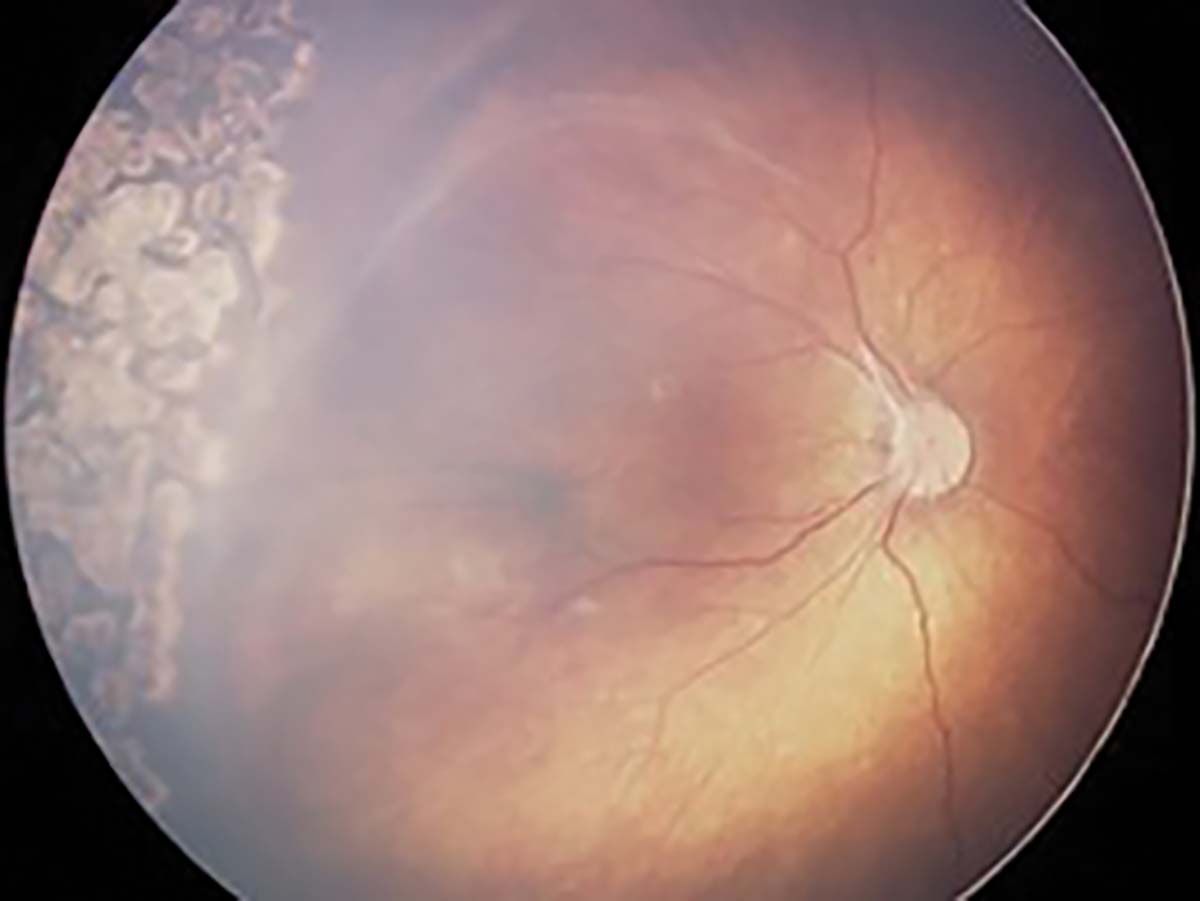
Copilul prematur trebuie urmărit timp îndelungat pentru diagnosticarea unor afecţiuni oftalmologice care pot fi tratate/corectate: ambliopie, strabism, miopie, anizometropie, dezlipire de retină tardivă (10,11,18,46,47).
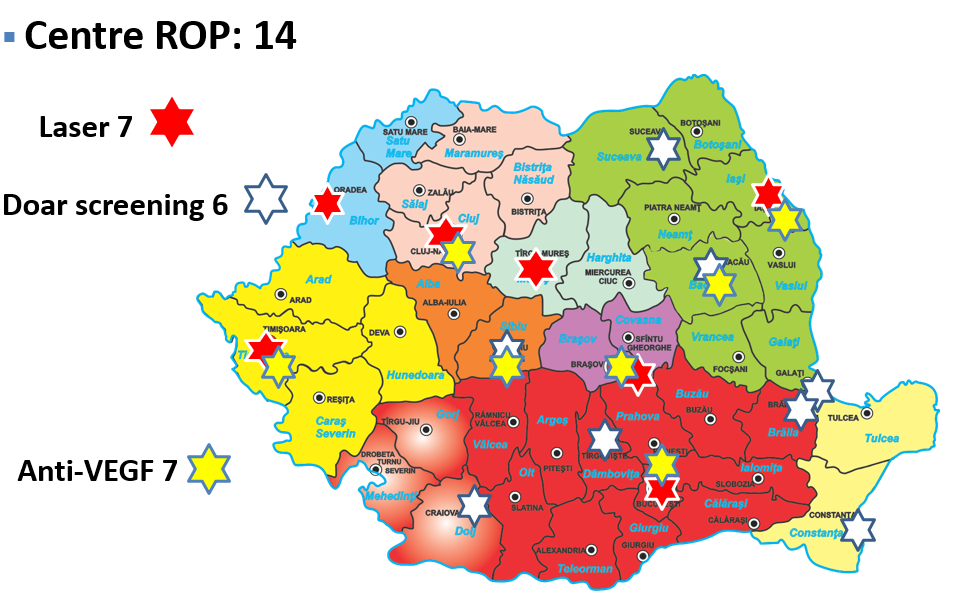
Programul Naţional de Screening și Tratament al Retinopatiei de Prematuritate în România a fost înfiinţat în anul 2002 la Institutul pentru Sănătatea Mamei și Copilului „Alessandrescu-Rusescu” București de Ministerul Sănătăţii, iar din anul 2004 acest program s-a implementat și în alte centre din ţară. Centrele ROP au luat fiinţă în maternităţile de nivel 3, la care sunt arondate și maternităţile de nivel 1 și 2, conform legislaţiei privind regionalizarea asistenţei materno-infantile (48). În prezent, în România sunt 14 centre ROP și 6 doar pentru screening. Laserterapie se face în 7 centre, iar în alte 7 centre se face tratament anti-VEGF. În jur de 22 de medici oftalmologi realizează screeningul ROP, 11 dintre aceștia fiind iniţiaţi în laserterapie (Figura 16).
Scopul acestui program este reducerea riscului de orbire și de sechele ROP, prin două aspecte principale: prevenţia primară, realizată printr-o cât mai bună îngrijire ante-, peri- și postnatală, și prevenţia secundară, realizată prin diagnosticul ROP, tratament și follow-up.
Se referă la reducerea ratei nașterilor premature, îmbunătăţirea îngrijirilor antenatale (controlul infecţiilor materne, administrarea de cortizon antenatal), intra- și postnatale, prin respectarea regionalizării maternităţilor și a protocoalelor de îngrijire neonatală (6). Studiile arată că incidenţa ROP crește cu scăderea VG și GN (7), de o importanţă radicală fiind prima oră de viaţă a nou-născutului prematur, numită și „ora de aur”, respectiv conduita în sala de naștere. Din acest motiv se recomandă respectarea regionalizării maternităţilor (nivel 1, 2 și 3), respectiv nașterea sau transferul imediat postnatal al nou-născutului prematur într-o unitate medicală adecvată, cu VG și GN ale acestuia, care poate asigura o îngrijire optimă. De exemplu, un copil cu VG<32 s sau/și GN<1.500 grame trebuie îngrijit într-o maternitate de nivel 3.
Incidenţa ROP este diferită de la o regiune la alta, precum și între unităţi din același oraș, în funcţie de respectarea protocoalelor de reanimare la naștere (22). Este demonstrată legătura directă între reanimarea nou-născutului cu O2 100% în sala de naștere și incidenţa crescută a formelor agresive posterioare la copiii cu VG mari (34). Din acest motiv este obligatoriu ca fiecare sală de naștere și unitate de terapie intensivă neonatală să fie echipată cu blendere, prin care O2 se mixează cu aer și se administrează nou-născutului, pentru a se obţine saturaţia dorită a O2 (27). Prevenţia infecţiilor neonatale (29), a hipotermiei, tratarea corectă a anemiei, nutriţia enterală cu lapte de mamă și nutriţia parenterală adecvată (32) sunt factori ce reduc apariţia ROP severe.
Se realizează prin screeningul și tratamentul ROP, având ca scop diagnosticarea formelor severe care necesită tratament imediat, întrucât tratamentul realizat la timp are ca efect vindecarea bolii în aproape 100% din cazuri (6).
Screenigul ROP trebuie iniţiat în maternitate înainte de externare la toţi copiii din grupa de risc, lucru care îmbunătăţește atât diagnosticul la timp, cât și aderarea la procesul de screening. Educaţia sanitară în România este deficitară, precum și comunicarea cu medicii de familie, așa că nu este suficientă o simplă recomandare de „control oftalmologic la o lună de viaţă”, fără a explica părinţilor motivul acestui control (5,6). Nu este deontologic ca prezentarea la control oftalmologic să fie doar responsabilitatea părinţilor dacă nu știu și consecinţele neprezentării. Este simplu să înţelegem acest lucru dacă reflectăm câţi dintre noi, medicii, respectăm datele de control atunci când suntem pacienţi.
ROP este una dintre afecţiunile a căror prevenţie prin screening și tratament este benefică nu numai prin raport cost/eficienţă, dar mai ales prin creșterea calităţii vieţii (54). Fiind unul dintre medicii implicaţi în acest program, pot afirma că impactul moral și social este unul major.
Din experienţa personală pot spune că tratamentul ROP efectuat corect și la timp are ca efect vindecarea bolii în aproape 100% dintre cazuri. De aceea, consider că ROP reprezintă o urgenţă în oftalmologie, pentru că uneori 24 de ore pot face diferenţa dintre lumină și întuneric. Nu există lucru mai greu în activitatea mea de medic decât să examinez copii nevăzători prin sechele ROP și să nu pot face nimic pentru ei.
Cred și sper ca toată munca și dăruirea noastră, a medicilor oftalmologi, precum și a zecilor de medici neonatologi și asistente care îngrijesc copii prematuri să ajute la luarea unor decizii simple, dar hotărâtoare pentru ei, o parte din viitorul acestei ţări. Consider că România are în prezent toate resursele necesare să corecteze ceea ce este de corectat în practica medicală curentă. Suntem un popor ambiţios, cu oameni inimoși, care știu ce au de făcut, doar să fie sprijiniţi și ascultaţi.
Bibliografie
1. International Committee for the Classification of Retinopathy of prematurity. The International Classification of Retinopathy of Prematurity revised. Arch Ophthalmol 2005; 123(7):991-999.
2. Retinal vascular disease A.M. Joussen, T.W. Gardner, B. Kirchhof, S.J. Ryan, Editors, Springer 2007:392-423.
3. Coats DK, Reddy AK: Retinopathy of prematurity. Wilson E et al. (eds.), Pediatric Ophthalmology,DOI 10.1007/978-3-540-68632-3_1, © Springer-Verlag Berlin Heidelberg 2009(375-386).
4. Holmstrom G, M el Azazi, Jacobson L, Lennerstrand G: A population based, prospective study of the development of ROP in prematurely born children in the Stockholm area of Sweden. BritishJournal of Ophthalmology 1993; 77:417-423.
5. UK Retinopathy of Prematurity Guideline, May 2008, Royal College of Paediatrics and Child Health, Royal College of Ophthalmologists, British Association of Perinatal Medicine.
6. Darlow BA, Gilbert CE, Quiroga AM: Setting up and improving Retinopathy of Prematurity Programs. Interaction of Neonatology, Nursing and Ophthalmology. Clin Perinatol 40 (2013) 215–227.
7. Coats DK, Garcia-Prats JA, Saunders RA, Armsby C: Retinopathy of prematurity: Pathogenesis, epidemiology, classification and screening.www.uptodate.com 2018UpToDate, Inc.and/or its affiliates.
8. AAP (American Academy of Pediatrics), AAPOS (American Association for Pediatric Ophthalmology and Strabismus), AAO (American Academy of Ophthalmology), Screening examination of premature infants for retinopathy of prematurity – 2013, Pediatrics 2013;131:189-195.
9. Coats DK, Garcia-Prats JA, Saunders RA, Armsby C: Retinopathy of prematurity: Treatment and prognosis. www.uptodate.com 2018UpToDate, Inc.and/or its affiliates.
10. Fielder A, Blencowe H, O’Connor A, Gilbert C: Impact of retinopathy of prematurity on ocular structures and visual functions. Arch Dis Child Fetal Neonatal 2015;100:F179-F184.
11. Quinn GE, Dobson V, Davitt BV, Wallace DK, Hardy RJ, Tung B, Lai D, Good WV: Progression of myopia and high myopia in the Early Treatment for Retinopathy of Prematurity Study: Findings at 4 to 6 years of age, on behalf of the Early Treatment for Retinopathy of Prematurity Cooperative Group. JAAPOS 2013;17(2):124–128.
12. Chan-Ling T, Gole GA, Quinn GE, Adamson SJ, Darlow BA: Pathophysiology, screening and treatment of ROP: A multi-disciplinary perspective. Progress in Retinal and Eye Research (2017), doi: 10.1016/j.preteyeres.2017.09.002.
13. https://media.vtoxford.org/multimedia/Cochrane/12182017/CochraneNeonatalWebinar_12-18-2017.mp4.
14. Silverman WA: Retrolental fibroplasia: a modern parable. New York: Grune and Straton, Inc; 1980. p. 2017.
15. Cryotherapy for Retinopathy of Prematurity Cooperative Group: Multicenter Trial of Cryotherapy for Retinopathy of Prematurity. Ophthalmological Outcomes at 10 Years. Arch Ophthalmol 2001;119(8):1110-1118.
16. Good Wv, Hardy Rj, Dobson V et al: The incidence and course of retinopathy of prematurity: findings from the early treatment for retinopathy of prematurity study. Pediatrics 2005; 116(1): 15-23.
17. Quinn GE: Retinopathy of prematurity blindness worldwide: phenotypes in the third epidemics. Eye and Brain 2016;8:31-36.
18. Wilson CM, Ells AL, Fielder AR: The challenge of screening for retinopathy of prematurity. Clin Perinatol 40 (2013) 241–259.
19. Gilbert C, Fielder A, Gordillo L, et al: Characteristics of infants with severe retinopathy of prematurity in countries with low, moderate, and high levels of development: implications for screening programs. Pediatrics 2005; 115:e518.
20. Smith LE, Hard AL, Hellstrom A: The Biology of Retinopathy of Prematurity. How Knowledge of Pathogenesis Guides Treatment. Clin Perinatol 40(2013)201-214.
21. Kocur I, Resnikoff S: Visual impairment and blindness in Europe and their prevention. Br J Ophthalmol 2002; 86: 716-722.
22. Zin A, Gole GA: Retinopathy of Prematurity – Incidence Today. Clin Perinatol 40 (2013) 185-200.
23. Jalali S, Matalia J, Hussain A, Anand R: Modification of screening criteria for retinopathy of prematurity in India and other middle – income countries. Am J Ophthalmol 2006; 141(5): 966-968.
24. Gilbert C et al: Retinopathy of prematurity in Middle Income Countries. Lancet 1997; 350: 12.
25. Nascutzy C: Screening and treatment of retinopathy of prematurity in Romania Congresso Internazionale del Gruppo di Studio per la R.O.P., Milano, 2011.
26. Nițulescu C, Nascutzy C: Standardul îngrijirii neonatale și incidența formei severe de retinopatie de prematuritate. Al VI-lea Congres al Societății Române de Oftalmopediatrie și Strabism, Sinaia, 2014.
27. SUPPORT Study Group of the Eunice Kennedy Shriver NICHD Neonatal Research Network, Carlo WA, Finer NN et al. Target ranges of oxygen saturation in extremely preterm infants. N Engl J Med 2010;362:1959.
28. Flynn JT, Bancalari E, Snyder ES et all: A cohort study of transcutaneous oxygen tension and the incidence and severity of retinopathy of prematurity. N Engl J Med 1992;326:1050.
29. Seiberth V, Linderkamp O: Risk factors in retinopathy of prematurity. A multivariate statistical analysis. Ophthalmologica 2000;214:131.
30. Hagadorn JI, Richardson DK, Schmid CH, Cole CH: Cumulative illness severity and progression from moderate to severe retinopathy of prematurity. J Perinatol 2007;27:512.
31. Bharwani SK, Dhanireddy R: Systemic fungal infection is associated with the development of retinopathy of prematuriy in very low birth infants: a meta-review. J Perinatol 2008;28:61.
32. Hellstrom A, Hard AL, Engstrom E, et al: Early weight gain predicts retinopathy in preterm infants: new, simple, efficient approach to screening. Pediatrics 2009;123:e638.
33. Mohsen L, Abou-Alam M, El-Dib M, et al: A prospective study on hyperglycemia and retinopathy of prematurity. J Perinatol 2014;34:453.
34. Shah PK, Narendran V, Kalpana N: Aggressive posterior retinopathy of prematurity in large preterm babies in South India. Arch Dis Child Fetal Neonatal Ed 2012;97:F371.
35. Reynolds JD, Dobson V, Quinn GE, Fielder AR, Palmer EA, Saunders RA et all: Evidence-based screening criteria for retinopathy of prematurity. Natural history data from the CRYO-ROP and LIGHT-ROP studies. Arch Ophthalmol 2002;120:1470-1476.
36. Early Treatment for Retinopathy of Prematurity Cooperative Group: Revised indications for the Treatment of Retinopathy of Prematurity.Results of the Early Treatment for Retinopathy of Prematurity Randomized Trial.Arch Ophthalmol. 2003;121:1684-1696.
37. Alba LE, Zaldua RA, Masini RA: Off-label use of intravitreal bevacizumab for severe retinopathy of prematurity. Arch Soc Esp Oftalmol. 2015;90(2):81-86.
38. Pertl L, Steinwender G, Mayer C, Hausberger S, Pöschl EM, Wackernagel W, Wedrich A, El-Shabrawi Y,Haas A: A Systematic Review and Meta-Analysis onthe Safety of Vascular Endothelial Growth.Factor (VEGF) Inhibitors for the Treatment of.Retinopathy of Prematurity.PLoS ONE 10(6): e0129383.doi:10.1371/journal.pone.0129383.
39. VanderVeen DK, Wilson LB, Melia M, Lambert SR: Anti-Vascular Endothelial Growth Factor Therapy for Primary Treatment of Type 1Retinopath-633.
40. Mintz-Hittner HA, M.D., Kennedy KA, Ch y of Prematurity. A Report by the American Academy of Ophthalmology. Ophthalmology 2017;124:619uangAZ for the BEAT-ROP Cooperative Group: Efficacy of Intravitreal Bevacizumab for Stage 3+ Retinopathy of Prematurity. The New England Journal of Medicine 2011;364(7):613-615.
41. Mintz-Hittner HA, Geloneck MM, Chuang AZ: Clinical management of recurrent retinopathy of prematurity following intravitreal bevacizumab monotherapy. Ophthalmology. 2016 September;123(9):1845–185564.
42. Lepore D, Baldascino A, Ricci D, Quinn GE, Ji MH, Mercuri E, Molle F, Sammartino, Orazi L, Sbaraglia F: Follow-up to Age 4 Years of Treatment of Type 1 Retinopathy of Prematurity Intravitreal Bevacizumab Injection versus Laser: Fluorescein Angiographic Findings. Ophthalmology 2017; 1-9.
43. Yonekawa Y, Wu WC, Nitulescu CE, Chan RVP, Thanos A, Thomas BJ, Todorich B, Drenser KA, Trese MT, Capone AJr: Progressive retinal detachment in infants with retinopathy of retinopathy treated with intravitreal bevacizumab or ranibizumab. Retina 2018;38(6):1079-1083.
44. Capone A Jr, Trese MT: Lens-sparing vitreous surgery for tractional stage 4A retinopathy of prematurity retinal detachments. Ophthalmology 2001;108:20168-2070.
45. Nițulescu C, Nascutzy C, Stamatian I, Lorenz B, Capone A Jr, Trese MT: Tratamentul retinopatiei de prematuritate. Cazuri clinice. Congresul Societății Române de Oftalmologie, Sinaia 2016.
46. Holmström G, Larsson E: Outcome of retinopathy of prematurity. Clin Perinatol 40 (2013) 311–321.
47. Mintz-Hittner, Geloneck MM: Review of effects of anti-VEGF treatment on refractive error. Eye and Brain 2016;8;135-140.
48. Hotărâre nr. 534 din 30 mai 2002 pentru aprobarea Strategiei privind reabilitarea şi reorganizarea sistemului de asistenţă medicală spitalicească de specialitate în obstetrică-ginecologie şi neonatologie din România, pe perioada 2002-2004. Monitorul Oficial nr. 396 din 10 iunie 2002.
49. Holmstrom GE, Hellstrom A, Jakobsson PG, Lundgren P, Tornqvist K, MD, Wallin A: Swedish National Register for Retinopathy of Prematurity (SWEDROP) and the Evaluation of Screening in Sweden. Arch Ophthalmol. 2012;130(11):1418-1424.
50. Nițulescu. C, Nascutzy C, Vătavu I: Screeningul și tratamentul retinopatiei de prematuritate în România. Al XXXIII-lea Congres al Societății Române de Oftalmologie, Sinaia, 2014.
51. Nițulescu. C, Stamatian I, Nascutzy C: Tratamentul retinopatiei de prematuritate. Cazuri clinice. A VIII-a ediție a Congresului Societății Române de oftalmopediatrie și strabism, Brașov, 2018.
52. Chiang MF, Melia M, Buffenn AN, Lambert SR et all: Detection of clinically significant retinopathy of prematurity using wide-angle digital retinal photography. Ophthalmology 2012;119;1272-1280.
53. Quinn GE et all: Validity of a telemedicine system for the evaluation of acute-phase retinopathy of prematurity. JAMA Ophthalmol 2014;132(10):1178-1184.
54. Rothschild MI, Russ R, Brennan K et all: The economic model of Retinopathy of Prematurity (EcROP)
screening and treatment: Mexico and United States. Investigative Ophthalmology&Visual Science 2015(56)967.
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe