
Progresele în genomică permit personalizarea abordării pacienţilor la risc de a dezvolta cancer de sân, precum și tratamentul acestor forme de cancer.
Anual, în lume, cancerul de sân afectează peste un milion de persoane și este una dintre cauzele principale de mortalitate prin cancer. Dintre cele 25.000 de gene umane, aproximativ 600 pot provoca o formă de cancer. În studiile recente s-au evidenţiat 110 gene asociate cu un risc înalt de apariţie a cancerului de sân, dintre care 32 corelate cu rata de supravieţuire, care au fost analizate prin tehnici moderne.
Interpretarea datelor de prognostic a fost iniţial complicată de faptul că studiile din anii precedenţi au folosit doar tehnica de imunohistochimie pentru a detecta acumularea de proteine modificate structural, izoforme de tip p-53, în citoplasma celulelor maligne, spre deosebire de studiile recente, bazate pe metode moleculare precum ELISA, fluorescenţa cu hibridizare in situ (FISH), metoda de secvenţiere genetică (Sequential Gene Method, SGN), reverse transcription-polymerase chain reaction (RT-PCR) și tehnologia CRISPR-Cas-9(1).
De-a lungul ultimului deceniu, mai multe gene au fost identificate ca fiind legate genetic de moștenirea cancerului de sân. Genele BRCA1 și BRCA2 sunt considerate cele mai importante, fiind legate de predispoziţia moștenită a cancerului de sân, alături de genele PTEN și P-53. Susceptibilitatea cancerului de sân la pacienţii cu mutaţia BRCA1 este de până la 87% pentru femeile în vârstă și este asociată cu genele CHECK2, PALB și ATM.
În mod similar, metilarea genelor la locusul CDKN2A (INK4a/ARF) poate reduce epigenetic expresia proteinei p14-ARF și poate să blocheze capacitatea genelor activate de a stabiliza răspunsul genei P-53 la o agresiune a ADN-ului. Identificarea genelor modificate care cresc riscul de cancer de sân nu este suficientă, deoarece anumite secvenţe din ADN-ul „la risc” pot interacţiona cu alte părţi din genom în cadrul unui fenomen numit „looping ADN” (2).
Conform consilierii genetice și studiilor epidemiologice, riscul de a dezvolta un anumit tip de cancer la pacienţii cu polimorfismele genei P-53 este de 90%. Gena P-53 reglează genele necesare pentru întreţinerea telomerilor, repararea ADN-ului și structura centromerului, prevenind dezvoltarea cancerului.
Studiile anterioare au arătat că Δ40p-53 este izoforma p-53 cel mai puternic exprimată în cancerul de sân, în afară de p-53a în sine, cu o expresie semnificativ mai mare în probele tumorale în comparaţie cu ţesutul adiacent. În plus, un raport ridicat Δ40-53/p-53a este asociat cu o probabilitate crescută de metastazare, sugerând că această izoformă joacă un rol în carcinogeneza cancerului de sân și că poate modifica rezultatele terapeutice (3).
Numeroase studii au demonstrat că expresiile aberante ale micro-ARN-urilor sunt implicate în iniţierea și dezvoltarea cancerului. Micro-ARN-urile (mi-ARN) sunt acizi ribonucleici care nu codifică proteine, sunt conservate evolutiv și conţin 19-25 de nucleotide care apar prin scindarea a 70-100 de precursori de nucleotide ale ADN-ului. Aceste tipuri de acizi ribonucleici au oferit o nouă dimensiune a reţelelor complexe de reglare a genelor.
Nu se cunoaște relaţia care poate exista între un mi-ARN și un ARN mesager (ARNm) în stresul celular citoplasmatic, dar este de așteptat o corelaţie negativă între nivelurile de expresie a acestor ARN-uri. S-a demonstrat că acidul ribonucleic mi-ARN-214 funcţionează ca un oncogen în diferite tipuri de cancer uman, inclusiv în cancerul de sân. Moleculele de mi-ARN joacă și roluri de reglare a diferitelor segmente de ADN, condensate transcripţional, în procesul de îmbătrânire și în momentele de stres.
De asemenea, s-a descoperit că gena mutantă P-53, prin proteina sa izomorfă p-53, este gena-ţintă a mi-ARN-214, acesta din urmă promovând progresia cancerului de sân. În aceste cazuri, anticorpii specifici anti-mi-ARN-214 sunt utilizaţi în analize paralele în studiile clinice (4,5).
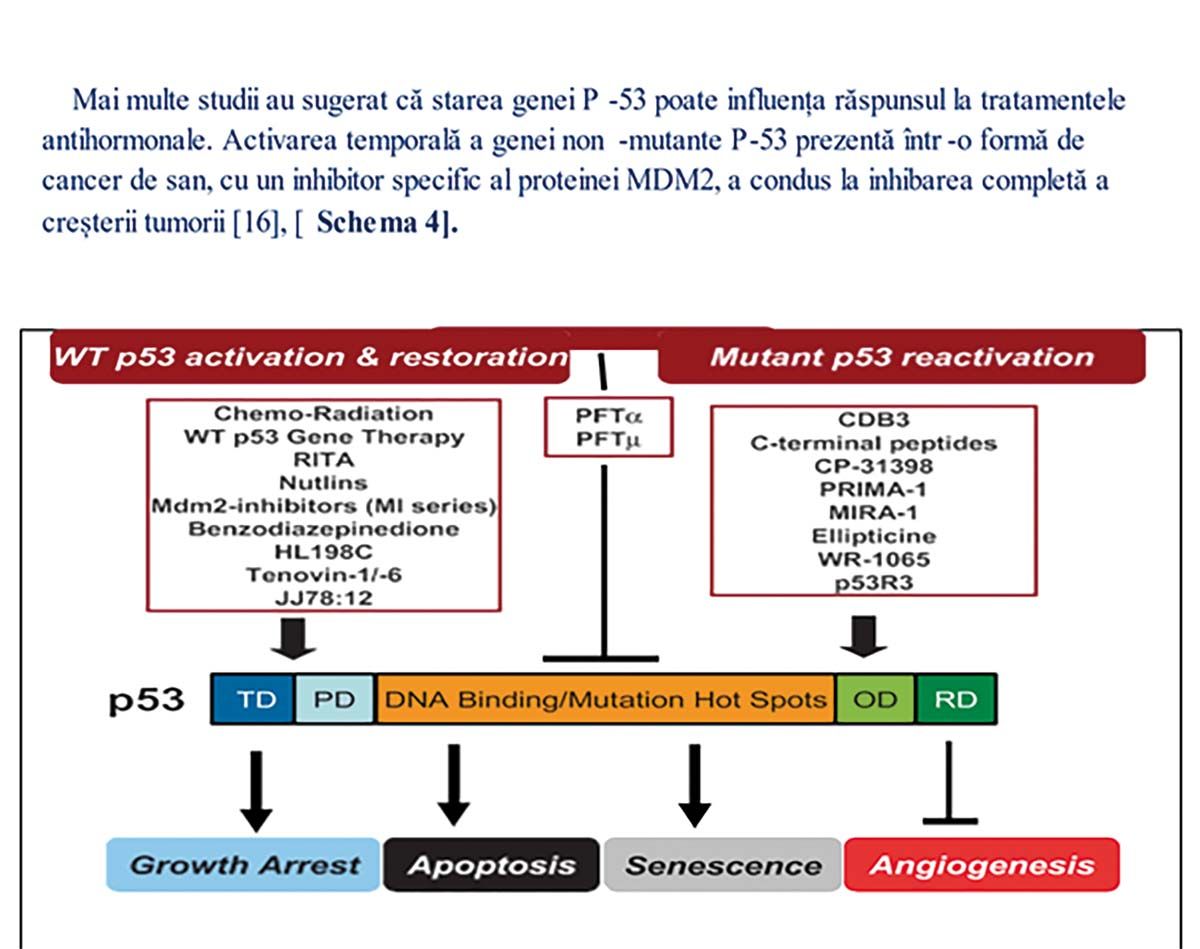
Studiile clinice la pacienţii cu cancer de sân local avansat trataţi cu tamoxifen sau chimioterapie primară au arătat că prezenţa mutaţiilor genei P-53 este asociată cu o supravieţuire mai scăzută. Odată cu descoperirea recentă a inhibitorilor specifici proteinei citoplasmatice MDM2 (Nutlin-3), care activează proteina p-53 nativă, cu structură normală, este acum posibil să se moduleze răspunsul interacţiunii p-53-MDM2 în diferite setări tumorale. Nutlins sunt un grup de compuși chimici, analogi de cis-imidazolină, care au o potenţă de legare și selectivitate ridicate pentru proteina citoplasmatică MDM2, care degradează proteina p-53 în stare nativă (Figura 1).
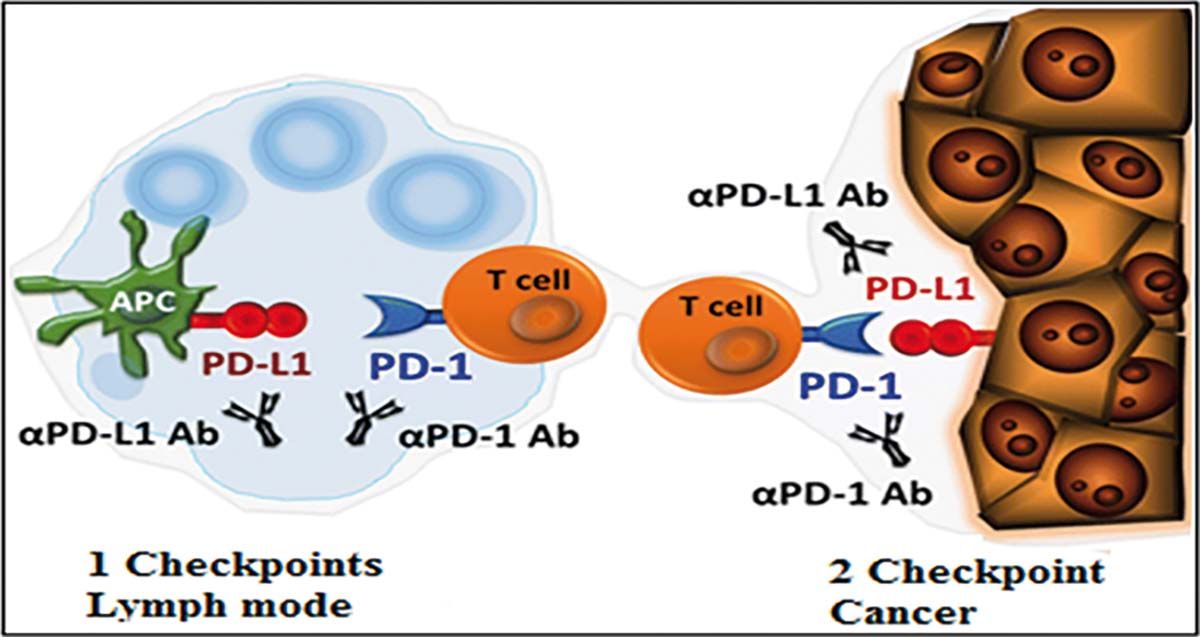
De asemenea, tratamentul cu inhibitori ai punctelor de control imunologic, cum ar fi PD-1/PD-L1, poate îmbunătăţi perspectivele pacienţilor cu diferite afecţiuni maligne. Interacţiunile dintre PD-1 și liganzii săi, PD-L1 și PD-L2, sunt complexe și apar în mai multe etape ale unui răspuns imun. Calea PD-1 este, de asemenea, probabil să fie importantă în micromediul tumoral în care PD-L1 exprimat de tumori interacţionează cu PD-1 pe celulele T pentru a suprima funcţia efectorie a limfocitelor T.
Astăzi sunt în curs de desfășurare studii clinice cu anti-CTLA-4 și puncte de control imunologic, care pot îmbunătăţi perspectivele pacienţilor cu diferite afecţiuni maligne. Interacţiunile dintre PD-1 și liganzii săi, PD-L1 și PD-L2, sunt complexe și apar în mai multe etape ale unui răspuns imun (Figura 2) (7).
Gestionarea eficientă a cancerului de sân se poate realiza prin crearea unei divizii de genomică (inclusiv de editare genomică de tipul CRISPR-Cas-9) şi de tip „multi-omics”, pentru identificarea precoce, diagnosticarea precisă şi tratarea mai eficientă în cancerul de sân – în colaborare cu Institutul Naţional de Genomică pentru terapiile celulare CAR-T (înalt personalizate) –, și cu decontarea testării panelului de gene implicate în detecţia cancerului de sân.
Tehnicile speciale de laborator utilizate pentru a identifica structura genetică a ADN-ului din cancere devin un predictor mai bun al agresivităţii și rezultatului tratamentului cancerului. Aceste studii pot însemna începutul unui nivel superior în tratamentul personalizat al cancerului de sân, cu noi teste genetice care pot prezice riscul de cancer, precum și noi tipuri de terapii ţintite.
Bibliografie
1. Senkus-Konefka E, Cardoso F, Douillard JY, Bramley C, Longo F, Jezdic S. ESMO Clinical Practice Guidelines: Breast Cancer Accessed in 5/12/2022
2. Grindedal EM, Heramb C, Karsrud I, Ariansen SL, Mæhle L, Undlien DE et. al. Current guidelines for BRCA testing of breast cancer patients are insufficient to detect all mutation carriers. BMC Cancer. 2017 Jun 21;17(1):438
2. Reinhardt LS, Zhang X, Groen K, Mortenl BC, Geoffry N, Iuliis D et al. Alterations in the p53 isoform ratio govern breast cancer cell fate in response to DNA damage. Cell Death and Disease 2022; 13:907;
4. Laxman N, Rubin CJ, Mallmin H, et al. Global miRNA expression and correlation with mRNA levels in primary human bone cells. RNA. 2015; 21(8):14-15
5. Torsin LI, Petrescu GED, Sabo AA, Chen B, Brehar FM, Dragomir MP, et al. Editing and Chemical Modifications on Non-Coding RNAs in Cancer: A New Tale with Clinical Significance. Int. J. Mol. Sci. 2021; 22: 581
6. Nag S, Zhang X, Srivenugopal KS, Wang MH, Wang W, Zhang R. Targeting MDM2-p53 interaction for cancer therapy: are we there yet? Curr Med Chem. 2014; 21(5): 553–74
7. Udriștioiu A., Cojocaru C. Role of P-53 Gene in Preventing Breast Cancer. Int J Women’s Health Care. 2018; 3(2): 1–4
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe