
O schimbare considerată „seismică” în gândirea oncologică medicală, imunoterapia celulară este încă la început, cu potenţial uriaș.
Termenul de imunoterapie celulară (ITC) antitumorală se referă la administrarea de celule vii imunocompetente unui pacient cu cancer pentru a elimina celulele maligne ale acestuia. Ea poate fi activă, precum utilizarea de celule dendritice, care pot stimula un răspuns imun antitumoral, sau pasivă, în care celulele administrate au o activitate specific antitumorală intrinsecă.
Aceasta din urmă a fost denumită „ITC adoptivă” sau „transfer celular adoptiv” și folosește limfocite autologe sau alogene modificate sau nu in vitro. Limfocitele transferate au fost în prealabil în contact imunologic sau, altfel spus, sensibilizate („primed”) in vivo sau ex vivo cu antigenul vizat. Pentru a avea un efect antitumoral eficient, aceste limfocite trebuie să recunoască antigenul tumoral ales, să fie în număr adecvat, să fie capabile de a ajunge la celulele tumorale și de a avea capacităţi citotoxice pentru distrugerea acestora.
Utilizarea celulelor vii ca medicament în cancer a reprezentat o schimbare considerată „seismică” în gândirea medicală oncologică în raport cu reprezentarea tradiţională a unui medicament, fie el o substanţă chimică sau biologică. Aceasta deoarece limfocitele sunt elemente dinamice, cu o „viaţă” proprie, influenţabile de mediul în care se află, interacţionează cu alte celule și pot produce o gamă mai largă de răspunsuri, prin căi complexe de semnalizare. Mai mult, medicamentele celulare pot persista în organism luni și chiar ani, creând interacţiuni complexe pacient-medicament, încă incomplet cunoscute.
În prezent există patru feluri de imunoterapie celulară, trei bazate pe limfocitul T și una pe limfocitul NK, și anume:
Dintre acestea, numai imunoterapia adoptivă cu limfocite T dotate cu receptor chimerizat a fost aprobată pentru utilizare în practica oncohematologică.
O altă formă de imunoterapie celulară este transplantul medular prin efectul de grefă-contra-leucemie, dar dezvoltarea acestui subiect depășește cadrul de faţă (aspecte ale transplantului medular se pot găsi și în „Viaţa Medicală” nr. 2/15.01.2021 și 3/22.01.2021).
Terapia adoptivă cu limfocite T care exprimă un receptor pentru antigen chimerizat (chimeric antigen receptor T – CAR-T) utilizează limfocite T autologe „înarmate” cu un CAR. Utilizarea CAR-T a apărut ca una dintre cele mai promiţătoare modalităţi de imunoterapie celulară antitumorală, demonstrând o activitate de o eficacitate remarcabilă îndeosebi în hemopatiile maligne.
Limfocitele T dotate cu CAR dobândesc abilitatea de a detecta și distruge celulele maligne prin combinarea specificităţii unui anticorp monoclonal cu capacitatea de memorare și citotoxicitate a limfocitelor T endogene, comportându-se ca un efector imun bispecific, în acest caz celular.
În forma sa din primele generaţii, CAR-T apare alcătuit din patru domenii principale (Fig. 1): unul extracelular (abreviat scFv), constând din regiunea variabilă a unui anticorp monoclonal specific; un domeniu intracelular format din regiunea de semnalizare intracelulară a receptorulului limfocitului T (notat CD3zeta); și un segment costimulator reprezentat de molecule notate CD28/4-1BB/OX40, domenii unite prin cel de legare transmembranar.
Fig. 1. Structura CAR. (Reprodus după Leuk Lymph Soc, 2018)

Domeniul extracelular asigură recunoașterea și legarea limfocitului T de antigenul tumoral și dă semnalul de activare a acestuia, în timp ce domeniul intracelular mediază activarea, proliferarea și secreţia de citokine și în final distrugerea celulelor tumorale, cu contribuţia segmentului costimulator, care asigură, printre altele, supravieţuirea de durată a limfocitelor T purtătoare de CAR în organism.
Complexitatea CAR a crescut treptat, acesta aflându-se deja la a cincea generaţie. Specificitatea produselor CAR-T utilizate până în prezent este pentru antigenul CD19 aflat pe limfocitul B și pentru BCMA aflat pe suprafaţa plasmocitului. Diferite alte antigene constituie ţinte potenţiale pentru produse CAR-T aflate în studiu.
CAR-T este un complex proteic produs în laborator, ale cărui gene codificatoare sintetizate prin editare genică sunt transfectate în limfocitele T anteprelevate prin leucafereză (prin transfecţie se înţelege transferul, prin diverse metode și vectori, într-o celulă-gazdă a uneia sau mai multor gene, care sunt inserate în genomul acesteia).
Termenul de chimerizat sau chimeric se referă în acest caz la proteine (denumite și proteine hibride) create prin unirea a două sau mai multor gene, care iniţial codificau aceste proteine separat.
Rezultatul este o genă de fuziune, a cărei translatare duce la sinteza uneia sau a mai multor polipeptide, cu proprietăţi funcţionale derivate din fiecare din proteinele iniţiale. După activare și multiplicare ex vivo prealabilă, limfocitele CAR-T sunt reintroduse pacientului, care este pregătit să le „facă loc” printr-o „precondiţionare” (cu chimioterapie citostatică), care produce depleţia limfocitelor proprii (Fig. 2).
Fig. 2. Ilustrare a etapelor imunoterapiei adoptive cu limfocite T modificate genetic. (Reprodus din Zhao L., Cao Yu J., 2019)
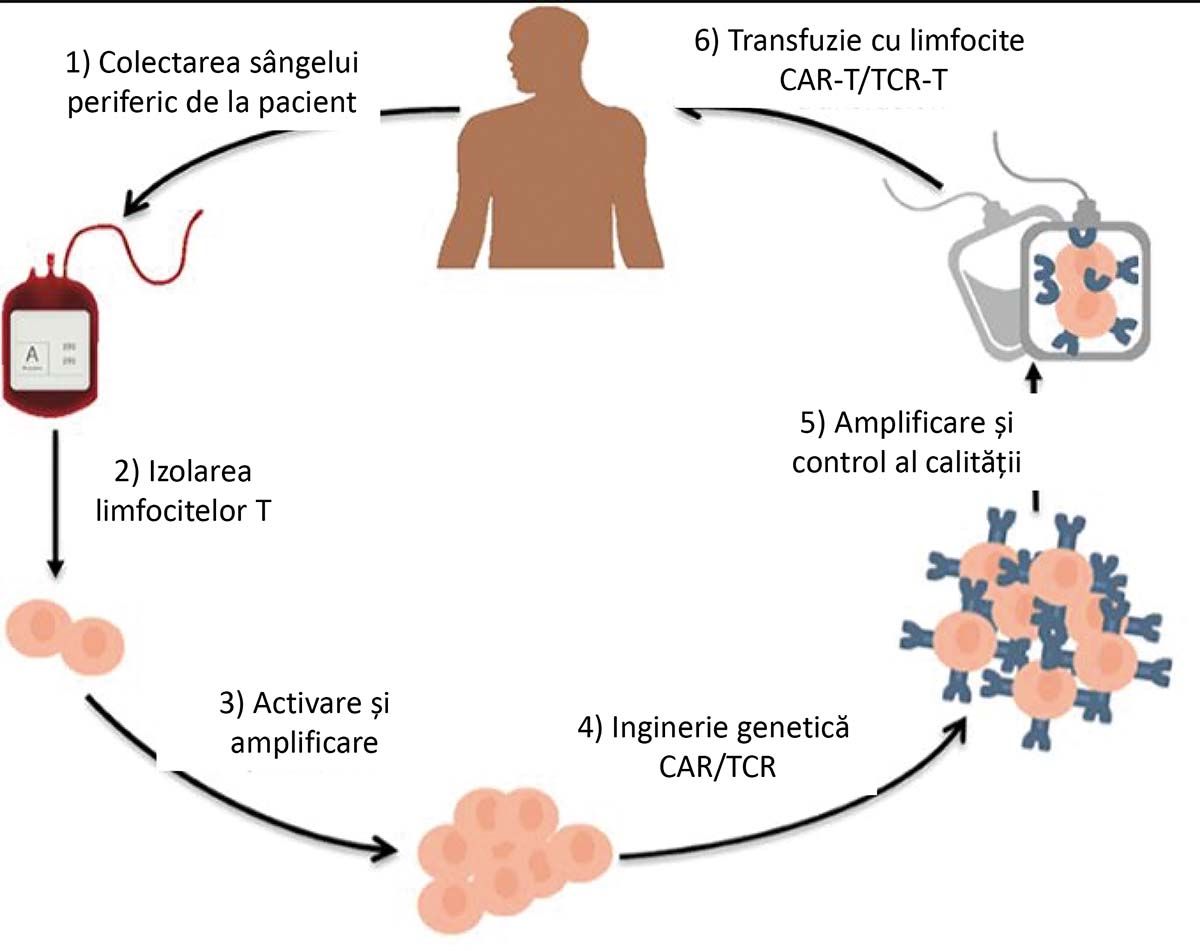
Există șase proceduri de imunoterapie adoptivă constând din administrarea de limfocite CAR-T în terapia hemopatiilor maligne aprobate de Administraţia pentru Controlul Alimentelor și Medicamentelor din SUA pentru utilizare în practica clinică. Ele se aplică numai la cazurile primar refractare sau în recădere după mai multe linii de tratament diagnosticate cu limfoproliferări tip B acute și cronice și mielom multiplu (Tabelul), rata de răspunsuri variind de la 90% la 70% sau 51%, în funcţie de afecţiune.
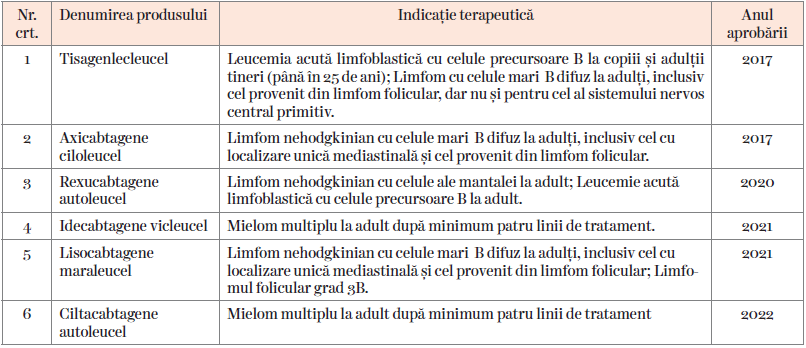
Totuși, deși rezultatele sunt considerate spectaculoase, constând în multe cazuri din instalarea rapidă a unei remisiuni complete, profunde, această terapie se confruntă în practica reală cu o serie de obstacole, precum rezistenţa la tratament la un număr de cazuri, eficacitate de durată limitată (uneori de numai patru luni), toxicitate deloc neglijabilă (incluzând sindromul de eliberare de citokine, neurotoxicitate, sindrom de activare a macrofagelor, aplazia limfocitelor B), complexitate procedurală (necesită centre specializate certificate și acreditate) și cost ridicat.
Aflată la începuturile ei, imunoterapia cu limfocite T-CAR reprezintă o autentică speranţă pentru pacienţii hematologici și medicii implicaţi, constituind în continuare un amplu domeniu de cercetare pentru creșterea performanţei și a toleranţei. Ea urmează a fi implementată și în practica oncohematologică din România prin eforturile hematologilor, și nu numai, din Institutul Clinic Fundeni, București.
Citește și: Imunoterapia umorală în hemopatiile maligne
Bibliografie
1. Sermer D. et al. Outcomes în patients with DLBCL treated with commercial CAR T cells compared with alternate therapies. Blood Adv 2020, 4(19):4669
2. Cirillo M. et al. Cellular immunotherapy for hematologic malignancies: beyond bone marrow transplantation. Biol Blood Marrow Transplant 24 (2018):433
3. Xu Z., Huang X. Cellular immunotherapy for hematological malignancy: recent progress and future perspectives. Cancer Biol Med 2021,18(4):967
4. Basar R. et al. Next-generation cell therapies: the emerging role of CAR-NK cells. Blood Adv 2020,4(22): 5868
5. Liu S. et al. NK cell based cancer immunotherapy: from basic biology to clinical development. J Hematol Oncol 2021,14:7
6. Hayes C. Cellular immunotherapies for cancer. Irish Journal of Medical Science 2021,190:41
7. Zhao L ., Cao Yu J. Engineered T cell therapy for cancer în the clinic. Front. Immunol. 2019,10:2250
8. Lu H.et al. From CAR-T Cells to CAR-NK Cells: A developing immunotherapy method for hematological malignancies. Front. Oncol. 2021,11:720501
9. Leukemia and Lymphoma Society. Facts about chimeric antigen receptor (CAR) T-cell therapy, 2018
10. Wells D.A. et al. A Review of CAR T-cell therapies approved for the treatment of relapsed and refractory B-cell lymphomas. J Hematol Oncol Pharm. 2022;12(1):30
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe