
Prezentarea succintă a principalelor diferenţe între tumorile lichide și cele solide poate fi utilă medicilor din diverse specialităţi și administratorilor din Sănătate, în contextul lansării Planului Naţional de Combatere a Cancerului 2022.

Termenul de cancer cuprinde un grup numeros și heterogen de boli care au la bază fenomenul de transformare neoplazică malignă a celulelor unui ţesut sau organ, fenomen biologic prin care acestea dobândesc capacitatea de a se înmulţi exagerat și necontrolat și de a invada ţesuturile înconjurătoare și de la distanţă.
Din punct de vedere clinic, o boală canceroasă se manifestă, cel mai adesea, prin mase (formaţiuni) tumorale rezultate din aglomerarea celulelor maligne generate în diferitele organe interesate, de unde și denumirea de „tumori solide” (TS), denumire încetăţenită și utilizată tot mai frecvent în literatura medicală. Mai puţin frecvent, boala canceroasă este de la început difuză și nu realizează în genere aglomerări celulare vizibile, de unde și denumirea acordată prin simetrie, dar mai puţin folosită, de „tumoră lichidă” (TL).
Dacă în TS celula malignă transformată este generată într-un ţesut ce are consistenţă, în TL aceasta provine dintr-un ţesut fluid, respectiv măduva osoasă, sânge circulant sau limfă. Cea de a doua categorie, cea a TL, cuprinde, conform definiţiilor actuale, leucemiile, limfoamele, mielomul multiplu, cărora li s-au adăugat sindromul mielodisplazic și neoplaziile mieloide cronice, afecţiuni reunite în ansamblu sub numele de neoplazii maligne hematologice sau hemopatii maligne (HM).
Această diferenţiere este grevată de aproximări, deoarece în HM se întâlnesc, în diferite momente ale evoluţiei, formaţiuni tumorale chiar voluminoase, cum ar fi, de exemplu, pachete ganglionare în limfoame, splenomegalii masive în mieloproliferări cronice. Totuși, termenii TS și TL s-au păstrat, ei conferind o mai simplă și fluentă comunicare în cadrul limbajului medical.
Au fost relevate în timp o serie de diferenţe importante între TL și TS, care au determinat crearea de departamente separate pentru îngrijire și de subspecialităţi dedicate, precum hemato-oncologia.
În SUA, în 2021, HM au reprezentat circa 10% (186.400 de cazuri) dintre cele aproximativ două milioane de cazuri noi de cancer diagnosticate, ele fiind responsabile de 9,5% dintre decesele prin cancer. HM ocupă locul al cincilea în cadrul cancerelor diagnosticate în Marea Britanie în 2021.
În timp ce TS afectează preponderent populaţia de vârstă mijlocie, TL sunt mai frecvente la copii și la vârstnici, constituind cancerul cel mai des întâlnit la vârsta copilăriei (45% dintre diagnosticele stabilite la grupa de vârstă 0-14 ani). Leucemia acută limfoblastică este responsabilă de 25% dintre formele de cancer diagnosticate la copii și adolescenţi cu vârsta până în 20 de ani.
În TL, o serie de manifestări clinice sunt sugestive pentru diagnostic (de exemplu, hipertrofia gingivală în leucemia acută mieloidă, adenopatii cu multiple localizări și dispunere simetrică în leucemia limfatică cronică și în limfoamele indolente, infiltrare amigdaliană bilaterală în limfoproliferări cronice, adenopatii însoţite de prurit și febră în limfomul Hodgkin, splenomegalie voluminoasă în mieloproliferările cronice). Ele se pot instala acut, cu afectare marcată a stării generale. Paloarea și hemoragiile cutaneo-mucoase domină tabloul clinic, iar complicaţiile infecţioase sunt frecvente pe tot parcursul evoluţiei.
Comparativ cu TL, în TS manifestările clinice sunt mai heterogene, variind în funcţie de localizarea și de stadiul clinic al bolii, cu apariţie și progresie în general insidioase, lent progresive.
Tot în TS, testele de laborator sunt puţin modificate până în fazele avansate și sunt nesugestive pentru diagnostic, interesarea măduvei osoase fiind rară și având loc doar în fazele terminale.
În TL, rezultatele investigaţiilor de laborator sunt cel mai adesea intens și variat modificate încă de la diagnostic. Elemente precum, de exemplu, prezenţa blaștilor leucemici cu corpi Auer sau a unui component monoclonal în sângele periferic au o valoare definitorie. Interesarea măduvei osoase este frecventă încă de la diagnostic, și examinarea cito-histopatologică a acesteia este un act medical de rutină.
Imunofenotiparea prin citometrie în flux este o investigaţie specifică și indispensabilă în hemato-oncologie pentru stabilirea unui diagnostic precis și rapid, îndeosebi în leucemiile acute și limfoproliferările cronice, dar nu este utilizată de rutină în TS. De asemenea, examenul citogenetic se dovedește mult mai util pentru diagnostic și îndeosebi pentru evaluarea prognosticului în TL faţă de TS.
Ca urmare a diferenţelor de ordin clinic și paraclinic, triajul în populaţie în scopul diagnosticării precoce a unor cancere (screeningul) este aplicabil și se dovedește util pentru creșterea duratei de viaţă a pacienţilor doar în TS, având și un raport cost/beneficiu favorabil.
Tratamentul TS are la baza rezecţia chirurgicală – extirparea chirurgicală a tumorii –, chimioterapia citostatică/imunoterapia umorală și radioterapia locoregională, iar chimioterapia are rol adjuvant în stadiile iniţiale ale bolii. În TL, însă, chimioterapia citostatică în combinaţie sau nu cu imunoterapia este folosită mai pe larg încă din stadiile iniţiale ale bolii. În TL, medicamentele citostatice eficiente sunt în cea mai mare parte diferite de cele aplicate în TS, iar ponderea terapiilor ţintite este mai mare. De asemenea, necesarul de sânge și derivate ale sale, de antibiotice și antimicotice este semnificativ mai crescut în TL.
Imunoterapia umorală, cu excepţia inhibitorilor punctelor de control (anti-CTLA4, PD-1 și PD-L1), este mai puţin eficace în TS decât în TL. Numărul de anticorpi monoclonali aprobaţi pentru terapia TS este de circa două ori mai mic faţă de cel aprobat pentru terapia TL (a se vedea și Viaţa Medicală nr. 13/2022).
Se consideră că eficacitatea mai mică a inhibitorilor punctelor de control în TL e consecinţa comportamentului disfuncţional al limfocitelor T, indus de celula tumorală hemato-limfopoietică în urma contactului direct cu acestea, fenomen denumit „ignoranţă imunologică”. În acest caz, limfocitele T se află în număr normal și proliferează adecvat ca răspuns la stimulii antigenici, dar ele nu sunt apte să atace celulele tumorale, ca și cum le-ar ignora printr-un proces de „letargie metabolică”, un comportament diferit de cel manifestat împotriva celulelor tumorilor solide.
Relativ recent introdusa imunoterapie celulară reprezentată de terapia cu limfocite de tip T chimerizate („CAR-T”), care a înregistrat un succes remarcabil în TL (a se vedea și Viaţa Medicală nr. 14/2022), manifestă deocamdată o eficienţă redusă în TS, din cauza diferenţelor în reprezentarea și dispunerea antigenică a celulelor tumorale.
Transplantul de măduvă osoasă (TMO) reprezintă o procedură frecvent folosită în terapia TL, atât ca tratament de primă linie (autotransplant în mielomul multiplu), cât și ca tratament de consolidare în leucemiile acute (alotransplant) sau în limfoamele refractare, după terapie de salvare. Nu este utilizat în TS.
Costul asistenţei medicale este mai ridicat (de circa trei ori) în TL, îndeosebi ca urmare a utilizării mai îndelungate a tratamentului specific, a necesarului crescut de antibiotice și antimicotice, de sânge și derivatele sale și de factori de creștere granulocitari și eritrocitari (figura).
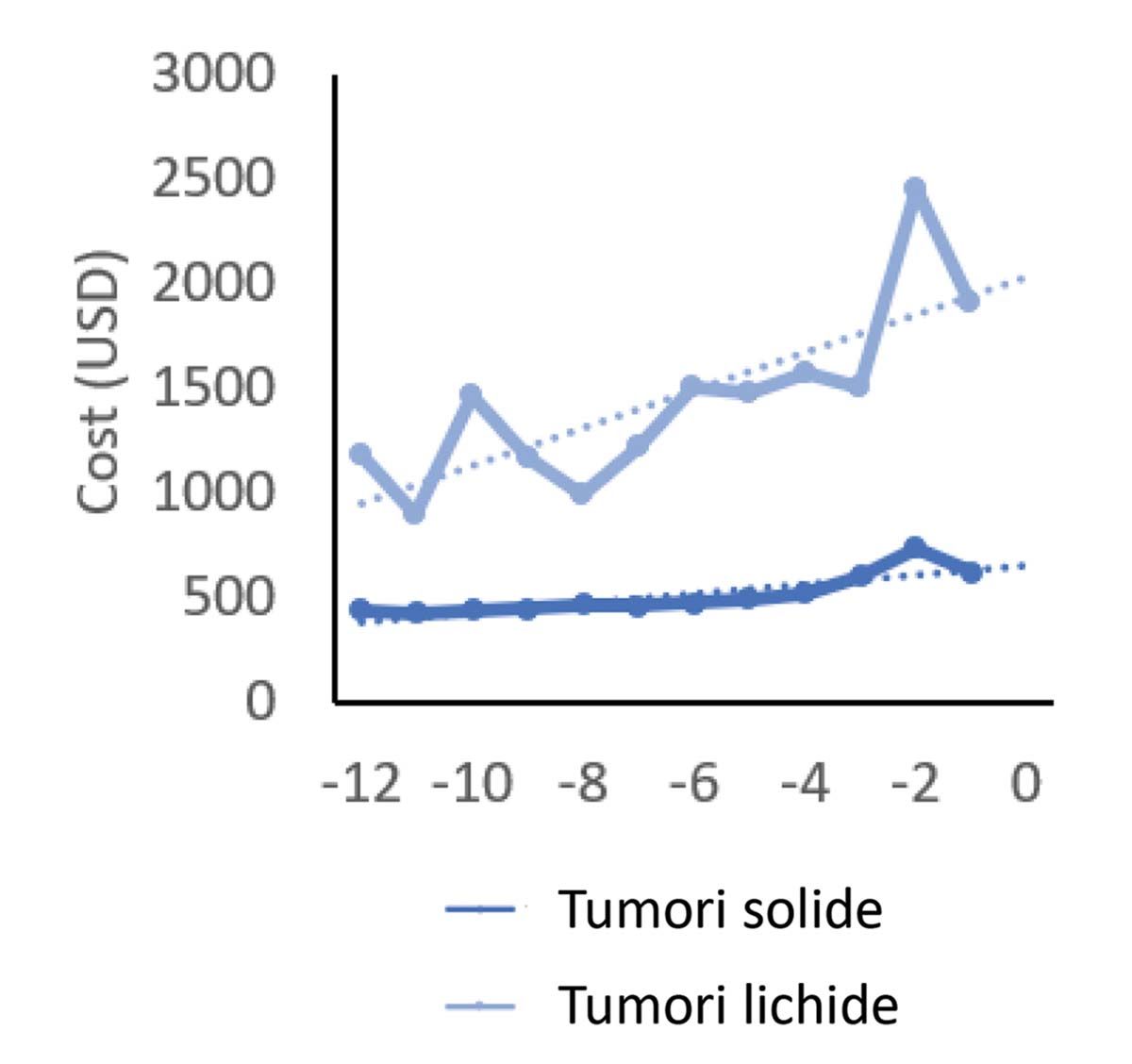
TL se asociază cu costuri mai mari de îngrijire și cu utilizarea mai frecventă a secţiilor de terapie intensivă.
Preocuparea sistemelor de sănătate pentru asigurarea îngrijirilor medicale pentru pacienţii oncologici aflaţi în faza terminală a bolii a cunoscut o traiectorie ascendentă în ţările civilizate, existând un interes continuu pentru asigurarea unor abordări adecvate, adaptate situaţiilor, fără o creștere exagerată a costurilor. Cu scopul de a furniza factorilor implicaţi responsabili elemente utile, au fost efectuate studii care au relevat o serie de diferenţe între situaţia pacienţilor cu TS faţă de a celor cu TL, precum:
Bibliografie
1. Yang S-Y, et al. Haematological cancer versus solid tumour end-of-life care: a longitudinal data analysis. BMJ Supportive & Palliative Care 2020
2. Montironi C. et al. Hematopoietic versus solid cancers and T cell dysfunction: looking for similarities and distinctions. Cancers 2021,13:284
3. LeBlanc T. W. et al. What is different about patients with hematologic malignancies? A retrospective cohort study of cancer patients referred to a Hospice Research Network. Journal of Pain and Symptom Management 2015, 49(3):505
4. Patel U. et al. CAR-T cell therapy in solid tumors: A review of current clinical trials. eJHaem 2022; 3(Suppl.1):24–31
5. Kirtane K. et al. Adoptive cellular therapy in solid tumor malignancies: review of the literature
and challenges ahead. Journal for ImmunoTherapy of Cancer 2021;9:e002723.
6. Mora J.et al. Autologous stem-cell transplantation for high-risk neuroblastoma: historical and ritical review. Cancers 2022, 14:2572
7. Tran G., Zafar S.Y. Financial toxicity and implications for cancer care in the era of molecular and immune therapies
8. Pham T. et al, An update on immunotherapy for solid tumors: A Review. Ann Surg Oncol 2018
9. Mancini S.J.C.,et al. Deciphering tumor niches: lessons from solid and hematological malignancies.
Front. Immunol. 2021
10. Trujillo S.C. et al. In Vitro Modeling of Non-Solid Tumors: How Far Can Tissue Engineering Go?
Int. J. Mol. Sci. 2020,21:5747
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe