Istoria tratamentului infecţiei cu virus
hepatitic B (VHB) este strâns legată de istoria virusului hepatitic B.
Descoperit în 1956 prin evidenţierea AgHBs, virusul hepatitic B a fost
identificat, câţiva ani mai târziu, la microscopia electronică sub forma
particulei Dane. În următorii ani, s-au putut stabili cu precizie ciclul de viaţă
al virusului şi semnificaţia markerilor virali privind evoluţia bolii şi riscul
de cronicizare. Omul este principala gazdă, iar ficatul este principalul organ
în care VHB se multiplică. Pătrunderea VHB în organism se face pe cale
parenterală şi principalul organ ţintă este ficatul, întrucât hepatocitele au
cea mai mare densitate de receptori pe care se fixează VHB şi cea mai mică
densitate de HLA, astfel încât hepatocitele găzduiesc cea mai ridicată
cantitate de VHB cu cea mai redusă posibilitate de eliminare imunologică a
virusului. În afara ficatului, şi alte organe – ca de exemplu splina,
intestinul subţire – sunt considerate ţinte şi devin sanctuare extrahepatice
unde virusul se fixează şi se replică. Odată pătruns în hepatocite, VHB îşi
desface mantaua, eliberează nucleocapsida, evidenţiază revers-transcriptaza şi
începe replicarea. Spre deosebire de virusul hepatitic C (VHC), VHB pătrunde în
nucleu şi aici continuă ciclul de replicare şi de stocare a informaţiei genetice
sub formă de cccDNA. În nucleu, VHB codifică şi arhivează informaţia genetică şi,
independent de procesul de arhivare, pătrunde în genomul celulei gazdă, pe
care îl dezorganizează, uneori cu efecte oncogene.
În fiecare din etapele de replicare a VHB,
exceptând forma cccDNA, se poate interveni terapeutic. Fapt remarcabil, spre
deosebire de virusul hepatitic C, în infecţia VHB dispunem de un vaccin
eficient, cu protecţie de 95–96%. Introducerea vaccinului a condus la scăderea
incidenţei şi a prevalenţei infecţiei VHB în întreaga lume, rămânând însă
importante rezervoare de purtători aparent sănătoşi sau bolnavi şi care necesită
tratament antiviral.
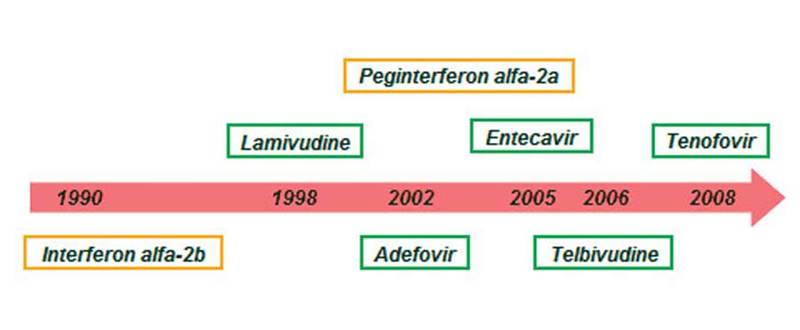
Primul antiviral anti-VHB administrat a
fost interferonul, în 1996. Ulterior, s-au introdus şi dezvoltat analogii de
nucleoz(t)ide, în prezent fiind disponibile cinci substanţe cu efect antiviral
dovedit.
Interferonul
Interferonul este primul antiviral utilizat
în terapia hepatitei cronice VHB. A fost introdus în 1981, iar in 2001 a fost
aprobat interferonul pegylat.
Inteferonul a are efecte antivirale,
antiproliferative şi imunomodulatoare, demonstrându-se că induce supresia
replicării virale şi remisiunea bolii hepatice. Este tratamentul de primă linie
pentru pacienţii tineri, cu viremii mici, dar transaminaze crescute, în
cirozele compensate şi pentru virusurile B cu genotip A sau B.
Dezavantajele acestei terapii constau în
administrarea injectabilă, neplăcută uneori pentru pacient, reacţii adverse
frecvente şi, nu în ultimul rând, preţul foarte mare.
rând, preţul foarte mare.
În 2005, a fost realizat un studiu, pe un
lot de 814 pacienţi cu AgHBe pozitiv. Un lot de pacienţi a fost tratat cu
peginterferon, un al doilea lot cu lamivudină şi un al treilea lot cu lamivudină
şi peginterferon. Concluzia studiului a fost că, la sfârşitul săptămânii 72,
pacienţii trataţi cu peginterferon aveau toţi parametrii urmăriţi (nivelul
ADN-VHB, seroconversia AgHBe, nivelul transaminazelor) net superiori celor
trataţi cu lamivudină, iar biterapia peginterferon plus lamivudină nu a adus
beneficii considerabile. În prezent, peginterferonul rămâne terapia de bază în
infecţia cu VHB la pacienţii tineri, cu viremii scăzute şi genotip VHB tip A.
Lamivudina
Lamivudina a fost aprobată în tratamentul infecţiei
cu VHB în 1998. Este primul medicament cu administrare orală \n tratamentul
acestei infecţii. Este un analog de nucleoz(t)ide şi acţionează prin inhibarea
ADN-sintetazei. Este foarte bine tolerat de pacient, nu are efecte adverse
notabile şi are un preţ scăzut.
Principalul dezavantaj al acestei terapii
este dezvoltarea rapidă a rezistenţei din cauza unui prag scăzut al rezistenţei
primare. Astfel, 23% din pacienţii trataţi dezvoltă rezistenţă în domeniul YMDD
al ADN-polimerazei (codonul rtM204V/I/S) la un an de terapie, crescând la 46%
la doi ani, 55% la trei ani şi 65–71% la patru şi cinci ani, aceste valori
modificându-se în funcţie de zona geografică.
Riscul de a dezvolta rezistenţă la
lamivudină este direct proporţional cu nivelul viremiei. Pacienţii cu nivelul
ADN-VHB mai mic de 200 copii/ml după şase luni de tratament au risc de a
dezvolta rezistenţă de numai 8,3%, comparativ cu 60% pentru cei cu viremii mai
mari de 200 copii/ml.
Doza recomandată este de 100 mg/zi la
pacienţii cu funcţie renală normală şi terapia trebuie continuată până la
seroconversia AgHBe. Astăzi,  lamivudina este recomandată în tratamentul
cirozelor hepatice, infecţia VHB stadiul Child B sau C, la pacienţii cu boli
oncologice sau hematologice maligne, precum şi la pacienţii vârstnici.
lamivudina este recomandată în tratamentul
cirozelor hepatice, infecţia VHB stadiul Child B sau C, la pacienţii cu boli
oncologice sau hematologice maligne, precum şi la pacienţii vârstnici.
Adefovirul
Adefovir dipivoxil este analog de
nucleoz(t)ide aprobat în tratamentul infecţiei VHB în 2002. Acţioneaza prin
inhibarea ADN polimerazei şi se administrează \n doze de 10 mg/zi. Este util la
pacienţii naivi terapeutic, dar şi la cei care au urmat tratament cu lamivudină
şi au dezvoltat rezistenţă, precum şi la pacienţii AgHBe pozitiv cu niveluri scăzute
ale ADN-VHB, în terapia de lungă durată, adefovirul poate induce toxicitate
renală. Adefovirul rămâne indicaţia de bază la pacienţii care au urmat
tratament cu lamivudină şi au dezvoltat rezistenţă la acesta.
Entecavirul
Entecavirul a fost aprobat în SUA în 2005
iar în Europa (şi în România) în 2007. Este, de asemenea, un analog de
nucleoz(t)ide. Într-un studiu cu entecavir, în săptămâna 96, 80% din pacienţii
trataţi aveau niveluri nedetectabile ale viremiei, faţă de numai 30% din
pacienţii trataţi cu lamivudină. Totodată, rata seroconversiei AgHBe ajunge la
31% în săptămâna 96, faţă de 26% la pacienţii trataţi cu lamivudină.
Entecavirul a fost aprobat pentru
tratamentul pacienţilor cu rezistenţă la lamivudină, fiind al doilea medicament
cu această caracteristică, după adefovir. La pacienţii trataţi cu entecavir, nu
a fost depistat niciun caz de rezistenţă în primii doi ani de tratament, iar
printre pacienţii cu rezistenţă la lamivudină, riscul de a dezvolta rezistenţă
la entecavir este de 6% în primul an şi de 9% în al doilea an. Este recomandat
în tratamentul infecţiei cronice VHB cu AgHBe pozitiv şi încărcătură virală
mare, se administrează în doză de 0,5 mg/zi (1 mg/zi la pacienţii cu rezistenţă
la lamivudină).
Tenofovirul
Tenofovirul este tot un agent
nucleoz(t)idic, cu structură similară celei a adefovirului, fiind diferit de
acesta printr-o singură grupare metil. A fost aprobat pentru tratamentul infecţiei
HIV în 2002 şi pentru tratamentul infecţiei VHB în 2008. Studii clinice au arătat
că, la 48 de săptămâni de terapie cu tenofovir, nivelul ADN-VHB a fost
nedetectabil la 76% din subiecţii AgHBe pozitiv şi 93% la cei AgHBe negativ.
Discuţii
Entecavirul şi tenofovirul sunt antivirale
de primă linie în infecţia VHB, fără risc de a dezvolta rezistenţă şi cu o rată
crescută de seroconversie, atât în sistemul antigenic „e“, cât şi în sistemul
antigenic „s“.
În cadrul terapiei cu analogi nucleozidici
sau nucleotidici (NUC), se ridică următoarele probleme: durata crescută a tratamentului,
uneori luni sau ani până la seroconversie; efectele secundare posibile;
costurile ridicate ale tratamentului şi monitorizării. Principalele efecte
adverse ale analogilor sunt legate de nefrotoxicitate (observată uneori la adefovir
şi tenofovir, dar sub 1–2%), precum şi de inducerea acidozei lactice.
Monitorizarea funcţiei renale şi a parametrilor funcţiei tubului proximal
(glicozurie, albuminurie, fosfaturie) permite depistarea precoce a modificărilor
funcţionale nefrologice, care sunt reversibile. Experienţa Centrului de Medicină
Internă şi Nefrologie din Institutul Clinic Fundeni, de peste 400 de pacienţi,
ne-a arătat că nu se întâlnesc
efecte nefrologice la entecavir, iar pentru adefovir şi tenofovir acestea sunt
rare şi perfect reversibile.
funcţiei renale şi a parametrilor funcţiei tubului proximal
(glicozurie, albuminurie, fosfaturie) permite depistarea precoce a modificărilor
funcţionale nefrologice, care sunt reversibile. Experienţa Centrului de Medicină
Internă şi Nefrologie din Institutul Clinic Fundeni, de peste 400 de pacienţi,
ne-a arătat că nu se întâlnesc
efecte nefrologice la entecavir, iar pentru adefovir şi tenofovir acestea sunt
rare şi perfect reversibile.
Privind importanţa terapiei combinate vs. monoterapie în infecţia VHB, date
recente atrag atenţia că asocierea imunomodulatoarelor cu efect antiviral cu
NUC, cu efect direct antiviral, dă rezultate mai bune în ceea ce priveşte
negativarea viremiei şi seroconversia AgHBs, faţă de monoterapia cu interferon
sau cu NUC. Explicaţia fenomenului constă în faptul că, pentru eliminarea AgHBs
şi apariţia anticorpilor anti-HBs, rolul cel mai important îl joacă stimularea
răspunsului imun de către interferon. Pe baza acestei observaţii, se estimează
că, în viitor, este puţin probabil să se renunţe la interferon în terapia VHB,
astfel încât această terapie încă rămâne o opţiune terapeutică importantă în
tratamentul infecţiei VHB, sub formă de monoterapie sau, mai bine, de terapie
combinată cu NUC.
Ghidul german de tratament al infecţiei VHB
are în vedere ca terapia de primă linie să fie peginterferon a2a, 180 µg/săptămână, cu control la patru şi
12 săptămâni. Scăderea cu mai puţin de 1 log la patru săptămâni şi persistenţa
la 12 săptămâni determină stoparea tratamentului cu peginterferon a2a. De
asemenea, ghidul elaborat de American Association for the Study of Liver
Diseases menţionează că, pentru pacienţii cu infecţie cronică VHB (AgHBe
pozitiv sau negativ), terapia se poate face cu oricare dintre cele şapte
substanţe antivirale, dar recomandabile sunt peginterferonul a2a, tenofovirul şi
entecavirul.
Concluzii
Tratamentul
infecţiei VHB a făcut progrese remarcabile în ultimii ani şi, în prezent, opţiunile
terapeutice existente reuşesc să reducă rapid şi eficient încărcătura virală.
Viremiile devin negative la numai două-patru săptămâni de la începerea
tratamentului. La 8–10% din bolnavi, se produce dispariţia AgHBs şi
seroconversia, cu apariţia anticorpilor anti-HBs. ¥inta finală a tratamentului
o constituie eradicarea completă a infecţiei, obiectiv irealizabil până în
prezent, din cauza persistenţei în nucleul celular a formei de arhivare a
informaţiei genomice cccDNA.
 rând, preţul foarte mare.
rând, preţul foarte mare. lamivudina este recomandată în tratamentul
cirozelor hepatice, infecţia VHB stadiul Child B sau C, la pacienţii cu boli
oncologice sau hematologice maligne, precum şi la pacienţii vârstnici.
lamivudina este recomandată în tratamentul
cirozelor hepatice, infecţia VHB stadiul Child B sau C, la pacienţii cu boli
oncologice sau hematologice maligne, precum şi la pacienţii vârstnici.  funcţiei renale şi a parametrilor funcţiei tubului proximal
(glicozurie, albuminurie, fosfaturie) permite depistarea precoce a modificărilor
funcţionale nefrologice, care sunt reversibile. Experienţa Centrului de Medicină
Internă şi Nefrologie din Institutul Clinic Fundeni, de peste 400 de pacienţi,
ne-a arătat că nu se întâlnesc
efecte nefrologice la entecavir, iar pentru adefovir şi tenofovir acestea sunt
rare şi perfect reversibile.
funcţiei renale şi a parametrilor funcţiei tubului proximal
(glicozurie, albuminurie, fosfaturie) permite depistarea precoce a modificărilor
funcţionale nefrologice, care sunt reversibile. Experienţa Centrului de Medicină
Internă şi Nefrologie din Institutul Clinic Fundeni, de peste 400 de pacienţi,
ne-a arătat că nu se întâlnesc
efecte nefrologice la entecavir, iar pentru adefovir şi tenofovir acestea sunt
rare şi perfect reversibile.