În ultimii ani au fost descrise şi alte
roluri ale leptinei, printre care:
–Promovarea creşterii liniare prin
mecanisme multiple: balanţă energetică pozitivă, inducţia mitozei în mai multe
tipuri de celule printre care şi condrocitele de la nivelul cartilajelor de creştere,
stimularea secreţiei de hormon de creştere la nivel hipofizar;
–Acţiune permisivă de inducere a pubertăţii
la mamifere, fără însă ca prezenţa sa să fie un factor determinant pentru
debutul pubertar; o dovadă indirectă a rolului său în inducerea pubertăţii la
om este dată de hipogonadismul hipogonadotrop ce caracterizează pacienţii cu
mutaţii ale genei ob;
–Modulează funcţia reproductivă la
adulţi, având acţiune permisivă pentru eliberarea pulsatilă de GnRH la nivelul
hipotalamusului (creşte frecvenţa pulsaţiilor, nu şi amplitudinea lor,
determinând eliberarea de FSH şi LH de la nivelul hipofizei; s-au descris
receptori pentru leptină la nivelul celulelor foliculare ovariene şi al celulelor
Leydig, precum şi ARNm pentru leptină la nivelul celulelor granuloase în
foliculul preovulator, sugerând un rol direct al leptinei asupra funcţiei
ovariene;
–Modulează secreţia de GH prin
receptorii specifici descrişi la nivelul nucleului arcuat şi periventricular –
administrarea fragmentului leptinic 126–140 la adulţi sănătoşi a determinat scăderea
secreţiei de GH prin efect inhibitor asupra eliberării de GHRh; efectul
inhibitor al leptinei asupra secreţiei de GH este sugerat şi de dovezi
indirecte – pacienţii cu obezitate sau cu sindrom Cushing, care au şi niveluri
serice crescute de leptină asociază niveluri scăzute de GH, iar în cazurile de
malnutriţie – caracterizate prin niveluri crescute de leptină – nivelurile
serice de GH sunt reduse;
–
Intervine în modularea activităţii axului
hipotalamo-hipofizo-suprarenal, scăzând expresia CRH la nivelul nucleilor
hipotalamici paraventriculari; pulsaţiile secretorii ale leptinei se corelează
în mod negativ cu pulsaţiile secreţiei de ACTH; în plus, leptina scade sinteza
de cortizol ACTH-mediată prin scăderea expresiei receptorului pentru ACTH şi a
enzimelor steroidogenezei sTAR şi a P450c21;
lep –
Determină activare tiroidiană prin
mecanism central: scăderea producţiei de leptină este însoţită experimental de
scăderea producţiei de TRH hipotalamic, iar mutaţiile leptinei/ale receptorului
său determină hipotiroidism central, care se ameliorează prin administrarea de
leptină;
–
Determină activare tiroidiană prin
mecanism central: scăderea producţiei de leptină este însoţită experimental de
scăderea producţiei de TRH hipotalamic, iar mutaţiile leptinei/ale receptorului
său determină hipotiroidism central, care se ameliorează prin administrarea de
leptină;
–
Are un rol determinant în dezvoltarea neuronală – şoarecii ob/ob şi db/db au o greutate redusă a creierului, care la cei ob/ob poate fi reversibilă la
administrarea de leptină; de asemenea leptina pare să inducă proliferarea
mitotică în diferite regiuni ale creierului şi ale hipotalamusului, determinând
astfel maturarea circuitelor centrale care controlează aportul alimentar;
– Contribuie la dezvoltarea osului şi la creşterea
şi funcţionarea pulmonară;
– Influenţează răspunsul imun şi pe cel
inflamator; are rol proinflamator prin creşterea expresiei limfocitelor TH1
(cu rol proinflamator) în detrimentul limfocitelor TH2 (cu rol antiinflamator);
şoarecii mutanţi pentru leptină sunt protejaţi de apariţia bolilor autoimune şi
există raportări în literatură conform cărora pacienţii cu artrită reumatoidă
au avut o evoluţie favorabilă a bolii în timpul restricţiei calorice;
– La nivelul adipocitelor determină scăderea sintezei de acizi graşi, efect lipolitic cu
eliberarea în circulaţie a glicerolului şi creşterea sintezei oxidului nitric;
– La nivelul celulelor musculaturii striate
creşte oxidarea acizilor graşi şi determină scăderea conţinutului lipidic
intracelular, facilitând acţiunile insulinei la acest nivel;
– Are rol în hematopoieză – induce proliferarea, diferenţierea şi activarea
celulelor hematopoietice; poate induce de asemenea funcţia proliferativă şi
fagocitară a macrofagelor.
Variaţii fiziologice
ale secreţiei de leptină
Nivelurile
plasmatice ale leptinei cresc la copiii prepuberi odată cu vârsta şi cu
acumularea consecutivă de masă grasă, atingând o valoare maximă în momentul
debutului pubertar. Între 5 şi 10 ani, nivelurile serice de leptină cresc în
paralel cu IMC, dar apoi scad, în pofida creşterii greutăţii corporale.
Nivelurile
serice de leptină sunt mai mici la sexul masculin decât la cel feminin atât la
copii, cât şi la adulţi; nivelurile serice la femeile adulte sunt de două ori
mai mari decât la sexul masculin, dar scad treptat după menopauză.
Leptina,
capitalul de ţesut adipos şi profilul lipidic
O serie de
studii au demonstrat creşterea expresiei ARNm pentru gena ob la nivelul adipocitelor şi respectiv creşterea nivelurilor
plasmatice de leptină în cazul pacienţilor obezi comparativ cu cei
normoponderali, raportându-se chiar o creştere exponenţială cu IMC. Există însă
dovezi ce sugerează că relaţia dintre masa ţesutului gras şi valorile serice
ale leptinei nu este liniară: postul alimentar determină scăderea secreţiei de
leptină, dar nu dependent de reducerea masei grase; studiile privind variaţia
nivelurilor serice de leptină în timpul deprivării calorice se asociază cu un
dimorfism sexual: în timp ce Nicklas BJ şi colab. au raportat în 1997 că
leptina scade mai repede în cazul femeilor supuse dietei hipocalorice, Ramel A şi
colab. au raportat în 2010 existenţa unei corelaţii semnificative între
nivelurile serice de leptină şi variaţia ponderală doar la sexul masculin.
Relaţia
pozitivă între nivelurile serice de leptină şi indicele de masă corporală,
capitalul adipos (CA), procentul de ţesut adipos a fost demonstrată pe loturi
populaţionale variate (tabelul 1) în
populaţia polineziană, în populaţia americană, la adulţii obezi italieni. Pe un
lot de copii de vârstă şcolară thailandezi (obezi şi normoponderali), leptina
s-a corelat cu CA şi trigliceridele plasmatice la sexul feminin şi respectiv cu
CA şi masa adipoasă totală la sexul masculin (tabelul 2).
Corelaţia
între nivelurile serice de leptină şi capitalul de ţesut adipos sugerează că
majoritatea persoanelor obeze devin rezistente la acţiunea leptinei. Alte
studii au arătat că leptina are un rol mai important în evaluarea progresiei
IMC şi a acumulării viitoare de masă grasă decât în evaluarea bazală a ţesutului
adipos.
La modul
generic, nu se cunoaşte încă dacă nivelurile serice de leptină pot fi
considerate un marker al câştigului ponderal ulterior; studiile au avut
rezultate discordante la populaţia adultă (tabelul
1): dacă în cazul unui lot populaţional mauritan, în cazul femeilor la
menopauză foste obeze, al tinerilor şi al vârstnicilor americani nu s-a
demonstrat corelaţia între nivelurile  plasmatice iniţiale de leptină şi variaţia
ulterioară a IMC, o relaţie pozitivă a fost identificată într-un alt studiu
efectuat pe femeile de vârstă medie elveţiene sau într-un studiu populaţional
american care a acoperit o plajă mai mare de vârste. Relaţia dintre nivelurile
serice de leptină şi variaţia IMC în sens descrescător este de asemenea
incompletă – scăderea ponderală prin dietă hipocalorică a fost corelată cu
nivelurile serice iniţiale de leptină doar la sexul masculin la populaţia adultă,
în timp ce variaţiile leptinei nu s-au corelat cu intensitatea efortului fizic
pe un lot de copii şi adolescenţi obezi supuşi scăderii ponderale prin program
de efort fizic controlat.
plasmatice iniţiale de leptină şi variaţia
ulterioară a IMC, o relaţie pozitivă a fost identificată într-un alt studiu
efectuat pe femeile de vârstă medie elveţiene sau într-un studiu populaţional
american care a acoperit o plajă mai mare de vârste. Relaţia dintre nivelurile
serice de leptină şi variaţia IMC în sens descrescător este de asemenea
incompletă – scăderea ponderală prin dietă hipocalorică a fost corelată cu
nivelurile serice iniţiale de leptină doar la sexul masculin la populaţia adultă,
în timp ce variaţiile leptinei nu s-au corelat cu intensitatea efortului fizic
pe un lot de copii şi adolescenţi obezi supuşi scăderii ponderale prin program
de efort fizic controlat.
Reglarea
greutăţii corporale, a apetitului şi consumului energetic este chiar mai greu
de estimat la copii comparativ cu adulţii, deoarece la grupele mici de vârstă o
mare parte a energiei este utilizată pentru creştere şi dezvoltare, rolul
leptinei în această fază dinamică a reglării greutăţii corporale fiind
incomplet cunoscut.
Totuşi, în
cazul copiilor cu risc de dezvoltare a obezităţii la vârstă adultă, nivelurile
iniţiale de leptină au fost de asemenea un factor pozitiv şi semnificativ de
prognostic pentru creşterea ponderală şi pentru acumularea de ţesut adipos.
La nivelul
adipocitelor (unde s-au identificat receptori leptinici), studiile in vitro au arătat că leptina scade
expresia genelor care controlează enzimele implicate în sinteza acizilor graşi
– sintetaza acizilor graşi (FAS) şi acetil-CoA carboxilaza şi creşte expresia
genelor care controlează acil-CoA oxidaza, carnitin-palmitoil transferaza 1 şi
proteina de decuplare 2. Efectele leptinei asupra capitalului lipidic sunt
duale – administrarea de leptină pe termen scurt determină lipoliză, în timp ce
administrarea îndelungată determină scăderea lipolizei.
În mod acut,
leptina determină lipoliză prin hidroliza triacilglicerolului prin triglicerid
lipaza adipocitară, lipaza hormon-sensibilă şi lipaza monogliceridelor; acizii
graşi se reesterifică intraadipocitar, în timp ce glicerolul se eliberează în
circulaţie.
Reesterificarea
acizilor graşi intraadipocitară necesită prezenţa glicerol-3-fosfat, acesta
rezultând din lactat, piruvat şi alţi aminoacizi prin gliceroneogeneză; sinteza
enzimei-cheie a acestui proces, fosfo-enol-piruvat-carboxikinaza (PEPCK-C) este
stimulată la nivel de transcripţie de receptorul PPARg şi implicit de liganzii
săi – tiazolidindionele – şi pare a fi inhibată de infuzia cronică de leptină
în hipotalamusul mediobazal. Administrarea cronică de leptină induce
experimental la şoareci scăderea expresiei PEPCK-C şi a gliceroneogenezei, ceea
ce se traduce în scăderea stocării energetice prin esterificarea acizilor graşi
concomitent cu scăderea eliberării de glicerol şi în consecinţă scăderea
trigliceridelor plasmatice.
Conceptul de rezistenţă
la leptină în obezitate
Variaţia
paralelă a nivelurilor serice de leptină cu capitalul adipos a condus la
ipoteza rezistenţei la leptină în cazul persoanelor obeze, un concept asemănător
rezistenţei la insulină, care explică de asemenea şi consecinţele metabolice
ale hiperleptinemiei asociate excesului ponderal.
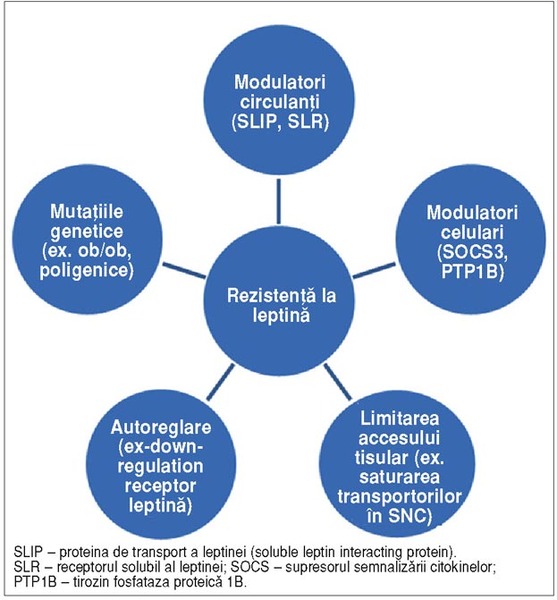
Mecanismele
leptino-rezistenţei sunt variabile (fig.
5): genetice (cauzele de obezitate monogenică prin mutaţii ale genei ob); scăderea transportorilor leptinei
la nivelul hipotalamusului (care sunt influenţaţi negativ de concentraţiile
serice mari de trigliceride), principalul său sediu de acţiune;
internalizarea/scăderea expresiei receptorilor ObR; un mecanism alternativ ar
fi autoinhibarea receptorială prin semnalizarea intracelulară îndeosebi pe calea
SOCS3 sau a PTP1B; legarea leptinei plasmatice de proteinele specifice de
legare (SLIP1-5, fracţiunea solubilă a receptorului leptinic).
Odată cu
dezvoltarea conceptului de leptinorezistenţă în cazul persoanelor obeze, a
evoluat în paralel şi ideea rezistenţei selective, doar a anumitor ţesuturi la
acţiunea leptinei; mecanismul propus este cel al inhibitorilor celulari (de tip
SOCS3), care acţionează doar în anumite ţesuturi, iar consecinţele sunt de
tipul apariţiei hipertensiunii arteriale în relaţie cu nivelurile plasmatice de
leptină atât la persoanele normoponderale, cât şi la cele obeze.
Leptina,
insulinorezistenţa şi riscul metabolic
În ceea ce
priveşte relaţia dintre leptină şi insulină, rezultatele nu sunt încă tranşante:
dacă în studiile in vitro pe
adipocite de şoareci insulina a determinat creşterea secreţiei de leptină, la
om insulina a reuşit să determine un efect similar doar după administrarea unor
doze suprafiziologice pe perioade lungi de timp.
Efectele
leptinei asupra secreţiei de insulină sunt de asemenea contradictorii, în
majoritatea studiilor descriindu-se totuşi un efect de tip inhibitor: leptina
pare să scadă secreţia pancreatică de insulină, acţionând în mod direct pe
receptorii situaţi la nivelul celulelor beta pancreatice; la nivelul altor ţesuturi
care intervin în metabolismul glucidic, leptina are acţiune de tip
insulinosensibilizantă: în ţesutul muscular creşte preluarea şi oxidarea
glucozei, iar la nivel hepatic scade gluconeogeneza; în ambele ţesuturi scade
acumularea de trigliceride, ceea ce conduce suplimentar la facilitarea acţiunii
insulinei.
În mod
aparent paradoxal însă, la pacienţii obezi, hiperleptinemia se asociază cu
insulinorezistenţa, şi aceasta datorită rezistenţei la leptină caracteristice
persoanelor obeze.
Aceasta
explică de ce în studiile clinice (tabelul
1), nivelurile serice de leptină s-au corelat cu valorile à jeun ale insulinemiei şi s-a mai
descris de asemenea o corelaţie între hiperleptinemie şi insulinorezistenţă
independent de valoarea IMC, atât pe grupuri mici de studiu, cât şi pe loturi
populaţionale mari. La pacienţii non-leptinorezistenţi, administrarea
experimentală de leptină a ameliorat insulinosensibilitatea: leptina a îmbunătăţit
profilul glicemic la copiii şi adulţii cu deficit congenital de leptină chiar
înainte de obţinerea unui IMC normal.
Acelaşi
mecanism al leptinorezistenţei pare să explice şi implicarea leptinei în
sindromul metabolic asociat excesului ponderal. Un studiu retrospectiv efectuat
pe un lot de 999 de adulţi taiwanezi a evidenţiat că valorile serice ale
leptinei sunt corelate nu doar cu valoarea insulinemiei bazale, ci şi cu
nivelurile serice de trigliceride şi cu prezenţa sindromului metabolic în
definiţia clasică.
Tot în
populaţia taiwaneză (tabelul 2), dar
de data aceasta în cea pediatrică, s-a arătat că leptina este în mod pozitiv şi
semnificativ asociată cu insulinorezistenţa cuantificată în mai multe moduri
(ca scor HOMA index sau ca scor de însumare a rezistenţei la insulină) şi că
asocierea se menţine indiferent de IMC sau de ceilalţi factori de risc.
Leptina
şi riscul cardiovascular
Legătura dintre leptină şi hipertensiunea
arterială. Studiile
clinice au arătat existenţa unei legături între nivelurile serice de leptină şi
valoarea tensiunii arteriale atât la pacienţii normotensivi, cât şi la cei
hipertensivi; femeile obeze hipertensive au în mod particular niveluri mai mari
de leptină.
Deşi
teoretic excesul ponderal se asociază cu valori crescute ale leptinei, dar şi
cu rezistenţă la acţiunea sa, apariţia HTA poate fi totuşi consecinţa efectelor
leptinei printr-o rezistenţă selectivă la leptină – în timp ce anumite ţesuturi
sunt rezistente la acţiunea leptinei, hipertonia simpatică se menţine;
mecanismul molecular propus este că autoinhibiţia receptorului ObRb al leptinei
prin sinteza SOCS3 este mai pregnantă doar în anumite ţesuturi.
În
acelaşi sens, leptina determină în mod acut eliberarea de NO şi vasodilataţie
mediată de endoteliu; administrarea cronică de leptină determină însă
experimental scăderea vasodilataţiei mediate de endoteliu, efect datorat
aceleiaşi rezistenţe la leptină şi acumulării de specii reactive de oxigen,
care scad eliberarea de NO. La copii, studiile populaţionale privind relaţia
dintre nivelurile serice de leptină şi valorile crescute ale TA sunt
discordante.
Efectul protrombotic al leptinei. Leptina are
efect proagregant prin mecanisme multiple: determină fosforilarea reziduurilor
de tirozină de la nivelul mai multor proteine trombocitare, determină activarea
fosfolipazei C, proteinkinazei C şi activarea canalelor de calciu; studiile in vivo au confirmat rolul protrombotic
al leptinei – şoarecii ob/ob formează
greu trombus după afectarea peretelui vascular şi defectul se remediază după
administrarea de leptină. Efectele
proagregante ale leptinei par să devină manifeste doar la concentraţii mari –
situaţie întâlnită doar la persoanele obeze, ceea ce oferă o nouă interpretare
a riscului cardiovascular la persoanele cu exces ponderal.
Un mecanism
complementar care ar putea conduce la riscul crescut de tromboză este
reprezentat de efectul procoagulant al leptinei – nivelurile sale serice s-au
corelat pozitiv cu secreţia de PAI-1 (inhibitor al activatorului
plasminogenului de tip 1), de fibrinogen şi de factor von Willebrand, de factor
VIIa şi negativ cu secreţia de activator al plasminogenului şi de proteină C.
Efectul proaterogen şi proinflamator al
leptinei. Leptina
are acţiune proaterogenă intrinsecă, mecanismele fiind multiple: determină
disfuncţie endotelială, stimulează reacţia inflamatorie şi stresul oxidativ,
determină migrarea, hipertrofia şi proliferarea celulelor musculare netede şi
agregarea plachetară.
Dovezile
funcţiei proaterogene ale leptinei sunt de ordin direct şi indirect: şoarecii ob/ob sunt rezistenţi la aterotomboză şi
la hiperplazia neointimală determinate de agresiunea peretelui vascular; s-a
descris prezenţa receptorilor leptinici la nivelul leziunilor aterosclerotice,
dar şi în celulele implicate în cascada evenimentelor inflamatorii
proaterogenice (limfomonocite şi macrofage).
Considerând
ateroscleroza o consecinţă a afectării de tip inflamator a peretelui vascular,
se demască alte roluri directe ale leptinei în etiopatogenia sa: stimulează
producerea de limfocite TH1 cu rol proinflamator, determină recrutarea intimală
a monocitelor, migrarea macrofagelor din vase în ţesutul adipos şi formarea de
macrofage spumoase, secreţia de citokine aterogene proinflamatorii (TNFa,
proteina C reactivă); structura sa de tip citokinic, care acţionează asupra
receptorului aparţinând familiei de receptori citokinici de tip I explică
efectele sale de tip inflamator în cazul persoanelor nonobeze.
Studiile
clinice (tabelul 1) au arătat că
există o legătură între nivelurile serice de leptină şi aterogeneza coronariană
atât în cazul persoanelor adulte din populaţia generală, cât şi în cazul
persoanelor diabetice fără boală coronariană clinic manifestă, corelaţiile
fiind independente de ceilalţi factori de risc metabolici.
Mai mult
decât atât, există un număr din ce în ce mai mare de studii care leagă nivelurile
serice de leptină de evenimentele cardiovasculare: s-a identificat o asociere
pozitivă între nivelurile plasmatice de leptină şi apariţia atât a primului
IMA, cât şi a primului AVC hemoragic, independent de factorii de risc tradiţionali;
studiile au continuat, arătând într-o manieră prospectivă că nivelurile serice
crescute de leptină prezic apariţia unui eveniment coronarian major atât în
cazul persoanelor cu aterogeneză coronariană demonstrată angiografic, cât şi în
cazul celor care au avut deja infarct miocardic sau angor instabil; într-un alt
studiu de tip caz-control care a cuprins peste 1.000 de pacienţi, Wallace şi
colab. au demonstrat că nivelurile plasmatice de leptină pot prezice
evenimentele cardiovasculare acute (IMA; necesitatea revascularizării
coronariene, deces) independent de IMC, glicemie, nivelul lipidelor plasmatice
sau proteina C reactivă.
Pe de altă
parte, o serie de alte studii clinice cuprinzând persoane sănătoase sau pacienţi
cu risc cardiovascular au indicat fie o asociere modestă a nivelurilor serice
de leptină cu riscul coronarian (şi aceasta dependentă de alţi FR), fie lipsa
acestei asocieri. Această discordanţă se explică pe de o parte prin statusul de
leptinorezistenţă asociat excesului ponderal, pe de altă parte prin ipoteza
recentă a unei acţiuni auto-/paracrine a leptinei – expresia sa crescând la
nivelul plăcilor de aterom la persoanele cu un eveniment vascular major.
Leptina, ca şi
adiponectina, nu pare să influenţeze/să fie corelată cu stadiile incipiente ale
aterogenezei: deşi cercetate, nu s-au descris corelaţii semnificative ale
leptinei cu markerii ultrasonografici ai aterogenezei în cazul femeilor obeze
nondislipidemice, al bărbaţilor vârstnici într-un studiu populaţional olandez
sau al copiilor obezi ori cu DZ tip I comparativ cu copiii sănătoşi.
 –
Determină activare tiroidiană prin
mecanism central: scăderea producţiei de leptină este însoţită experimental de
scăderea producţiei de TRH hipotalamic, iar mutaţiile leptinei/ale receptorului
său determină hipotiroidism central, care se ameliorează prin administrarea de
leptină;
–
Determină activare tiroidiană prin
mecanism central: scăderea producţiei de leptină este însoţită experimental de
scăderea producţiei de TRH hipotalamic, iar mutaţiile leptinei/ale receptorului
său determină hipotiroidism central, care se ameliorează prin administrarea de
leptină; plasmatice iniţiale de leptină şi variaţia
ulterioară a IMC, o relaţie pozitivă a fost identificată într-un alt studiu
efectuat pe femeile de vârstă medie elveţiene sau într-un studiu populaţional
american care a acoperit o plajă mai mare de vârste. Relaţia dintre nivelurile
serice de leptină şi variaţia IMC în sens descrescător este de asemenea
incompletă – scăderea ponderală prin dietă hipocalorică a fost corelată cu
nivelurile serice iniţiale de leptină doar la sexul masculin la populaţia adultă,
în timp ce variaţiile leptinei nu s-au corelat cu intensitatea efortului fizic
pe un lot de copii şi adolescenţi obezi supuşi scăderii ponderale prin program
de efort fizic controlat.
plasmatice iniţiale de leptină şi variaţia
ulterioară a IMC, o relaţie pozitivă a fost identificată într-un alt studiu
efectuat pe femeile de vârstă medie elveţiene sau într-un studiu populaţional
american care a acoperit o plajă mai mare de vârste. Relaţia dintre nivelurile
serice de leptină şi variaţia IMC în sens descrescător este de asemenea
incompletă – scăderea ponderală prin dietă hipocalorică a fost corelată cu
nivelurile serice iniţiale de leptină doar la sexul masculin la populaţia adultă,
în timp ce variaţiile leptinei nu s-au corelat cu intensitatea efortului fizic
pe un lot de copii şi adolescenţi obezi supuşi scăderii ponderale prin program
de efort fizic controlat.