Sub
denumirea de tulburări cognitive uşoare
se înţelege astăzi un echivalent al sindromului consacrat în neuroştiinţe ca mild
cognitive impairment (MCI), concept dezvoltat la începutul anilor ’90
datorită lui Ronald C. Petersen, care l-a definit drept o asociere a unei
pierderi de memorie observate de anturaj, cu alterarea obiectivă a memoriei, fără
modificări asupra activităţilor vieţii cotidiene. Acest concept, care a definit
mai mult un stadiu evolutiv decât o patologie în întregimea sa, s-a extins în
zone cognitive diferite etiologic. În momentul de faţă putem vorbi de un
concept pentru un stadiu evolutiv al mai multor maladii. Tulburările cognitive
uşoare pot fi atribuite diferitelor patologii: boala Alzheimer, în principal, şi
alte afecţiuni neurodegenerative, neurovasculare şi psihiatrice. Dezvoltarea
conceptului de MCI a permis accentuarea eforturilor ştiinţifice asupra celor
mai uşoare stadii ale bolii Alzheimer şi chiar în maladii asociate. Studii
recente arată că aproape 26% din pacienţii suferind de Parkinson vor prezenta
criteriile diagnostice de MCI, cu deficit mnezic, alterarea performanţelor
vizual-spaţiale, a funcţiilor executive şi a capacităţilor atenţionale.
Conceptul
de vascular
cognitive impairment se defineşte printr-o alterare cognitivă în raport
cu leziunile vasculare foarte heterogene cum sunt lacunele, leucoaraioza şi
chiar accidentele vasculare cu localizare strategică, nealterându-se activităţile
vieţii cotidiene. Acest concept prezintă un interes particular pentru
stabilirea dificultăţilor cognitive ale pacienţilor cu encefalopatie vasculară
fără demenţă, dar prezentând o tulburare cognitivă uşoară de importanţă majoră în
prevenţia factorilor de risc cardiovasculari şi favorizează în mod cert prevenţia
demenţei vasculare şi chiar expresia clinică din boala Alzheimer cu componente
cerebrovasculare. Recent, s-a demonstrat că 40% din subiecţii cu risc genetic
de boală Huntington reunesc criteriile de diagnostic ale MCI, mai curând de tip
non-amnezic, marcate de o încetinire a vitezei de prelucrare a informaţiilor şi
o degradare a funcţiilor executive. Acest exemplu ilustrează interesul asupra
conceptului de MCI în ansamblul bolilor care induc o alterare cognitivă
progresivă, în scopul înţelegerii mai corecte a stadiilor precoce şi a
factorilor predictivi de conversie către handicapul cognitiv mai sever şi de a
optimiza modalităţile de management începând cu primele semne care anunţă
această conversie, înainte de a avea în vedere tratamente etiopatogenice, care
nu pot fi în mod real eficace decât în stadiile precoce.
Preocuparea actuală asupra stadiilor precoce din boala
Alzheimer
Popularitatea conceptului de MCI s-a
dezvoltat considerabil începând cu anii 2000, atunci când 90% din neurologii
americani au utilizat în consultaţii acest concept. Termenul a fost întărit
odată cu observarea atentă a pacienţilor înaintea stadiului de demenţă, existând
posibilitatea luării unor măsuri non-medicamentoase cum ar fi sprijinul la
domiciliu, urmărirea clinică, prevenţia secundară, în special cu privire la
factorii de risc cardiovasculari. Medicii americani semnalează că atunci când
se pune diagnosticul de MCI există practica recomandării unor măsuri
igieno-dietetice, exerciţii fizice şi stimulări cognitive, informându-se
pacientul asupra riscului de demenţă. Pentru aceşti specialişti, conceptul de
MCI este important în organizarea măsurilor de viitor cu privire la pacient şi
ajutoare financiare, dar o parte din medici regretă existenţa unei dificultăţi
de diagnostic după criteriile actuale, subliniind faptul că va fi mai util
uneori să se evoce o boală Alzheimer precoce. Se poate observa că acest concept
este vag: revenirea la un statut cognitiv normal este destul de frecventă. Dar
definiţia MCI permite, de asemenea, confirmarea unor tulburări ale pacientului,
fără a se anunţa prea devreme diagnosticul unei patologii incurabile. Acţiunile
medico-sociale realizate în acest stadiu de MCI sunt determinante, căci, dacă
putem întârzia cu cinci ani stadiul demenţial în boala Alzheimer, impactul
medical şi economic al bolii va fi redus la jumătate, aşa cum arăta Cummings, în
2007.
regretă existenţa unei dificultăţi
de diagnostic după criteriile actuale, subliniind faptul că va fi mai util
uneori să se evoce o boală Alzheimer precoce. Se poate observa că acest concept
este vag: revenirea la un statut cognitiv normal este destul de frecventă. Dar
definiţia MCI permite, de asemenea, confirmarea unor tulburări ale pacientului,
fără a se anunţa prea devreme diagnosticul unei patologii incurabile. Acţiunile
medico-sociale realizate în acest stadiu de MCI sunt determinante, căci, dacă
putem întârzia cu cinci ani stadiul demenţial în boala Alzheimer, impactul
medical şi economic al bolii va fi redus la jumătate, aşa cum arăta Cummings, în
2007.
Limitele
conceptului de MCI
Limitele
conceptului de MCI au apărut atunci când evoluţia pacienţilor afectaţi a fost
precizată prin studii de cohortă. În fapt, deşi 10–15% din pacienţi evoluează
anual către stadiul demenţial al bolii Alzheimer, conceptul definit de Petersen
nu permite anticiparea mai precisă a acestui risc de conversie, chiar dacă
boala Alzheimer este în mod particular legată de MCI de tip amnezic (dar
compatibil cu MCI din alte domenii şi chiar MCI „nespecific“). Aceste subtipuri
de MCI pot fi în mod cu totul special întâlnite în demenţa fronto-temporală,
demenţa cu corpi Lewy sau demenţa vasculară. Conceptul de MCI nu integrează
calitatea tulburărilor mnezice (codare, stocare şi consolidare, recuperare),
datele de imagistică encefalică şi nici markerii biologici.
Astfel,
utilizarea sa în studii terapeutice în stadiul precoce al bolii Alzheimer a
condus la un eşec, foarte probabil datorită heterogenităţii patologiilor
subiacente. Dacă inhibitorii de acetilcolinesterază nu şi-au putut demonstra
eficacitatea într-un grup de pacienţi recrutaţi după criteriile de diagnostic
MCI, nu putem avea în vedere nici testarea grupului heterogen al moleculelor
care vizează mecanismele intime ale bolii Alzheimer – în special amiloidul şi
proteina tau. Pentru moleculele cu
potenţial de modificare a cursului bolii, diagnosticul de boală Alzheimer este
indispensabil. Apare deci necesitatea de a distinge problema stadiilor
evolutive (MCI şi demenţă) de alte patologii subiacente.
Boala Alzheimer: un continuum de leziuni şi stadii
clinice
Urmărirea
îndelungată a unor studii a permis evidenţierea unui declin cognitiv care
precede cu circa zece ani boala Alzheimer evidentă clinic, în particular
testele explorând memoria semantică. Timp de mai mulţi ani anterior expresiei
clinice, se poate detecta o afectare cognitivă globală, pierderi de memorie şi
simptome depresive (aproximativ cu şapte ani înainte de diagnostic), apoi
degradarea funcţională survine cu cinci ani, în medie, înainte de diagnostic.
Acest tip de abordare pune accentul asupra
duratei fazei preclinice din boala Alzheimer, fază în timpul căreia
tratamentele etiopatogenice ar trebui să fie cele mai eficace. Literatura
ultimilor ani a deschis o dezbatere în jurul diagnosticului predemenţial.
Conceptul de boală Alzheimer „prodromală“ a permis reunirea criteriilor
diagnostice, pentru cercetare. Aceste criterii se bazează în principal pe
dezvoltarea unui sindrom amnezic progresiv de tip hipocampic asociat la unul
din biomarkerii care sugerează un proces degenerativ de tip Alzheimer, în
particular atrofia hipocampică evaluată prin IRM, diminuarea amiloidului β şi
creşterea componentei tau în lichidul
cefalorahidian, imagistică metabolică (tomografie prin emisie de pozitroni –
PET – cu trasor amiloid sau trasor glucozat, tomografie cu emisie monofotonică
evaluând debitele sanguine cerebrale).
Iniţial
dedicate selecţiei pacienţilor pentru cercetare, aceste criterii au fost recent
adaptate clinicii, cu dezvoltarea conceptelor bolii Alzheimer presimptomatice
(a se lua în consideraţie pacienţii cu risc de mutaţie genetică), predemenţiale
şi demenţiale (tabelul 1). Anumite
teste neuropsihologice permit definirea unui profil amnezic hipocampic şi
predicţia (cu o probabilitate importantă) a conversiei din stadiul MCI la
stadiul demenţial de boală Alzheimer. Totuşi, acest tip de marker
neuropsihologic nu poate fi luat în seamă  decât atunci când pacientul sau
anturajul său semnalează o dificultate de memorie, deoarece valoarea sa
diagnostică predictivă este semnificativă în populaţia generală. De altfel,
aportul biomarkerilor care explorează procesele lezionale precoce asociate
bolii Alzheimer confirmă că această boală poate să debuteze printr-un MCI în
unul sau mai multe alte domenii patologice, şi nu exclusiv printr-un „MCI
amnezic“.
decât atunci când pacientul sau
anturajul său semnalează o dificultate de memorie, deoarece valoarea sa
diagnostică predictivă este semnificativă în populaţia generală. De altfel,
aportul biomarkerilor care explorează procesele lezionale precoce asociate
bolii Alzheimer confirmă că această boală poate să debuteze printr-un MCI în
unul sau mai multe alte domenii patologice, şi nu exclusiv printr-un „MCI
amnezic“.
Diagnosticul
de boală de Alzheimer prodromală nu poate fi pus decât dacă simptomele clinice
sunt evocatoare şi dacă biomarkerii sunt concordanţi. Dacă biomarkerii sunt
pozitivi dar clinica nu este evocatoare, nu este sigur că simptomele au o legătură
cu leziunile de tip Alzheimer: ele pot fi revelatoare pentru leziuni care se
cumulează dar care nu au încă expresie clinică. Dacă clinica este evocatoare şi
biomarkerii sunt negativi, nu este rezonabil de a folosi diagnosticul de boală Alzheimer
(bA).
Boala începe cu mult timp înainte de demenţă
Biomarkerii imagistici sau biologici prezintă
o sensibilitate şi o specificitate care depăşesc 85–90%, dacă sunt evaluaţi în
raport cu neuropatologia. Ei au permis reflexia diagnostică precoce din punct
de vedere etiologic. Coroborarea unei creşteri a proteinei tau / fosfo-tau cu diminuarea
amiloidului β semnalează, in vivo,
o acumulare de leziuni caracteristice bolii Alzheimer, riscul conversiei din
stadiul de MCI către stadiul demenţial la cinci ani putând fi multiplicat de 18
ori, după cum arată lucrările lui Hansson şi colab.
Variaţiiletau şi A β în LCR intervin foarte precoce în cursul evolutiv al bolii, în
timp ce cascada amiloidă începe cu mult înaintea semnelor clinice, conform observaţiilor
lui Jack şi colab. Variaţiile proteinei tau
intervin apoi în timp ce degenerescenţa neurofibrilară se extinde.
Imagistica
metabolică, în particular PET-CT utilizând trasori amiloid, a arătat o foarte
mare sensibilitate în stadiul de MCI al bolii Alzheimer (fig. 1).
Acest tip de abordare a permis constatarea
importanţei depozitelor de amiloid, în timp ce degradarea cognitivă este încă
extrem de modestă. Chiar subiecţii martor consideraţi sănătoşi, dar la care s-a
observat un rezultat pozitiv la PET cu trasor amiloid, prezintă un anumit risc
de a suferi de boala Alzheimer manifestă clinic în anii următori acestui examen
(Morris şi colab.).
Atunci
când markerii care explorează acumularea de amiloid β în LCR sau imagistic sunt
sensibili foarte precoce, în mod cert, în anii ce preced simptomele, măsurătorile
atrofiei cerebrale, în particular la nivelul hipocampului, ar putea fi
sensibile şi specifice, dar „în aval“, ilustrând consecinţele neuronale ale
cascadei acumulării de amiloid şi ale degenerescenţei neurofibrilare. În acelaşi
mod apar variaţiile metabolice ale consumului de glucoză în PET. Aceste variaţii
metabolice ilustrează consecinţele cerebrale funcţionale care intervin înaintea
degradării cognitiv-comportamentale şi funcţionale care semnalează stadiul de
demenţă. Schematic, variaţiile biomarkerilor şi ale semnele clinice în cursul
bolii Alzheimer, din stadiul preclinic până la demenţă, sunt ilustrate în fig. 2.
Schematic, variaţiile biomarkerilor şi ale semnele clinice în cursul
bolii Alzheimer, din stadiul preclinic până la demenţă, sunt ilustrate în fig. 2.
Diagnosticul precoce vs.
diagnosticul conversiei iminente către demenţă. Aplicaţii în studii terapeutice
Combinarea markerilor clinici, biologici şi
radiologici este importantă pentru a putea prevedea conversia din stadiul MCI către
demenţă (Ewersn şi colab.). Markerii cei mai precoce ai leziunii, cum este
prezenţa amiloidului β în LCR, vor fi mai puţin utili în anticiparea conversiei
către demenţă pe termen scurt şi mediu, dar vor permite mai degrabă
prognosticul severităţii declinului cognitiv pe termen lung. Alţi markeri vor
fi mai sensibili pentru evaluarea riscului de conversie iminentă din stadiul de
MCI către cel demenţial. Astfel, funcţiile executive intră într-un declin rapid
imediat înaintea conversiei clinice din stadiul de MCI către stadiul demenţial.
Combinarea unei alterări a amintirilor
verbale cu modificarea PET-CT la FDG (fluorodezoxiglucoză) vor fi foarte
importante în anunţarea conversiei din stadiul de MCI către demenţa de tip
Alzheimer în doi ani (Landau şi colab.). O serie de alţi parametrii
neuroradiologici, în special IRM, vor fi importanţi în evaluarea riscului de
conversie pe termen mediu din stadiul de MCI către demenţă, în special
hipersemnalele substanţei albe în regiunile fronto-parietale şi subcorticale de
origine vasculară asociate unui declin al funcţiilor executive (Jacobs şi
colab.).
Astfel, se cuvine să urmărim studierea
locului pe care îl ocupă biomarkerii în evoluţia bolii Alzheimer, începând cu
stadiul presimptomatic de MCI şi mai ales evaluarea valorilor predictive cu
privire la conversia rapidă sau medie. O cercetare multimodală, clinică,
neuropsihologică şi neuroradiologică trebuie să fie realizată în cadrul acestei
abordări importante pentru studiile terapeutice. Într-adevăr, utilizarea
biomarkerilor care nu sunt pertinenţi decât atunci când evoluţia către un
stadiu demenţial este încă îndepărtată ar putea pune probleme etice cu privire
la speranţa de viaţă a persoanelor de vârstă înaintată. Pozitivitatea
biomarkerilor care ţintesc amiloidul β nu vor permite predicţia în această
populaţie a conversiei clinice către handicapul cognitiv şi comportamental într-un
interval rezonabil.
Este deci necesar să se aprecieze calitativ
markerii care semnalează o conversie rapidă, cum ar fi, de exemplu, domeniul
neuropsihologic, variaţiile proteinei tau,
consumul de glucoză în imagistică.
Evoluţia recentă a conceptelor a permis
elaborarea unor criterii diagnostice internaţionale pentru MCI prin boală
Alzheimer (Albert şi colab.), în paralel cu noile criterii diagnostice ale
bolii Alzheimer (McKhann şi colab.). Aceste criterii sunt de două tipuri: de uz
clinic şi cu rol în cercetare.
Criterii
clinice: schimbarea recentă a statusului cognitiv al pacientului; alterarea
semnificativă a unuia sau mai multor domenii cognitive; absenţa modificărilor
semnificative în viaţa profesională sau domestică; absenţa demenţei. Chiar dacă
amnezia episodică este simptomul cel mai evocator pentru boala Alzheimer în
acest stadiu, este recunoscut faptul că simptomele atipice, cum sunt tulburările
vizuale, tulburările de comunicare verbală şi chiar cele comportamentale pot fi
primele simptome de boală. Pentru a evoca o boală Alzheimer în stadiul de MCI,
este necesar să excludem – pe cât posibil – encefalopatia vasculară, demenţa
cu corpi Lewy şi degenerescenţa lobară fronto-temporală. Coexistenţa mai multor
patologii trebuie avută în vedere, în special la persoanele în vârstă.
Criterii
pentru cercetare: studiile integrează biomarkerii ce ilustrează depozitele
de amiloid β (Aβ1–42) în LCR şi PET cu
trasor amiloid, precum şi markerii de disfuncţie sau de liză neuronală (tau şi fosfo-tau) în LCR, atrofia medio-temporală în PET cu FDG, SPECT.
Diferenţele gradelor de probabilitate
diagnostică a unui MCI în raport cu boala Alzheimer sunt propuse după coerenţa
datelor clinice şi a biomarkerilor (tabelul
2).
Concluzii
Conceptul
de MCI poate figura în curând în DSM-V. Dacă el apare foarte util pentru
integrarea pacientului în sistemul de îngrijiri cât mai curând posibil, apare
esenţială acţiunea energică, într-un demers diagnostic optimal, pentru a
stabili un diagnostic etiologic precis. Dar va fi, în mod cert, nevoie ca
informaţiile multiple provenite din observaţia clinică şi a biomarkerilor să
fie utilizate cu precauţie înainte de a preciza şi, mai ales, anunţa
diagnosticul. Aceasta înseamnă şi indicarea unor tratamente cu totul
particulare, în condiţiile unei mai bune precizări a riscului de conversie către
stadiul demenţial, pe termen scurt, mediu şi lung.
Încercând să atrag atenţia asupra unui nou
sindrom – vascular cognitive impairment, a
fost necesară incursiunea în datele moderne cu privire la mild cognitive impairment, sindrom binecunoscut în apariţia bolii
Alzheimer.
MCI
reflectă un stadiu evolutiv al unei degradări cognitive progresive.
Acest
sindrom poate fi dat de mai multe procese lezionale neurodegenerative sau
neurovasculare.
Boala
Alzheimer poate fi diagnosticată în stadiul de MCI.
Putem accepta
existenţa conceptului de vascular
cognitive impairment şi pentru faptul – cunoscut – că, la vârste înaintate,
demenţa Alzheimer se „vascularizează“ iar demenţa vasculară se „alzheimerizează“.
Delimitarea în acest mod a tulburărilor cognitive în stroke (AVC) este posibilă
şi foarte necesară. 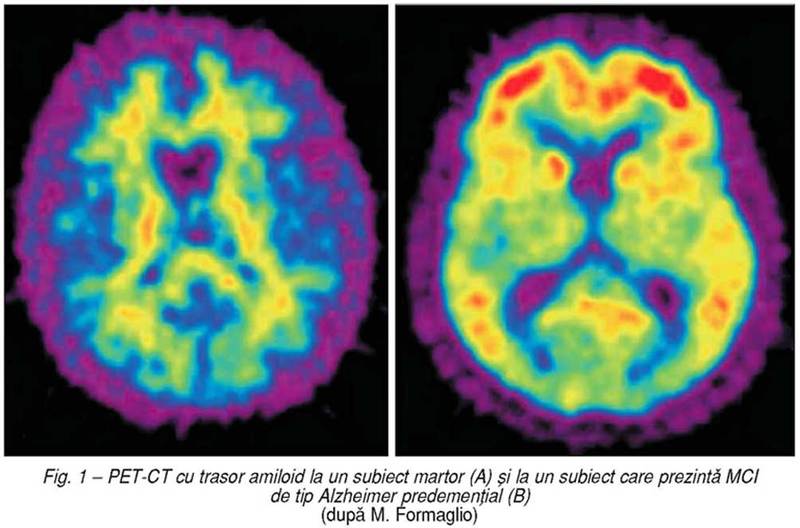
 regretă existenţa unei dificultăţi
de diagnostic după criteriile actuale, subliniind faptul că va fi mai util
uneori să se evoce o boală Alzheimer precoce. Se poate observa că acest concept
este vag: revenirea la un statut cognitiv normal este destul de frecventă. Dar
definiţia MCI permite, de asemenea, confirmarea unor tulburări ale pacientului,
fără a se anunţa prea devreme diagnosticul unei patologii incurabile. Acţiunile
medico-sociale realizate în acest stadiu de MCI sunt determinante, căci, dacă
putem întârzia cu cinci ani stadiul demenţial în boala Alzheimer, impactul
medical şi economic al bolii va fi redus la jumătate, aşa cum arăta Cummings, în
2007.
regretă existenţa unei dificultăţi
de diagnostic după criteriile actuale, subliniind faptul că va fi mai util
uneori să se evoce o boală Alzheimer precoce. Se poate observa că acest concept
este vag: revenirea la un statut cognitiv normal este destul de frecventă. Dar
definiţia MCI permite, de asemenea, confirmarea unor tulburări ale pacientului,
fără a se anunţa prea devreme diagnosticul unei patologii incurabile. Acţiunile
medico-sociale realizate în acest stadiu de MCI sunt determinante, căci, dacă
putem întârzia cu cinci ani stadiul demenţial în boala Alzheimer, impactul
medical şi economic al bolii va fi redus la jumătate, aşa cum arăta Cummings, în
2007.  decât atunci când pacientul sau
anturajul său semnalează o dificultate de memorie, deoarece valoarea sa
diagnostică predictivă este semnificativă în populaţia generală. De altfel,
aportul biomarkerilor care explorează procesele lezionale precoce asociate
bolii Alzheimer confirmă că această boală poate să debuteze printr-un MCI în
unul sau mai multe alte domenii patologice, şi nu exclusiv printr-un „MCI
amnezic“.
decât atunci când pacientul sau
anturajul său semnalează o dificultate de memorie, deoarece valoarea sa
diagnostică predictivă este semnificativă în populaţia generală. De altfel,
aportul biomarkerilor care explorează procesele lezionale precoce asociate
bolii Alzheimer confirmă că această boală poate să debuteze printr-un MCI în
unul sau mai multe alte domenii patologice, şi nu exclusiv printr-un „MCI
amnezic“. Schematic, variaţiile biomarkerilor şi ale semnele clinice în cursul
bolii Alzheimer, din stadiul preclinic până la demenţă, sunt ilustrate în fig. 2.
Schematic, variaţiile biomarkerilor şi ale semnele clinice în cursul
bolii Alzheimer, din stadiul preclinic până la demenţă, sunt ilustrate în fig. 2.