Spre
deosebire de ischemia miocardică, în care ateromul reprezintă cauza principală
sau chiar unică, în patologia ischemiei cerebrale rezultă mecanisme vasculare
variate. De la cele implicate în procesele de ocluzie arterială şi alterarea
debitului sanguin cerebral, lucrările din ultimii ani au permis o mai bună înţelegere
a diversităţii mecanismelor celulare implicate.
În
cadrul trombolizei, este important să fim atenţi la supravegherea efectelor
potenţial negative ale reperfuziei, în special asupra barierei hematoencefalice
şi capacităţilor funcţionale ale vaselor, a căror alterare ar putea contribui
la agravarea leziunilor ţesutului cerebral.
MECANISME VASCULARE
Debitul sanguin
cerebral
Debitul sanguin cerebral (DSC) este, în
medie, de 50 ml/min/100 g de ţesut cerebral, la adult. Fiziologic, acest debit
variază paralel cu starea de dilataţie sau contracţie a arterelor cerebrale.
Capacitatea de vasorelaxare sau de
vasoconstricţie a acestor artere depinde de vârstă şi de existenţa sau nu a
unor patologii precum diabetul sau hipertensiunea arterială (HTA). Ele depind,
de altfel, de numeroase mecanisme în funcţie de care se produce eliberarea de
molecule vasodilatatoare (cum este oxidul nitric – NO) sau vasoconstrictoare
(cum este endotelina) sau, încă, activarea canalelor de potasiu din celulele
musculare vasculare netede (cum este Kir 2.1, canal implicat în special în
cuplajul dintre metabolism şi DSC).
Infarctul cerebral este rezultatul diminuării,
apoi al opririi perfuziei ţesutului cerebral şi ca urmare a depăşirii capacităţii
acestor sisteme de supleanţă. La nivel individual, gravitatea expresiei clinice
a unei ocluzii arteriale va fi puternic dependentă de calitatea reţelelor
anastomotice, pe de o parte, şi de capacităţile de autoreglare ale DSC, pe de
altă parte.
Mecanismele de protecţie sunt puse în
activitate atunci când DSC scade sub 50 ml/min/100 g de ţesut cerebral. Dacă
acest debit atinge valori de ordinul a 20 ml/min/100 g de ţesut cerebral,
metabolismul celular este alterat; pot să apară simptome neurologice şi anomalii
ale traseelor EEG şi potenţialelor evocate, ca şi anomalii la imagistica prin
rezonanţă magnetică (IRM). Între 15 şi 20 ml/min/100 g de ţesut, zona de
oligemie maximală tolerată este atinsă. Se vorbeşte în acest caz de zona de penumbră ischemică. La EEG, se
notează un silenţiu electric complet, reversibil, cu condiţia ca fluxul
arterial să fie restabilit.
La IRM, datele recente din literatură sugerează
că diferenţa între anomaliile observate în secvenţele de difuzie şi cele
observate în secvenţele de perfuzie ar putea fi reprezentativă pentru această
zonă de penumbră şi constituie un marker interesant pentru candidaţii la
tromboliză. În schimb, dacă această oligemie se prelungeşte mai mult de câteva
zeci de minute, se ajunge în stadiul de necroză tisulară. Necroza apare, de
asemenea, atunci când DSC este menţinut pentru mai mult de trei minute sub 10
ml/min/100 g de ţesut cerebral. IRM de difuzie poate, în acest caz, să
delimiteze un marker precoce.
Diferite mecanisme
vasculare la originea ischemiei cerebrale
Sunt de reţinut trei mecanisme vasculare
principale: embolic arterio-arterial sau
de origine cardiacă; hemodinamic; atingerea arterelor perforante.
Mecanismul embolic este evocat mai ales de
apariţia brutală a deficitului neurologic. Poate fi vorba fie de o embolie
fibrino-plachetară dată de un trombus alb rezultat din adeziunea plachetelor la
nivelul plăcii de ateroscleroză, fie de o embolie ce provine din fragmentarea
unui trombus mural, plecând de la o placă de ateroscleroză ulcerată, de un
trombus produs într-o cavitate cardiacă sau, mai rar, prin migrarea unui
trombus venos profund, traversând foramen ovale permeabil.
Poate fi vorba, de asemenea, de o embolie de
colesterol, provenind din conţinutul ateromatos al plăcii, migrând în circulaţie
cu ocazia rupturii acesteia, de o embolie calcară, pornind de la o îngustare
aortică calcificată sau de un embol de material septic, în cadrul unei
endocardite infecţioase.
În fine, trebuie semnalată posibilitatea
unei embolii arteriale de celule neoplazice, plecând de la un neoplasm sau o
tumoră intracardiacă, cum este mixomul.
În imagistică, este obişnuit să se
considere că infarctele cerebrale consecutive unui mecanism embolic ating mai
curând teritoriul unei artere mari intracraniene (silviană, cerebrală anterioară,
cerebrală posterioară), dar aceasta nu are un caracter exclusiv. În fapt,
diagnosticul de mecanism, în afara imagisticii, se bazează pe argumente clinice
şi pe rezultatele explorărilor vasculare.
Accidentul hemodinamic este, la rândul său,
evocat de fluctuaţiile simptomatologiei neurologice deficitare, mai ales dacă
această fluctuaţie este concomitentă schimbărilor de poziţie (ridicare bruscă,
trecerea într-o anumită poziţie) sau dacă este asociată cu o scădere a
presiunii arteriale. Acest tip de mecanism este uşor de observat în cazul
stenozelor severe ale vaselor mari cu destinaţie cerebrală. Este, de altfel,
posibil ca acest mecanism să fie pus în evidenţă în infarctul legat de o
hemoabatere, cum este „furtul
subclavicular“ sau în condiţiile unui şoc
cardiogenic. În afară de infarctele cu sediul în teritoriul vaselor mari,
acest tip de mecanism este mai curând responsabil de dezvoltarea infarctelor
joncţionale. Infarctele consecutive unui şoc cardiogen sunt, la rândul lor, mai
curând infarcte bilaterale, uneori de tip joncţional sau atingând preferenţial
nucleii cenuşii centrali.
Atingerea arterelor perforante este cel mai
adesea consecutivă unei patologii arteriale, cum este hipohialinoza, care apare
în contextul unei HTA sau al unui diabet. Patologia acestor artere mici se
traduce prin leziuni ischemice zise lacunare (infarcte cerebrale de talie mică
sau prin apariţia hemoragiilor profunde). S-ar părea că infarctele sunt
determinate de obturaţia uneia din ramurile perforante profunde. Diagnosticul
poate fi orientat de simptomatologia clinică sau de numeroase sindroame, mai
mult sau mai puţin specifice. Acestea pot fi multiple, la anumiţi pacienţi. În
acest context, apariţia unei noi leziuni este uneori un diagnostic dificil –
secvenţele IRM de difuzie ar permite facilitarea diagnosticului.
PRINCIPALELE MECANISME CELULARE ÎN ISCHEMIA CEREBRALĂ
Un proces care
evoluează în spaţiu şi timp
În prezent, nu se poate rezuma suferinţa
tisulară cerebrală indusă de ischemie prin simplele efecte directe ale privării
energetice şi de oxigen. Leziunile tisulare cerebrale din cursul ischemiei sunt
rezultatul mecanismelor complexe, care variază în timp şi spaţiu.
Centrul ischemiei este sediul unei necroze,
adesea rapidă şi secundară morţii celulare de origine citoplasmică, unde
eliberarea masivă de calciu joacă un rol important. În schimb, zona de penumbră,
unde persistă o anumită perfuzie, este sediul apoptozei, un proces de moarte
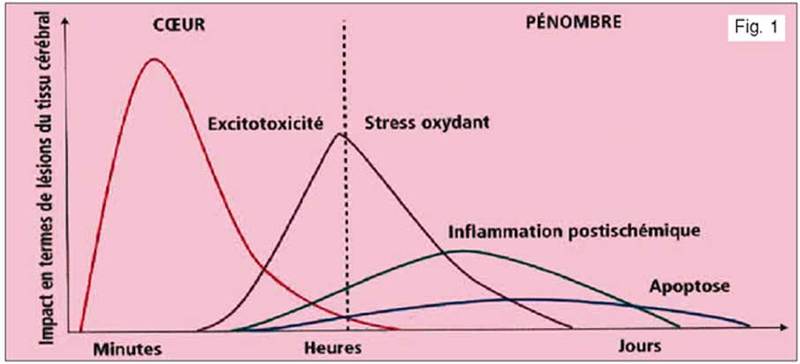
celulară programată la nivel nuclear. Maturarea leziunilor ischemice este, de
altfel, rezultanta succesiunii proceselor distructive, care încep imediat în
decursul ischemiei, cu toate că excitotoxicitatea sau stresul oxidativ se
prelungesc uneori mai multe zile, ca şi inflamaţia postischemică (fig. 1).
Calciul şi excitotoxicitatea:
determinante iniţiale ale morţii celulare
Una din principalele şi cele mai rapide
consecinţe ale ischemiei în interiorul ţesutului cerebral este creşterea
concentraţiei intracelulare de calciu, care conduce rapid la necroză. Această
distrucţie celulară se efectuează prin intermediul activării unor sisteme
enzimatice (proteinkinaze,  proteaze, NO-sintetaze) responsabile de inhibiţia
sintezei proteice, producţia de radicali liberi sau alterarea proteinelor
citoscheletice (fig. 2).
proteaze, NO-sintetaze) responsabile de inhibiţia
sintezei proteice, producţia de radicali liberi sau alterarea proteinelor
citoscheletice (fig. 2).
Dacă invazia calcică este declanşată de
depleţia energetică celulară şi prin anoxie, responsabilă, de altfel, de
depolarizarea anormală a celulelor, ea este întreţinută de eliberarea masivă de
acizi aminaţi excitatori, în particular de glutamat (fig. 2). Aceste evenimente succesive vor fi completate rapid, prin
intrarea în joc a altor mecanisme distructive, dar şi protectoare în raport cu
sinteza de NO.
 proteaze, NO-sintetaze) responsabile de inhibiţia
sintezei proteice, producţia de radicali liberi sau alterarea proteinelor
citoscheletice (fig. 2).
proteaze, NO-sintetaze) responsabile de inhibiţia
sintezei proteice, producţia de radicali liberi sau alterarea proteinelor
citoscheletice (fig. 2).