Amprentele
cancerului
După
cum precizam în primul articol al acestui „serial“ dedicat oncogenomicii („Viaţa medicală“ nr. 46/2012, pag. 7), numeroasele
cercetări din ultimele decenii au stabilit cu certitudine că boala canceroasă este o afecţiune genetică
complexă produsă prin acumularea în timp a
unor modificări genetice şi epigenetice,
moştenite şi/sau dobândite, în gene
multiple (oncogene, gene supresoare ale creşterii tumorale, genele
microARN). Prin aceste evenimente, o clonă
celulară capătă un set de caracteristici specifice, proliferează intens şi
formează o tumoră, care creşte necontrolat şi diseminează.
Într-un
articol de referinţă, publicat în anul 2000 de prestigioasa revistă Cell (1), Douglas Hanahan şi Robert
Weinberg au stabilit şase caracteristici distinctive („the hallmarks of cancer“) dobândite de
celulele canceroase în timpul dezvoltării multistadiale a tumorilor: 1)
semnalizarea proliferativă permanentă; 2) insensibilitatea la semnalele
antiproliferative; 3) evitarea morţii celulare programate (apoptoza); 4) potenţialul
replicativ nelimitat; 5) inducţia angiogenezei; 6) invazia tisulară şi
metastazarea. Achiziţia acestor caracteristici
definitorii ale tumorilor maligne este posibilă ca urmare a două „proprietăţi
permisive“: instabilitatea genomică a celulelor canceroase şi starea
inflamatorie a leziunilor maligne.
În
anul 2011, aceiaşi autori (2) analizează cele şase caracteristici esenţiale ale
cancerului, pe baza descoperirilor ştiinţifice realizate în ultimul deceniu, şi
concluzionează că aceste caracteristici „au rezistat la proba timpului“,
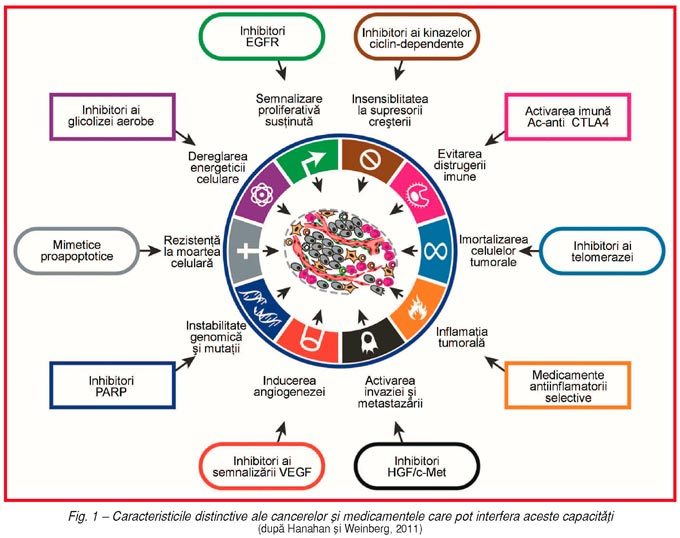
generând şi anumite soluţii terapeutice eficiente (fig. 1). Hanahan şi Weinberg adaugă alte două însuşiri distinctiveposibile, emergente, ale tumorilor:dereglarea energeticii celulare şi
evitarea distrugerii imune – implicate în patogenia multor forme de cancer,
dar care nu sunt complet validate şi valabile pentru toate tumorile; probabil
ele nu sunt necesare pentru producerea cancerului, dar „asistă“ celulele în tranziţia de la normalitate la neoplazie.
Pe baza celor două articole de referinţă, vom încerca succint să prezentăm esenţa
acestor „amprente ale cancerului“, care oferă un cadru logic şi unitar
pentru înţelegerea diversităţii deosebite a bolii canceroase, precum şi
posibilităţi eficace de tratament.
1. Celulele canceroase stimulează propria lor creştere şi
proliferare (semnalizare
proliferativă permanentă)
Una
dintre caracteristicile fundamentale ale celulelor canceroase este, probabil, capacitatea de a-şi stimula permanent
propria lor creştere şi proliferare. Pentru a înţelege această proprietate,
este util să ne amintim că celulele normale au nevoie pentru creştere şi
diviziune de semnale mitogene externe
(reprezentate în special de factori de
creştere1), produse (sub o formă difuzibilă) de alte celule (semnalizare paracrină). Aceste molecule(liganzi) se fixează pe receptori transmembranari specifici,
care, după activare, transmit semnalul – prin căi de semnalizare intracelulare ramificate – la nucleu, declanşând
diviziunea (fig. 2). Întregul proces
este reglat prin mecanisme feedback negative, care atenuează semnalizarea
proliferativă excesivă (o fac tranzitorie)
şi, dacă persistă, induc senescenţa celulară şi apoptoza (3).
Celulele
canceroase au o dependenţă redusă faţă de
stimulii proliferativi externi şi deseori nu au nevoie de o astfel de
stimulare pentru a se multiplica; prin mutaţiile unor oncogene, aceste celule dobândesc o autonomie proliferativă, producându-şi propriile lor semnale
mitogene. Strategiile majore utilizate de celulele tumorale pentru a-şi obţine
independenţa proliferativă sunt următoarele (fig.
2): • producerea de factori de creştere
proprii, la care răspund prin proliferare (semnalizare autocrină) (de exemplu, TGF-α în sarcoame) • dereglarea receptorilor factorilor de creştere,
care transduc semnalele proliferative în interiorul celulei; dereglarea implică
fie hiperexpresia receptorilor în
multe cancere (de exemplu, amplificarea receptorului HER2/neu în circa 30% din
cancerele de sân sau a EGFR în cancerul pulmonar fără celule mici), fie alterarea structurii lor, care produce
activarea receptorului şi deci semnalizarea, fără ligand (de exemplu, versiunea
trunchiată a receptorului EGF) • alterarea componentelor
căilor de semnalizare citoplasmatice, care produc un flux de semnalizare
mitogenă fără stimularea lor de către
receptori; de exemplu, calea MAP-kinazelor (mitogen-activated
protein-kinases), alcătuită din proteinele RAS→ RAF → MEK → MAPK → ERK →
FOS, joacă un rol central în circa 25% din cancerele umane (1–3).
Autonomia
proliferativă a celulelor canceroase este determinată de mutaţii activatoare
ale oncogenelor. Amplificarea oncoproteinelor
care produc independenţa proliferativă este ţinta unor medicamente eficace în
tratamentul tumorilor (fig. 2).
2. Celulele canceroase sunt rezistente la semnalele
inhibitorii ale proliferării (insensibilitatea la semnalele
antiproliferative)
Pe
lângă capacitatea de a-şi stimula intens propria creştere şi proliferare (prin
activarea oncogenelor), celulele canceroase sunt insensibile la semnalele care ar putea opri diviziunea celulară. În
ţesuturile normale acţionează multiple semnale antiproliferative, externe sau
interne, care menţin homeostazia tisulară. Semnalele inhibitorii exogene – fie
solubile (TGF-β), fie încorporate în matricea extracelulară şi suprafaţa
celulelor vecine (prin molecule de adeziune de tipul caderinelor, care determină
„inhibiţia de contact“)2 – sunt primite de receptori transmembranari cuplaţi
cu circuite intracitoplasmatice de semnalizare, care blochează diviziunea
celulară. Celulele trec din etapa G1 postmitotică în faza G0 de repaus, de unde
pot reveni în ciclul celular – atunci când condiţiile o permit – sau renunţă
definitiv la diviziune şi se diferenţiază în celule specifice (3).
Majoritatea
circuitelor antiproliferative depind de proteinele codificate de genele supresoare ale creşterii tumorale
(GST). Aceste proteine acţionează pe două căi reglatoare complementare, care au
ca element principal proteina RB („asociată retinoblastomului“) sau proteina TP53 („gardianul genomului uman“), „gatekeepers“
importanţi pentru progresia în ciclul celular mitotic. Calea RB răspunde, în special, la semnale antiproliferative exogene (de exemplu, TGF-b sau caderina E), care
produc fosforilarea proteinei RB şi sechestrarea factorului de transcripţie
E2F1, activator al expresiei genelor necesare pentru progresia ciclului celular
(G1 → S). Calea TP53 primeşte informaţii de la senzori intracelulari care depistează leziuni ale ADN sau
alterarea altor subsisteme celulare; celula trece în starea G0 de repaus iar dacă
leziunile nu pot fi reparate se declanşează apoptoza. În cancere se produc mutaţii
inactivatoare ale GST, care alterează receptorii sau proteinele căilor RB şi
TP53, determinând insensibilitatea/rezistenţa la semnalele antiproliferative
(1–3).
3. Rezistenţa la mecanismele morţii celulare programate
Capacitatea
tumorilor de a-şi spori numărul de celule
este determinată nu numai de creşterea ratei de proliferare, ci şi de rezistenţa
celulelor canceroase la mecanismele normale de moarte celulară programată (în
special apoptoza sau „sinuciderea“ celulei),
care sunt profund alterate în cancer. „Maşinăria“ apoptozei este alcătuită din senzori,
care monitorizează semnalele extra- şi intracelulare, efectori (caspazele, ce
produc proteoliza celulei) şi reglatori,proapoptotici (de exemplu, proteinele
TP53 şi BAX) sau antiapoptotici (de
exemplu, proteina BCL-2). Apoptoza este declanşată pe două căi majore: o cale extrinsecă, mediată de receptori
membranari, şi o cale intrinsecă sau
mitocondrială (3) (fig. 3). Calea
extrinsecă este iniţiată prin ataşarea unor liganzi (TNF-α, FAS) la receptori
membranari specifici, ce produce recrutarea şi activarea caspazei iniţiatoare
8, care la rândul ei va activa caspaza efectoare 3, răspunzătoare de inducţia
apoptozei. Calea intrinsecă este declanşată în special de alterări ale ADN,
care, prin activarea proteinei TP53, determină eliberarea unor factori
proapoptotici (citocromul c, SMAC3)
din mitocondrii, care activează caspazele efectoare 3 şi 9.
canceroase la mecanismele normale de moarte celulară programată (în
special apoptoza sau „sinuciderea“ celulei),
care sunt profund alterate în cancer. „Maşinăria“ apoptozei este alcătuită din senzori,
care monitorizează semnalele extra- şi intracelulare, efectori (caspazele, ce
produc proteoliza celulei) şi reglatori,proapoptotici (de exemplu, proteinele
TP53 şi BAX) sau antiapoptotici (de
exemplu, proteina BCL-2). Apoptoza este declanşată pe două căi majore: o cale extrinsecă, mediată de receptori
membranari, şi o cale intrinsecă sau
mitocondrială (3) (fig. 3). Calea
extrinsecă este iniţiată prin ataşarea unor liganzi (TNF-α, FAS) la receptori
membranari specifici, ce produce recrutarea şi activarea caspazei iniţiatoare
8, care la rândul ei va activa caspaza efectoare 3, răspunzătoare de inducţia
apoptozei. Calea intrinsecă este declanşată în special de alterări ale ADN,
care, prin activarea proteinei TP53, determină eliberarea unor factori
proapoptotici (citocromul c, SMAC3)
din mitocondrii, care activează caspazele efectoare 3 şi 9.
În
cancer, rezistenţa la apoptoză este dobândită prin strategii variate (care
blochează calea extrinsecă sau intrinsecă), dar cea mai importantă este
pierderea unor reglatori proapoptotici prin mutaţii ce implică gena
supresoare TP53 (prezente în peste
50% din tumorile umane) şi inactivarea Bax sau hiperexpresia proteinei
antiapoptotice Bcl-2 (fig. 3).
Majoritatea
metodelor actuale de chimio-, radio- şi imunoterapie au ca rezultat activarea
mecanismelor care declanşează apoptoza. De aceea, o mai bună înţelegere a
mecanismelor normale şi de rezistenţă în faţa apoptozei va avea fără îndoială
un rol major pentru dezvoltarea unor noi strategii de tratament în cancer. În
acest context, precizăm că există şi alte
mecanisme de moarte celulară programată: autofagia şi necroptoza (3). Autofagia suprimă tumorigeneza în stadiile
precoce, dar favorizează progresia tumorală în stadiile avansate. Necroza tumorală produsă de terapiile
antitumorale clasice – deşi este la prima vedere un fenomen benefic, ce
contrabalansează hiperproliferarea celulelor tumorale – poate fi în ultimă
instanţă un fenomen care facilitează evoluţia tumorală, deoarece celulele
necrotice eliberează factori proinflamatori, ce stimulează proliferarea
celulelor viabile vecine (3).
4. Imortalizarea celulelor tumorale (potenţial replicativ
nelimitat)
Cele
trei caracteristici esenţiale ale celulelor tumorale – autonomia semnalelor de creştere, insensibilitatea la semnalele
antiproliferative şi rezistenţa la apoptoză – produc o dereglare a proliferării,
care însă nu este suficientă pentru expansiunea unei clone celulare spre o
tumoră macroscopică, deoarece celulele umane au un program care limitează
natural multiplicarea lor, prin două „bariere antiproliferative“: senescenţa (o
stare viabilă, dar neproliferativă) şi apoptoza. Totuşi, într-un anumit moment
din cursul evoluţiei progresive, clona canceroasă dobândeşte o capacitate de replicare şi multiplicare fără limite,
numită imortalizare.
Celulele
normale ale organismului pot suferi un număr limitat de diviziuni (limita
Hayflick) datorită scurtării progresive a
telomerelor („călcâiul lui Achile al ADN“), implicate în protejarea
capetelor cromozomilor; această scurtare este consecinţa caracterului asimetric al replicării celor două catene ale ADN. La un moment dat,
scurtarea telomerelor duce la pierderea capacităţii protectoare a capetelor
cromozomilor, putându-se genera o instabilitate
genomică (prin fuziunea „cap la cap“
a cromozomilor), oprirea proliferării şi apoptoză. Deci lungimea ADN telomeric
reprezintă un veritabil „ceas molecular“,
ce determină numărul de diviziuni pe care celulele le mai au de efectuat.
În
aproximativ 90% din cancerele umane se produce (prin mutaţiile oncogenei MYC) o reactivare a telomerazei, o ADN polimerază ce repară eroziunile
telomerelor, menţine lungimea lor şi determină un potenţial replicativ
nelimitat sau imortalizarea celulelor canceroase4. Deşi reactivarea
telomerazei joacă un rol-cheie în dezvoltarea tumorilor, se pare că pentru
imortalizare este necesar şi un alt eveniment – inactivarea căii RB-E2F1 de control al ciclului celular. Cunoaşterea
acestor fenomene are consecinţe practice potenţiale: determinarea activităţii
telomerazei poate fi un marker de diagnostic precoce în cancer, iar inhibitorii
telomerazei ar putea deveni un mijloc eficace de tratament (molecula GRN163L se
află în stadiul de trial clinic).
5. Inducţia şi stimularea angiogenezei tumorale
Pentru
a creşte şi expansiona, tumorile au nevoie de aprovizionarea continuă cu
substanţe nutritive şi oxigen, precum şi de eliminarea deşeurilor metabolice şi
a bioxidului de carbon. Aceste funcţii sunt realizate prin dezvoltarea unei neovascularizaţii asociate tumorii, prin inducerea şi
stimularea procesului de angiogeneză sau de formare a unor vase noi.
Angiogeneza este reglată de diferite proteine de semnalizare: inductori (reprezentaţi de factorii de
creştere VEGF – „vascular endothelial
growth factors“ şi de FGF1 şi 2 – „fibroblast
growth factors“) şi inhibitori
(de exemplu, trombospondinele 1 şi 2, reglate de TP53), care se fixează pe
receptori specifici ai celulelor endoteliale, activând căile de semnalizare
intracelulară ce influenţează proliferarea şi creşterea celulelor endoteliale.
În
celulele tumorale se produc cantităţi crescute de inductori ai angiogenezei
precum şi blocarea inhibitorilor, ambele fenomene determinând o angiogeneză
intensă şi continuă, fenomen important pentru dezvoltarea tumorală. În aceste
condiţii, utilizarea unor inhibitori ai
angiogenezei ar putea fi benefică în terapia oncologică; în 2004, a fost
aprobată folosirea unui anticorp monoclonal direcţionat împotriva VEGF (bevacizumab) şi, mai recent, a unor
inhibitori ai receptorilor VEGF, de tipul sorafenibşi sunitinib. Efectele
terapeutice sunt însă tranzitorii, dată fiind dezvoltarea secundară a unor
mecanisme de rezistenţă. Există şi produse alimentare cu efecte
antiangiogenetice: derivatele de soia, bananele, ceaiul verde, vinul roşu etc.
6. Invazia tisulară şi metastazarea
Invazia
ţesuturilor vecine şi metastazarea la distanţă reprezintă caracteristica esenţială
a tumorilor maligne. Acest proces începe precoce
(!) în dezvoltarea tumorală şi se desfăşoară într-o secvenţă de mai multe etape cunoscută sub numele de „cascada invaziei şi metastazării“:
invadarea ţesuturilor vecine, pătrunderea celulelor canceroase în circulaţia
sangvină şi limfatică, tranzitul lor spre alte situsuri, ieşirea din circulaţie
sau extravazarea, formarea şi creşterea micrometastazelor (colonizarea).
Fiecare dintre aceste evenimente este determinat de achiziţia unor noi modificări
genetice şi epigenetice în clonele de celule tumorale, precum şi de cooptarea
unor celule stromale, care împreună „dotează“ celulele metastatice iniţiale cu
caracteristici necesare producerii de metastaze macroscopice (4). „Actorii şi
regizorii“ acestui „scenariu“ încep să fie elucidaţi. Un rol important îl au
anumiţi factori de transcripţie care stimulează expresia unor gene (deseori
specifice unui anumit tip tumoral) ce promovează iniţierea, progresia şi
agresivitatea invaziei şi metastazării (2, 4); la aceasta se adaugă inactivarea
unor gene supresoare ale metastazării. Descifrarea programelor ce reglează
aceste procese devine importantă pentru identificarea unor noi soluţii de
tratament. Progrese substanţiale s-au realizat în definirea unui set de gene („semnătura metastatică“) – de exemplu, MammaPrint® sau Oncotype Dx® în cancerul de sân – care se corelează cu
metastazarea, putând avea un rol prognostic şi utilitate în luarea unor decizii
terapeutice.
7. Instabilitatea genomică
În
majoritatea tumorilor umane se observă o creştere marcată a instabilităţii genomice, o proprietate
„permisivă“ care determină achiziţia caracteristicilor distinctive discutate
mai sus. Celulele canceroase au o rată
crescută a mutaţiilor (2, 3), care determină o succesiune de  expansiuni
clonale. Acest fenomen se explică prin: • creşterea sensibilităţii la mutageni • compromiterea sistemului de supraveghere care monitorizează integritatea
genomului şi determină celulele non-maligne cu alterări genetice să intre în
senescenţă sau apoptoză • alterarea unor componente ale „maşinăriei“ de menţinere a stabilităţii genomului şi de reparare a
leziunilor ADN. Recent au fost evidenţiate intervenţia frecventă a unor mecanisme epigenetice (metilarea ADN,
modificări ale histonelor) ce produc represia unor gene supresoare a creşterii
tumorale, precum şi rolul telomerelor în menţinerea stabilităţii genomice.
expansiuni
clonale. Acest fenomen se explică prin: • creşterea sensibilităţii la mutageni • compromiterea sistemului de supraveghere care monitorizează integritatea
genomului şi determină celulele non-maligne cu alterări genetice să intre în
senescenţă sau apoptoză • alterarea unor componente ale „maşinăriei“ de menţinere a stabilităţii genomului şi de reparare a
leziunilor ADN. Recent au fost evidenţiate intervenţia frecventă a unor mecanisme epigenetice (metilarea ADN,
modificări ale histonelor) ce produc represia unor gene supresoare a creşterii
tumorale, precum şi rolul telomerelor în menţinerea stabilităţii genomice.
8. Inflamaţia tumorală
O
altă proprietate „permisivă“ ce creşte achiziţia caracteristicilor definitorii
ale celulelor maligne este reprezentată de inflamaţia
asociată tumorilor. Cercetări recente arată că aproape toate tumorile
prezintă diferite grade de infiltraţie cu celule imunitare şi că inflamaţia
asociată tumorilor este un proces precoce
care poate exercita un efect de stimulare
a progresiei tumorilor incipiente. Inflamaţia furnizează numeroase molecule bioactive în micromediul
tumoral, inclusiv factori de creştere care susţin proliferarea celulară,
factori de supravieţuire care reduc moartea celulară, factori proangiogenetici,
enzime care modifică matricea extracelulară şi facilitează angiogeneza, invazia
şi metastazarea, precum şi specii reactive de oxigen cu efect mutagen, care pot
accelera evoluţia celulelor canceroase (2, 3).
9. Reprogramarea metabolismului energetic
Proliferarea
celulară cronică şi necontrolată conduce la ajustări importante ale
metabolismului energetic pentru a susţine creşterea şi diviziunea celulară.
Spre deosebire de celulele normale, care produc energie prin fosforilare
oxidativă mitocondrială, în celulele canceroase se produce o reprogramare a
metabolismului energetic şi majoritatea energiei celulare este furnizată pe calea glicolizei aerobe (efect
Warburg). Deşi eficienţa producerii de ATP este mai redusă, celulele canceroase
îşi intensifică importul de glucoză în citoplasmă. Se pare că principalul
avantaj al utilizării glicolizei aerobe este acela al generării de nucleozide şi
aminoacizi care sunt folosiţi pentru biosinteza de macromolecule şi organite
celulare necesare în cadrul diviziunii celulare rapide.
10. Evitarea distrugerii imune
Sistemul
imun operează ca o barieră la formarea şi progresia tumorilor incipiente. Declanşarea unor mecanisme
imunologice de apărare antitumorală este posibilă prin recunoaşterea unor
antigene tumorale specifice de pe suprafaţa celulelor tumorale şi activarea
celulelor dendritice mature, care, prin stimularea unor efectori intermediari,
determină expansiunea limfocitelor T citotoxice şi celulelor NK („natural killer“), care distrug
celulele tumorale. Celulele tumorale dezvoltă însă în timp mecanisme de imunoevaziune: evitarea
detecţiei („se deghizează“ şi
devin invizibile pentru sistemul
imun) şi secreţia unor factori
imunosupresori (TGF-β, IL-10, IDO, iNOS), care paralizează limfocitele T
citotoxice. Astfel, celulele canceroase evită distrugerea imună (2).
În
final, vom sublinia două idei, una teoretică şi alta practică, privind
caracteristicile distinctive ale cancerului.
• Tumorile nu sunt o masă „insulară“ omogenă,
de celule proliferative; ele formează un organ
complex, alcătuit din multiple tipuri de celule distincte, care interacţionează
unele cu altele. Parenchimul tumoral
este alcătuit din celulele canceroase
care iniţiază şi conduc progresia tumorală; ele nu sunt o populaţie omogenă, ci
un ansamblu de clone cu profil mutaţional diferit (heterogenitate intratumorală). O subclasă de celule tumorale este
reprezentată de celule stem canceroase
care se reînnoiesc continuu şi sunt mai rezistente la chimioterapie. Stroma şi micromediul tumoral sunt
reprezentate de celule normale asociate/recrutate de tumoră: celule
endoteliale, pericite, fibroblaşti, celule inflamatorii imune. Între toate
tipurile de celule ce formează tumora se produc interacţiuni complexe (prin diferite tipuri de semnale) care
„orchestrează“ dezvoltarea tumorală.
• Pe
baza definirii şi elucidării caracteristicilor
distinctive definitorii ale cancerului („hallmarks of cancer“) s-au
dezvoltat, în ultimul deceniu, terapii ţintitecătre moleculele implicate în aceste caracteristici (fig. 1). Ele au puţine efecte în afara ţintei (toxicitate redusă),
dar răspunsurile clinice sunt tranzitorii,
fiind urmate de recădere („rezistenţă adaptativă“), deoarece exprimarea fiecărei
capacităţi tumorale se realizează prin căi de semnalizare multiple, paralele şi
parţial redundante. Soluţia optimă ar fi combinarea terapiilor („ţintirea
concomitentă a tuturor căilor“), pe baza faptului că numărul căilor de
semnalizare este totuşi limitat. Despre toate acestea vom discuta în următorul
„capitol“ al oncogenomicii.
1Alte semnale
mitogene provin de la matricea extracelulară sau de la adeziunile
intercelulare;
2TGF-β = transforming growth factor beta;
caderine sau
CDH = calcium-dependent adhesion;
3SMAC = Second Mitochondria-derived Activator of
Caspase;
4În alte 10% din
cancere, menţinerea normală a lungimii telomerelor se realizează printr-un
mecanism alternativ, ce implică multiple recombinări la nivelul telomerelor.
 canceroase la mecanismele normale de moarte celulară programată (în
special apoptoza sau „sinuciderea“ celulei),
care sunt profund alterate în cancer. „Maşinăria“ apoptozei este alcătuită din senzori,
care monitorizează semnalele extra- şi intracelulare, efectori (caspazele, ce
produc proteoliza celulei) şi reglatori,proapoptotici (de exemplu, proteinele
TP53 şi BAX) sau antiapoptotici (de
exemplu, proteina BCL-2). Apoptoza este declanşată pe două căi majore: o cale extrinsecă, mediată de receptori
membranari, şi o cale intrinsecă sau
mitocondrială (3) (fig. 3). Calea
extrinsecă este iniţiată prin ataşarea unor liganzi (TNF-α, FAS) la receptori
membranari specifici, ce produce recrutarea şi activarea caspazei iniţiatoare
8, care la rândul ei va activa caspaza efectoare 3, răspunzătoare de inducţia
apoptozei. Calea intrinsecă este declanşată în special de alterări ale ADN,
care, prin activarea proteinei TP53, determină eliberarea unor factori
proapoptotici (citocromul c, SMAC3)
din mitocondrii, care activează caspazele efectoare 3 şi 9.
canceroase la mecanismele normale de moarte celulară programată (în
special apoptoza sau „sinuciderea“ celulei),
care sunt profund alterate în cancer. „Maşinăria“ apoptozei este alcătuită din senzori,
care monitorizează semnalele extra- şi intracelulare, efectori (caspazele, ce
produc proteoliza celulei) şi reglatori,proapoptotici (de exemplu, proteinele
TP53 şi BAX) sau antiapoptotici (de
exemplu, proteina BCL-2). Apoptoza este declanşată pe două căi majore: o cale extrinsecă, mediată de receptori
membranari, şi o cale intrinsecă sau
mitocondrială (3) (fig. 3). Calea
extrinsecă este iniţiată prin ataşarea unor liganzi (TNF-α, FAS) la receptori
membranari specifici, ce produce recrutarea şi activarea caspazei iniţiatoare
8, care la rândul ei va activa caspaza efectoare 3, răspunzătoare de inducţia
apoptozei. Calea intrinsecă este declanşată în special de alterări ale ADN,
care, prin activarea proteinei TP53, determină eliberarea unor factori
proapoptotici (citocromul c, SMAC3)
din mitocondrii, care activează caspazele efectoare 3 şi 9. expansiuni
clonale. Acest fenomen se explică prin: • creşterea sensibilităţii la mutageni • compromiterea sistemului de supraveghere care monitorizează integritatea
genomului şi determină celulele non-maligne cu alterări genetice să intre în
senescenţă sau apoptoză • alterarea unor componente ale „maşinăriei“ de menţinere a stabilităţii genomului şi de reparare a
leziunilor ADN. Recent au fost evidenţiate intervenţia frecventă a unor mecanisme epigenetice (metilarea ADN,
modificări ale histonelor) ce produc represia unor gene supresoare a creşterii
tumorale, precum şi rolul telomerelor în menţinerea stabilităţii genomice.
expansiuni
clonale. Acest fenomen se explică prin: • creşterea sensibilităţii la mutageni • compromiterea sistemului de supraveghere care monitorizează integritatea
genomului şi determină celulele non-maligne cu alterări genetice să intre în
senescenţă sau apoptoză • alterarea unor componente ale „maşinăriei“ de menţinere a stabilităţii genomului şi de reparare a
leziunilor ADN. Recent au fost evidenţiate intervenţia frecventă a unor mecanisme epigenetice (metilarea ADN,
modificări ale histonelor) ce produc represia unor gene supresoare a creşterii
tumorale, precum şi rolul telomerelor în menţinerea stabilităţii genomice.