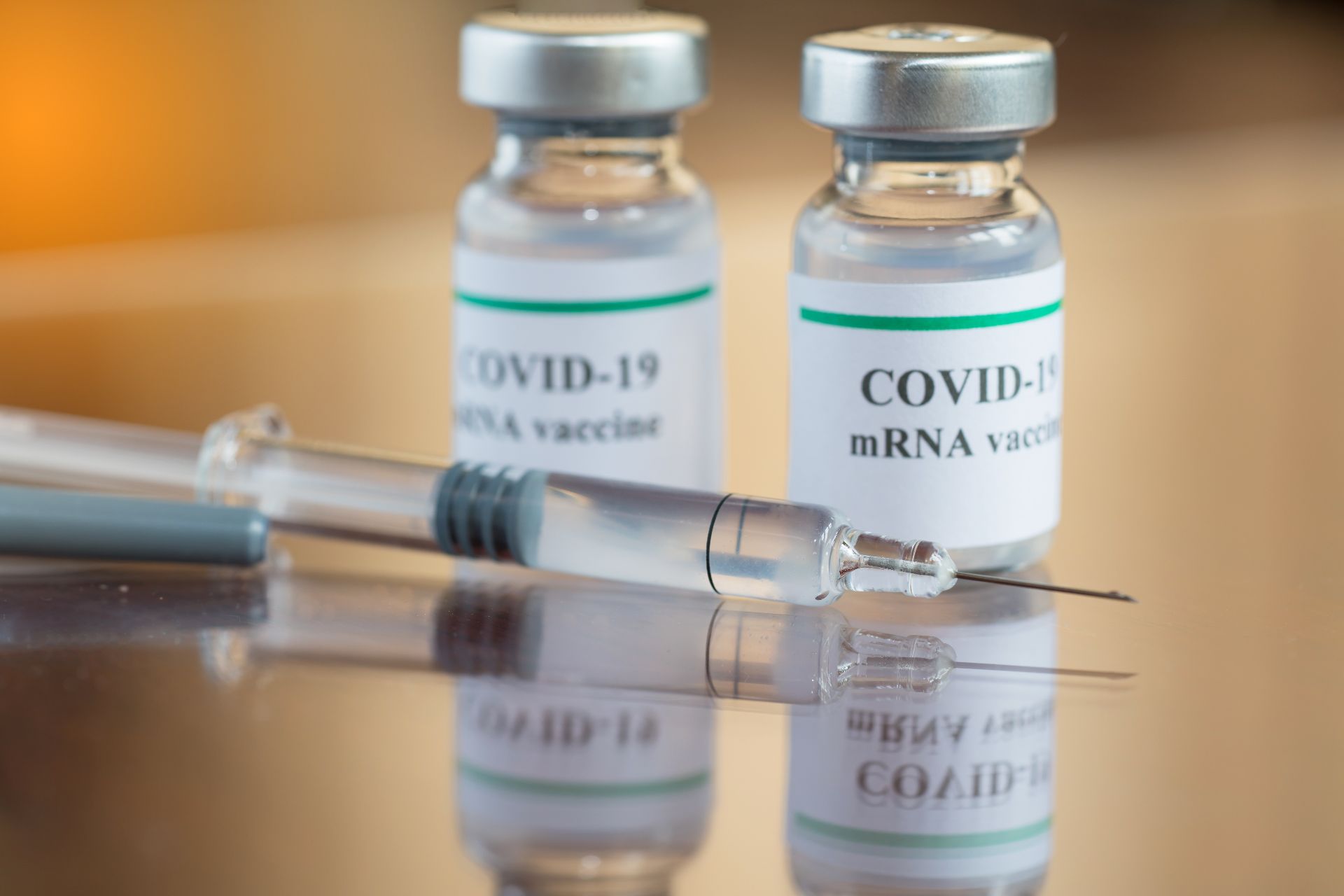
Compania farmaceutică Moderna a înaintat către FDA documentele pentru aprobarea utilizării de urgenţă pentru vaccinul său anti-COVID-19.
 Reprezentanţii companiei plănuiesc și să ceară o autorizare condiţionată de punere în piaţă din partea Agenţiei Europene pentru Medicamente (EMA). Procesul de evaluare a vaccinului pe bază de ARN mesager (mRNA) va fi efectuat de EMA după un orar accelerat.
Reprezentanţii companiei plănuiesc și să ceară o autorizare condiţionată de punere în piaţă din partea Agenţiei Europene pentru Medicamente (EMA). Procesul de evaluare a vaccinului pe bază de ARN mesager (mRNA) va fi efectuat de EMA după un orar accelerat.
O opinie referitoare la autorizarea de punere pe piaţă ar urma să fie emisă în câteva săptămâni, spun reprezentanţii agenţiei. Acest lucru se va întâmpla dacă datele depuse de compania farmaceutică sunt suficient de robuste și complete pentru a demonstra calitatea, siguranţa şi eficacitatea vaccinului împotriva COVID-19.
Agenţia și comitetele sale știinţifice vor continua procesul de evaluare în perioada Crăciunului. În cazul în care se va ajunge la concluzia că vaccinul de la Moderna este sigur și eficace, Comitetul EMA pentru medicamente de uz uman va finaliza evaluarea în timpul unei întâlniri programate anul viitor, în 12 ianuarie.
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe