
Cu o eficienţă similară cu a produselor originale, dar cu costuri mai reduse, biosimilarele permit un acces mai larg la tratamente de ultimă generaţie în oncologie.
Termenul de „toxicitate financiară” (TF) a început să circule în literatura medicală și în paginile media cu precădere în ultima decadă, odată cu creșterea tot mai accentuată a contribuţiei materiale a pacientului pentru a-și asigura tratamentul pentru boala de care suferă – cel mai adesea, cancer. Dificultăţile financiare ale pacientului oncologic au cauze complexe. Printre acestea, o pondere însemnată o are preţul tot mai ridicat al tratamentelor, în special cu medicamente noi, diferite de „citostaticele” clasice.
Fără să existe o definiţie standard, termenul de TF circulă sinonim cu dificultăţi financiare sau greutăţi financiare legate de un tratament. El se referă la consecinţele nefaste pe care le au costurile ridicate ale tratamentelor, peste limitele sustenabile, asupra calităţii vieţii și chiar duratei de viaţă a pacienţilor, îndeosebi cei oncologici. Consecinţele sunt atât de ordin fizic (întreruperea fortuită a tratamentului, reducerea dozelor prescrise, lipsirea de o serie de mijloace de existenţă, precum locuinţă, alimentaţie), cât și psihologice, inducând sau agravând starea de depresie și anxietate. 
Astfel, termenul de TF vrea să atragă atenţia asupra unui alt fel de efect advers pe care medicamentele, îndeosebi cele oncologice, recunoscute în general pentru toxicitatea lor fizică, le înregistrează la un număr tot mai mare de pacienţi. De asemenea, conceptul de TF are ca scop sensibilizarea forurilor decidente și a medicilor din fiecare ţară asupra acestei probleme, pentru a-i determina să intervină prin măsuri sociale și politici de sănătate, precum și prin opţiuni terapeutice adecvate. Contrar a ceea ce s-ar putea crede, TF afectează pacienţii din toate ţările, chiar și din cele mai avansate economic, precum SUA.
Una dintre căile la îndemână pentru reducerea costurilor tratamentelor oncologice este utilizarea pe scară tot mai largă a medicamentelor generice și biosimilare (BS). Medicamentele biologice sunt adesea singurele tratamente disponibile pentru o serie de afecţiuni grave, precum cancerul sau bolile genetice, dar accesul la acestea presupune eforturi financiare considerabile, de multe ori imposibile, pentru pacienţi și familiile lor, chiar și pentru cei asiguraţi sau cei cu venituri importante. Biologicele reprezintă aproape 40% din cheltuielile cu medicamentele eliberate pe bază de reţetă și sunt responsabile de 70% din cuantumul creșterii cheltuielilor cu medicamentele în perioada 2010–2015.
Medicamentele biosimilare sunt versiuni alternative ale medicamentelor biologice existente, făcând parte, din acest punct de vedere, din aceeași categorie cu a genericelor. Ambele tipuri de produse sunt similare cu medicamentele producătorului care le-a iniţiat, le-a patentat și le-a introdus pe piaţă, ele fiind însă realizate și distribuite de alţi producători, după expirarea patentului, adică a perioadei în care proprietarul patentului sau al brandului are drept exclusiv de comercializare. Spre deosebire de generice, care sunt molecule mici, identice cu originalul, obţinute prin sinteză chimică, biosimilarele provin din surse umane, animale sau din microorganisme vii, au o complexitate moleculară mare și o structură care poate suferi modificări în decursul procesului de producţie. Astfel, BS sunt mai degrabă „copii biologice” ale produsului de referinţă. Ele sunt însă sigure, au puritate, eficacitate și toxicitate similare cu ale produsului de referinţă, sunt puse în circulaţie după o procedură similară de aprobare cu cea a „originalului”, iar producerea și distribuţia lor sunt reglementate prin reguli specifice. Costurile de producţie și distribuţie sunt substanţial mai mari faţă de cele ale genericelor, însă semnificativ mai reduse (cu cca. 10–50%) decât ale produselor de referinţă.
Beneficiul financiar adus de biosimilare este perceput și de sistemele de sănătate, care înregistrează astfel reduceri de cheltuieli semnificative (de cel puţin 54 de miliarde de dolari în viitorii zece ani în SUA, de exemplu), comparativ cu scenariile în care s-ar folosi doar biologice originale. Mai mult, ele aduc un plus de competitivitate pe un segment de piaţă în care altfel erau puţini competitori și, totodată, încurajează consumul de medicamente biologice în general, care devin astfel accesibile unei proporţii mai largi de pacienţi, îndeosebi unor categorii mai defavorizate ale populaţiei, care altfel nu și le-ar permite, după cum rezultă din primele analize realizate în SUA în acest domeniu (fig. 1).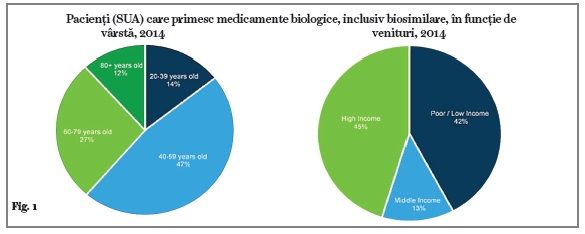
BS trebuie diferenţiate de biosuperioare („biobetters” sau „biosuperiors”), care sunt medicamente biologice similare unora anterioare, dar care au o eficacitate terapeutică crescută și un regim asemănător cu cel al medicamentelor noi.
BS sunt supuse unui „atac” susţinut din partea unor producători de branduri, care speculează tocmai lipsa identităţii acestor produse, pentru a induce îndoiala printre consumatori, pacienţi și medici, mai ales privind substituibilitatea. În fapt, este practic imposibil pentru un producător de biosimilare să realizeze un produs perfect identic cu originalul, însă diferenţele minime existente nu afectează nici eficacitatea și nici siguranţa. Cu toate reticenţele încă prezente printre pacienţi și medici, de la aprobarea lor în 2006 în Europa și în 2010 în SUA, producţia de BS este într-o continuă extindere, piaţa lor globală urmând a ajunge, conform unor estimări recente, la 100 de miliarde de dolari în 2025.
Subliniind progresele înregistrate până în prezent, trebuie menţionat, totuși, că domeniul BS se află încă la început, el rămânând totodată unul complex, incluzând aspecte juridice, administrative, tehnice, medicale, psihologice, de marketing și altele. Între acestea, una dintre condiţiile importante pentru reușita implementării largi a BS este o bună și largă informare și educare a profesioniștilor și a pacienţilor privind produsele, precum și o activă supraveghere și informare „post-market” privind efectelor acestora.
Până în anul 2018, erau aprobate pentru aplicare în terapia medicală 16 biosimilare în USA și aproximativ 50 în UE (fig. 2). 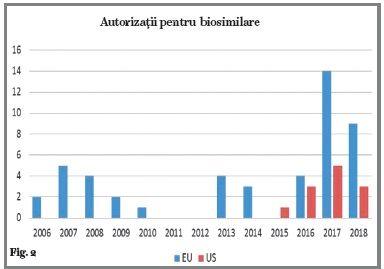
BS cu aplicaţie în oncologie aprobate în prezent în UE și SUA corespund unor categorii de biologice precum anticorpii monoclonali (respectiv Trastuzumab-Herceptin, utilizat în cancerul de sân, Bevacizumab-Avastin, în cancerul metastazat de colon, pulmonar, mamar și renal, Rituximab-Mabthera, în limfoamele nonhodgkiniene) și factorii de creștere hematopoietici (respectiv eritropoietina alfa-Eprex și Procrit și factorul de creștere granulocitar plus varianta sa pegylata – Neupogen și Neulasta). BS au denumiri comerciale proprii, diferite de la un producător la altul, existând mai multe BS pentru un singur biologic. Fiecare produs necesită reţetă specifică din partea medicului specialist, neputând să substituie automat un produs de referinţă sau unul cu o altă denumire. Utilizarea BS și modul de rambursare sau acoperire a costurilor sunt reglementate de fiecare stat.
1. Zafar S.Y., Abernethy A.P. Financial Toxicity, Part I: A New Name for a Growing Problem. Oncology 2013; 27(2):80
2. Tran, G. Zafar S.Y. Financial toxicity and implications for cancer care in the era of molecular and immune therapies. Ann Transl Med 2018;6(9):166
3. Naveed Saleh, The Reality of Cancer Biosimilars: Challenges and New Hope. CancerNetwork, 30 Oct., 2018
4. Lyman G.H. et al. Rationale, Opportunities, and Reality of Biosimilar Medications. New England Journal of Medicine, 2018,378(21):2036–44
5. Lee K.H. et al. Analytical similarity assessment of rituximab biosimilar CT-P10 to reference medicinal product. mAbs 2018, 10(3):380–96
6. Zafar S.Y. The Financial Toxicity of Cancer Treatment: A Pilot Study Assessing Out-of-Pocket Expenses and the Insured Cancer Patient’s Experience. The Oncologist 2013; 18:381–90
7. de Souza J.A. et al. The Development of a Financial Toxicity Patient-Reported Outcome in Cancer. Cancer 2014;120:3245–53
8. Beck A. Biosimilar, biobetter and next generation therapeutic antibodies. mAbs 2011, 2(3):108
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe