
În iulie, a fost publicat de comitetul GOLD* un articol ce poate fi un îndreptar pentru medicul de familie în privinţa BPOC, o afecţiune care adesea pendulează între medicul de familie și pneumolog.
Medicii de familie au propriile ghiduri și legi, iar acest protocol le este mai puţin cunoscut. Pentru pneumologi, bronhopneumopatia obstructivă cronică (BPOC) dă în fiecare an semnalul unor schimbări în strategia diagnostică și terapeutică. Am considerat că publicarea unor mesaje-cheie din partea acestei echipe de experţi trebuie să aibă un răsunet în lumea medicilor de familie din România, cu atât mai mult cu cât accesul lor la Viaţa Medicală este mult mai facil, iar această publicaţie reprezintă ea însăși o trambulină între specialităţi.
Se pleacă de la premisa că BPOC reprezintă o afecţiune heterogenă, cu simptome clasice – dispnee, tuse, expectoraţie – și/sau exacerbări, însoţită de anomalii ale căilor aeriene (bronșiolite, bronșită) și anomalii alveolare (emfizem), acestea fiind progresive și cu obstrucţie (VEMS/CVF<0,7). Dacă înainte se considera că boala este apanajul bărbaţilor fumători cu vârsta peste 45 de ani, acum se cunoaște că prevalenţa este similară la bărbaţi și femei și că această afecţiune poate fi întâlnită și la tineri sau la nefumători. Totodată, se sugerează că cele mai dăunătoare efecte ale fumatului se înregistrează la sexul feminin.
Femeile prezintă mai multă dispnee și tuse, un declin mai profund al funcţiei pulmonare și o agravare mai importantă legată de spitalizări, precum și insuficienţă respiratorie și risc de deces mai mare decât bărbaţii. În plus, pe lângă faptul că se vorbește acum și de implicarea poluării în apariţia bolii, se mai semnalează și mutaţia unei gene, SERPINA 1, care duce la deficienţa de α1-antitripsină. Expunerile profesionale asociate cu BPOC sunt praful organic și anorganic, agenţii chimici, fumul și poluanţii aerieni.
Se știe că 50% dintre marii fumători dezvoltă BPOC, dar și o treime dintre nefumători fac această boală. Fumatul pasiv este un factor de risc, iar expunerea fătului în timpul sarcinii alterează creșterea plămânului. În ţările în curs de dezvoltare sau cu dezvoltare medie, nefumătorii reprezintă 60-70% dintre pacienţii cu BPOC, deoarece arderea de biomasă, precum și focurile utilizate pentru pregătirea hranei slab funcţionale expun mai mult femeile și tinerii.
În cazul nefumătorilor, simptomele și disfuncţiile spirometrice sunt similare cu cele induse de fumat, dar emfizemul este mai puţin prevalent, iar diminuarea funcţiei pulmonare este mai puţin evidentă. De asemenea, acum se știu mai multe despre evoluţia plămânului după naștere: crește și ajunge la maturitate la 20-25 de ani (sau mai devreme la sexul feminin), atinge platoul și apoi începe un declin ușor, prin îmbătrânire.
La capitolul diagnostic, în prezenţa simptomatologiei trebuie realizată spirometria. Aceasta ar trebui efectuată și în centre de medicină primară, dar, atenţie, de medici, asistente și tehnicieni pregătiţi, instruiţi pentru a face spirometrii valide, scenariu care nu este realizabil în ţările în curs de dezvoltare. Având în vedere că această patologie este subdiagnosticată, este recomandat screeningul activ în cazurile cu simptome și factori de risc, dar nu screeningul spirometric simplu cu anumite corecţii (dispozitivele portabile mici pot fi folosite pentru a exclude BPOC, dar nu pentru a confirma afecţiunea). Screeningul spirometric simplu nu poate face diferenţa între BPOC și alte boli respiratorii parţial reversibile, precum astmul, bronșiectaziile, sindroamele post-tuberculoase etc.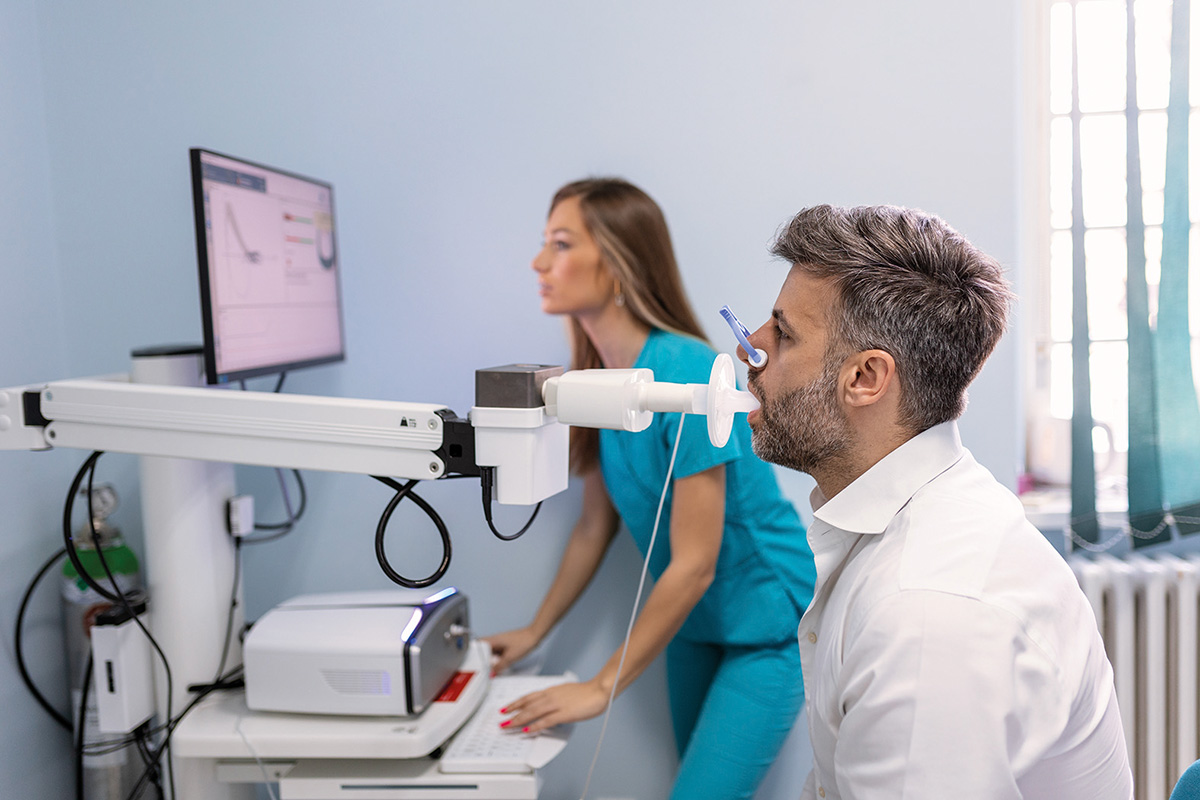
Dacă pentru evaluarea gradului de severitate a BPOC rămâne valabilă clasificarea legată de VEMS, pentru asimptomaticul fără expunere nu se recomandă screeningul spirometric. Pentru cei cu simptome și cu factori de risc (≥20 pachete de ţigări pe an, infecţii pulmonare recurente, prematuritate sau evenimente în primii ani de viaţă), spirometria rămâne metoda validă. Se vorbește și de un pre-BPOC, pe care noul GOLD 2023 îl recunoaște la cei fără obstrucţie de căi aeriene, dar cu simptome și anomalii funcţionale (reducere a capacităţii de difuziune a monoxidului de carbon, declin accentuat al VEMS) sau cu anomalii pe CT (emfizem în progresie), dar cu raport VEMS/CV păstrat. Pacienţii cu VEMS/CV păstrat, dar cu VEMS scăzut sunt incluși acum în grupul PRISm („Preserved Ratio with Impaired Spirometry”). Ei pot sau nu să progreseze către BPOC.
Medicul de familie trebuie să știe, la fel ca și specialistul, că s-a schimbat și definiţia exacerbării. Este considerată un eveniment caracterizat prin amplificarea dispneei și/sau tusei și producţiei de spută, care se agravează în mai puţin de 14 zile de la debutul exacerbării și care se însoţește de tahipnee și/sau tahicardie, fiind asociată cu inflamaţie locală și sistemică provocată de infecţii, poluare sau alte agresiuni. Medicul de familie poate juca aici o carte câștigătoare pentru pacient, prin detectarea și recunoașterea precoce a semnelor și simptomelor sugestive de exacerbare. 
Sigur că trebuie să facă diagnostic diferenţial cu insuficienţa respiratorie, pneumonia sau tromboembolismul pulmonar. Confirmarea severităţii exacerbărilor se poate face printr-o scală vizuală de apreciere a dispneei de la 0 la 10, prin măsurarea nivelului proteinei C reactive, iar dacă se consideră că are indicaţie de terapie intensivă, prin gazometrie (în ţările în care medicul de familie are acces la gazometrie, aceasta poate tranșa indicaţia).
Printre recomandările comisiei de experţi se conturează și indicaţiile de spitalizare: severitatea simptomelor (dispnee, rată respiratorie crescută, saturaţia de O2 sub 92%), confuzie, somnolenţă, insuficienţă respiratorie acută, cianoză, edeme periferice, lipsa de răspuns la iniţierea terapiei, prezenţa unor comorbidităţi (insuficienţă cardiacă, aritmii etc.), absenţa sau insuficienţa suportului la domiciliu.
O variantă de tratament ambulatoriu o constituie administrarea de anticolinergic de scurtă durată asociat cu beta-2 adrenergic de scurtă durată în pMDI, cu spacer, dar uneori este nevoie de nebulizare (aceasta se va face însă cu aer ambiant, și nu cu oxigen, pentru a nu exista risc de creștere a CO2). Trebuie evitată administrarea de aminofiline, teofiline etc. Corticoizii orali (40 mg de prednisolon) pot fi indicaţi în exacerbările severe, cu administrare doar pentru 5 zile; la fel și antibioticele (5-7 zile la infecţiile bacteriene, adaptate în funcţie de antibiorezistenţele locale sau personalizate individual). 
Oxigenoterapia la domiciliu este indicată cu titrare pentru menţinerea saturaţiei între 88-92% și se recomandă în special pe mască Venturi, iar ventilaţia noninvazivă este indicată în caz de acidoză respiratorie. Medicul de familie trebuie să fie atent și la comorbidităţile cele mai frecvente, precum cele cardiovasculare, cancerul pulmonar (screeningul pentru cancer indicat în prezent se poate face la vechii fumători și în căutarea emfizemului pulmonar), bronșiectaziile, sindromul de apnee în somn (prezent la 14% dintre bolnavii cu BPOC), osteoporoza, diabetul, sindromul metabolic, anemia, policitemia, boli psihice și refluxul gastroesofagian.
Riscul de infecţie COVID-19 nu este mai mare pentru persoanele cu BPOC, dar atunci când infectarea se produce, se asociază cu un risc mai mare de spitalizare, de internare în terapie intensivă și cu o mortalitate crescută. Astfel că medicii de familie ar trebui să fie avertizaţi asupra acestei posibile combinaţii. Toate aceste recomandări au o singură misiune: să pregătească medicul de familie pentru a contribui la deconspirarea acestei afecţiuni cronice, adesea subdiagnosticată și subevaluată. Poate că spirometriile realizate precoce, la grupele de vârstă 20-25 de ani, în contextul altor comorbidităţi, ar fi utile în această luptă de identificare a unei boli cu potenţial de cronicizare.
Evoluţia plămânului poate fi afectată de factori multipli:
– prematuritate, greutate mică la naștere, fumatul mamei în timpul sarcinii, infecţii respiratorii repetate, deficit de elemente nutritive (50% dintre persoanele cu BPOC prezintă aceste dezvoltări și creșteri pulmonare anormale);
– sărăcia și statusul socioeconomic scăzut, cu expunere la poluare ambientală;
– infecţiile respiratorii severe ale copilăriei asociate cu reducerea funcţiei pulmonare și creșterea simptomatologiei respiratorii la vârsta adultă (la adult, în special infecţiile cu Pseudomonas aeruginosa și tuberculoza determină declin accelerat al VEMS).
Se propune și o nouă taxonomie ancorată în etiotipuri:
– BPOC determinat genetic
(COPD-G),
– determinat de dezvoltarea anormală a plămânului (COPD-D),
– de mediu (cauzat de fumat – COPD-C – sau de expunerea la biomasă și aer poluat – COPD-P),
– determinat de infecţii (COPD-I),
– BPOC asociat astmului (COPD-A, particular la copii),
– BPOC de cauze necunoscute (COPD-U).
Trecerea de la clasificarea ABCD (ţinând cont de exacerbări, calitatea vieţii, nivelul simptomelor) la cea ABE reprezintă o altă schimbare de abordare terapeutică. Practic, zonele AB rămân nemodificate, dar cazurile CD merg în grupul E (exacerbări). Acest lucru schimbă abordarea farmacologică. Totul se construiește în această zonă pe alegerea terapiei inhalatorii. Aici, medicina primară are o misiune importantă, deoarece trebuie făcută educaţia și iniţierea bolnavului, de preferat faţă în faţă, și nu prin telemedicină. Și pe aceste direcţii intervin o multitudine de elemente, precum:
– disponibilitatea medicamentului și a dispozitivului;
– părerea pacientului, satisfacţia cu actualul și anteriorul dispozitiv;
– numărul dispozitivelor folosite – acesta ar trebui diminuat, preferabil la unul singur;
– trecerea să nu se facă fără justificări medicale, fără informare, educare și monitorizare;
– alegerea dispozitivului de inhalare cel mai apropiat de strategia aleasă;
– cunoașterea dexterităţii și puterii de înţelegere a bolnavului;
– se vor folosi inhalatoare cu pudră uscată (DPI) doar dacă pacientul are suficientă putere pentru o inhalare profundă (de verificat vizual acest lucru);
– folosirea MDI (metered-dose inhalers) sau a SMI (slow mist inhalers) impune coordonare, inhalare profundă și lentă (dacă pacientul nu îndeplinește condiţia, se adaugă un spacer sau alte alternative);
– la cei neadaptaţi la vreo formă de utilizare se recomandă nebulizator;
– alţi factori care pot influenţa alegerea terapiei pot fi portabilitatea, costurile;
– pentru persoanele incapabile să folosească vreun dispozitiv, trebuie folosite inhalatoare inteligente care pot verifica aderenţa;
– medicii vor prescrie doar dispozitive pe care pacientul sau familia știu să le
folosească.
În ce privește iniţierea terapiei, dacă la grupa A a rămas recomandată administrarea unui bronhodilatator, la grupa B se recomandă dualterapie bronhodilatatorie (superioară monoterapiei). La grupa E se merge similar, cu excepţia pacienţilor cu ≥300 de eozinofile/µl. La aceștia se începe cu tripla terapie cu două bronhodilatatoare și un corticoid inhalator. Nu se mai încurajează asocierea beta 2 adrenergic-corticoid inhalator, ci se preferă tripla terapie, dacă este cazul de asociere de corticoid inhalator. Pacienţii cu astm și BPOC vor fi trataţi ca bolnavi de astm.
La capitolul terapie de întreţinere, dacă pacientul are dispnee și nu răspunde bine la monoterapie bronhodilatatorie, după verificarea tehnicii administrării medicamentului și a aderenţei la tratament va fi trecut pe dualterapie bronhodilatatorie. Iar dacă nici acum nu este bine, se caută alte molecule sau inhalatoare, se face reabilitare și se verifică să nu existe cauze adiacente de dispnee. Pentru cei care au exacerbări în continuare, cu sau fără dispnee, se poate face escaladarea la două bronhodilatatoare și doar la cei cu eozinofile peste 300/µl se trece la triplă terapie.
Și la cei care au exacerbări și sunt pe dualterapie bronhodilatatorie se poate face trecerea pe triplă terapie dacă au eozinofilele peste 100/µl. Există semnale că tripla terapie poate reduce mortalitatea. Pentru cei care au în continuare exacerbări pe triplă terapie sau care au eozinofile sub 100/µl se poate adăuga roflumilast, în particular la cei cu VEMS <50% din cel prezis, sau macrolide la cei care sunt fumători. Toate acestea impun monitorizări stricte și dezescaladările de pe corticoizi inhalatorii, dar cu mare atenţie la riscul de reapariţie a exacerbărilor.
În schimb, pentru cei cu BPOC și fără trăsături de astm, care, indiferent de raţiunile motivante, au fost trataţi cu beta-2 adrenergic și corticoid inhalator și au mers bine din punctul de vedere al simptomelor și exacerbărilor, autorii recomandă să rămână în continuare pe această asociere. Cei dispneici vor fi trecuţi pe două bronhodilatatoare, iar dacă prezintă noi exacerbări vor fi trecuţi pe triplă terapie.
În zona de tratament nonfarmacologic lista este foarte lungă. Pe lângă educaţia de bază despre inhalatoare, medicaţie – unde medicul de familie este o piesă de bază –, se atrage atenţia și asupra unei intervenţii personalizate, individuale și în context sociodemografic. Sunt necesare cel puţin sfatul minimal pentru fumători, alături de strategiile de reducere a poluării ambientale.
Se impun vaccinarea împotriva gripei, a pneumococului, COVID-19, pertussis și herpes zoster, activitatea fizică și suportul nutriţional și psihosocial. O altă variantă o constituie reabilitarea respiratorie (adaptată în funcţie de comorbidităţi și de caracteristicile bolii) pentru cei din grupele B și E, dar și reabilitarea combinată, în anumite situaţii, de exemplu pentru cei cu afecţiuni cardiovasculare.
La toate acestea se adaugă oxigenoterapia, ventilaţia noninvazivă și variantele chirurgicale: chirurgia de reducere a parenchimului (la cei cu emfizem omogen sau heterogen, cu hiperinflaţie refractară la tratament chirugical sau bronhoscopic). La pacienţii tineri cu BPOC sever se poate opta pentru transplantul pulmonar. De asemenea, bolnavul și familia acestuia trebuie să ia în considerare îngrijirile paliative.
*Global Initiative for Chronic Obstructive Lung Disease
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe