Această alternativă la „standardul de aur” în transplantul medular le ușurează pacienţilor accesul la un donator, respectiv la un tratament eficient.
De la prima sa aplicare cu succes la om în 1956 (E.D. Thomas, SUA, premiul Nobel pentru medicină în 1975), transplantul de măduvă osoasă, devenit între timp transplantul de celule stem hematopoietice (TCSH), și-a câștigat, după numeroase îmbunătăţiri, un loc bine definit în arsenalul terapeutic al hemopatiilor maligne și nu numai. Acest loc s-a menţinut, cu toate progresele înregistrate în ultimele două decade în chimio- și imunoterapie.
Complexitatea procedurii, complicaţiile imediate și la distanţă, riscul vital și costul ridicat sunt printre principalii factori care obligă la o judicioasă selecţie a candidaţilor, bazată pe evaluarea raportului risc/beneficiu, și care au limitat accesul pacienţilor la această procedură terapeutică cu potenţial curativ. În plus, absenţa unui donator HLA (human leukocyte antigen) compatibil înrudit sau neînrudit cu pacientul a constituit un element frecvent limitativ, atât prin faptul că numai pentru cca. 50% dintre candidaţii la TCSH se găsesc donatori compatibili, cât și prin întârzierea mare cu care celulele stem hematopoietice ale donatorului compatibil neînrudit ajung să fie transplantate. Lor li se adaugă costul adeseori prohibitiv al obţinerii lor, îndeosebi în ţările mai puţin dezvoltate (1-4).
Plecând de la conștientizarea faptului că membrii de gradul 1 ai familiei unui individ (părinţi, copii), dar și 50% dintre fraţi sau surori au în comun o jumătate („haplo”) din genotipul HLA și că, astfel, aproape toţi candidaţii pentru alo-TCSH pot avea acces la un membru al familiei ca donator de celule stem hematopoietice, s-a propus efectuarea transplantului cu celule prelevate de la aceștia. Primele încercări, efectuate în anii ’70, s-au dovedit însă infructuoase, ca urmare a procentului mare de cazuri de boală grefă-contra-gazdă (BGcG) și respingerii grefei, prin aloreactivitatea limfocitelor T ale donatorului și ale gazdei, dar și prin complicaţiile infecţioase grave, consecinţă a refacerii imune întârziate (1,3,4).
Situaţia s-a îmbunătăţit substanţial când un colectiv din Centrul de Cercetări afiliat Universităţii Johns Hopkins (Baltimore, Maryland, SUA) a aplicat, în 2008, iniţial la șoareci și apoi la om, practica administrării la un interval scurt post-transplant de doze mari de ciclofosfamidă (abreviat PTCy). Acesta este un medicament alchilant cu efecte deja cunoscute experimental de creștere a toleranţei imune (5), în afara efectelor sale antitumorale. Principala realizare a TCSH haploidentic (haplo-TCSH) a constituit-o controlul efectelor secundare aloreactivităţii, însoţit de menţinerea echilibrului privind refacerea imună și efectul benefic grefă-anti-tumoră (leucemie) (5). A fost astfel posibilă transplantarea de celule stem hematopoietice conţinând un număr normal de limfocite T, înlocuind procedurile anterioare, care presupuneau manipulări complexe ale grefei pentru depletizarea (eliminarea) limfocitelor donatorului (1,5).
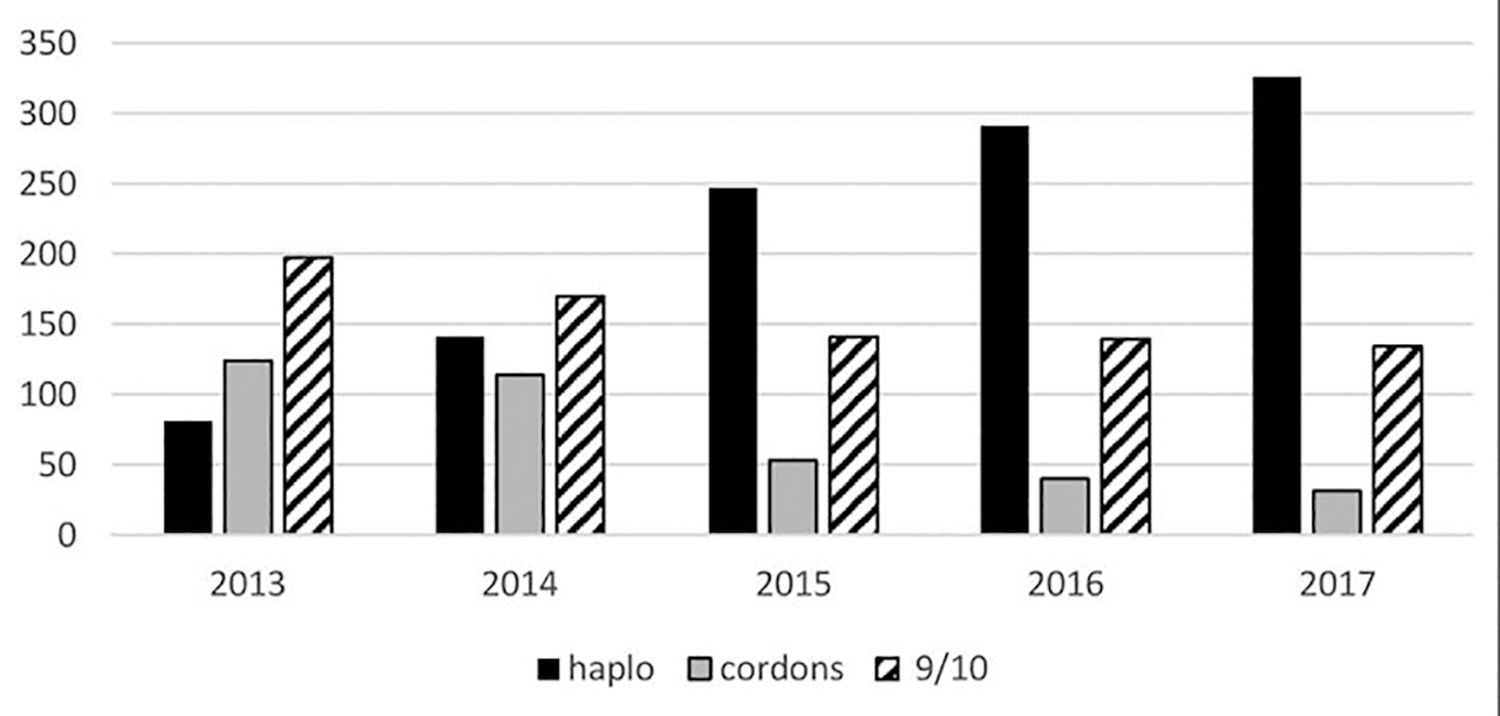
Ca urmare, metoda haplo-TCSH-PTCy s-a impus pe plan mondial, ea cunoscând un plin avânt (fig. 1) și devenind tot mai populară începând cu anul 2012. Metodologia sa a fost aplicată cu succes în multe ţări cu grade variate de dezvoltare economică, inclusiv în ţara noastră (6-9).
Procedura a avut la bază constatarea că limfocitele T aloreactive aflate în proliferare, atât ale gazdei, cât și ale donatorului, sunt mai sensibile la efectele citotoxice ale ciclofosfamidei (Cy) comparativ cu limfocitele T în repaus sau de memorie. Administrarea de Cy pacientului candidat pentru TCSH la un anume interval de timp (3-4 zile) după introducerea celulelor medulare haploidentice, Cy fiind medicament antineoplazic puternic imunosupresor, determină eliminarea limfocitelor T puternic activate și intens proliferante atât ale donatorului, responsabile de boala grefă-contra-gazdă (BGcG) severă, cât și ale gazdei, responsabile de respingerea grefei, însă fără să afecteze limfocitele T de memorie, în repaus, responsabile de imunitatea antiinfecţioasă. Este vorba despre un proces de distrugere selectivă. Limfocitele T aloreactive sunt mai sensibile la acţiunea apoptotică a Cy, deoarece se află în faza de proliferare intensă sub acţiunea stimulului oferit de aloantigenele puternic reactive, furnizate tocmai de incompatibilitatea parţială („haploidentitate”) dintre donator și primitor. În schimb, limfocitele T „naive” ale donatorului primite odată cu grefa persistă în organismul gazdei, contribuind substanţial la reconstituirea imună periferică. Ele se diferenţiază și devin rapid efectorii și active atât împotriva antigenelor agenţilor infecţioși, cât și împotriva antigenelor tumorale (efect „grefă-contra-leucemie”). Totodată, are loc dezvoltarea unei toleranţe periferice, atât imediată, cât și de lungă durată, ca urmare îndeosebi a supresiei realizate de limfocitele T reglatoare (T-reg) și deleţiei limfocitelor T anti-gazdă ale donatorului după grefare.
De menţionat că administrarea Cy înainte de grefare a indus o bună acceptare a celulelor grefate, dar a fost urmată de o creștere marcată a BGcG, urmare a acţiunii limfocitelor T ale donatorului rămase neafectate.
În același timp, celulele stem hematopoietice pluripotente grefate sunt protejate de efectele citotoxice ale ciclofosfamidei datorită nivelurilor ridicate ale enzimei dehidrogenază aldehidică prezente și care le conferă rezistenţă faţă de agenţii alchilanţi, asigurându-se astfel supravieţuirea grefei și sinteza de limfocite T. Prin același mecanism sunt protejate și populaţiile de limfocite T reglatoare (Treg) foxp3+ care conferă protecţie împotriva BGcG, ceea ce explică incidenţa mai redusă a acestei complicaţii constatată post-haplo-TCSH (1-4,10).
O ilustrare schematică a evenimentelor legate de administrarea de ciclofosfamidă post-TCSH haploidentic (haplo-TCSH-PTCy) este prezentată în fig. 2.
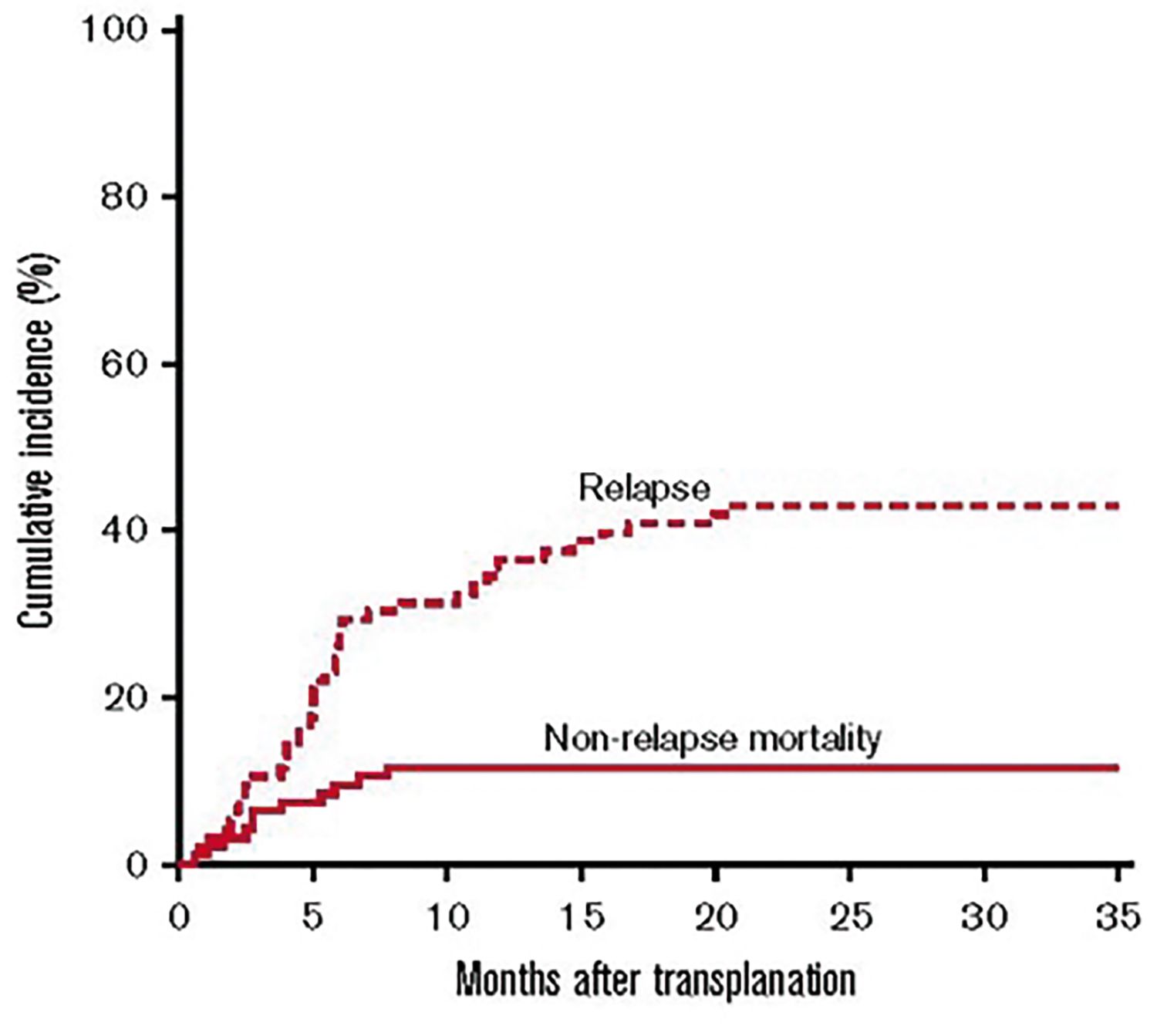
H.J. et al, 2020 (19)
Comparativ cu TCSH înrudit HLA-identic, care este în continuare „standardul de aur” în practica transplantului medular, se constată că post-haplo-TCSH, limfocitele T CD4 sunt mai reduse numeric în ziua 90, dar ajung la niveluri similare după un an. Limfocitele T CD8 sunt mai scăzute în ziua 30, dar ajung la valori superioare celor iniţiale în ziua 90. Limfocitele B și limfocitele NK și monocitele evoluează în mod asemănător.
Haplo-TCSH-PTCy se dovedește foarte eficace în eliminarea limfocitelor T aloreactive ale donatorului, reducând astfel incidenţa și severitatea BGcG precum și mortalitatea precoce legată de procedură, dar se asociază cu o refacere întârziată a sistemului imun, ceea ce ar explica o frecvenţă mai mare a infecţiilor cu citomegalovirus.
Aplicarea la om s-a făcut în baza unui protocol care a cuprins iniţial un regim de condiţionare non-mieloablativ (administrat înainte de introducerea celulelor donatorului nedepletizate de limfocitele T) prezentat în fig. 3.
Fig. 3. Protocolul aplicat inițial pentru haplo-TCSH de către colectivul de la Universitatea Johns Hopkins. Reprodus după Elmariah H., Fuchs J.E., 2018 (5)
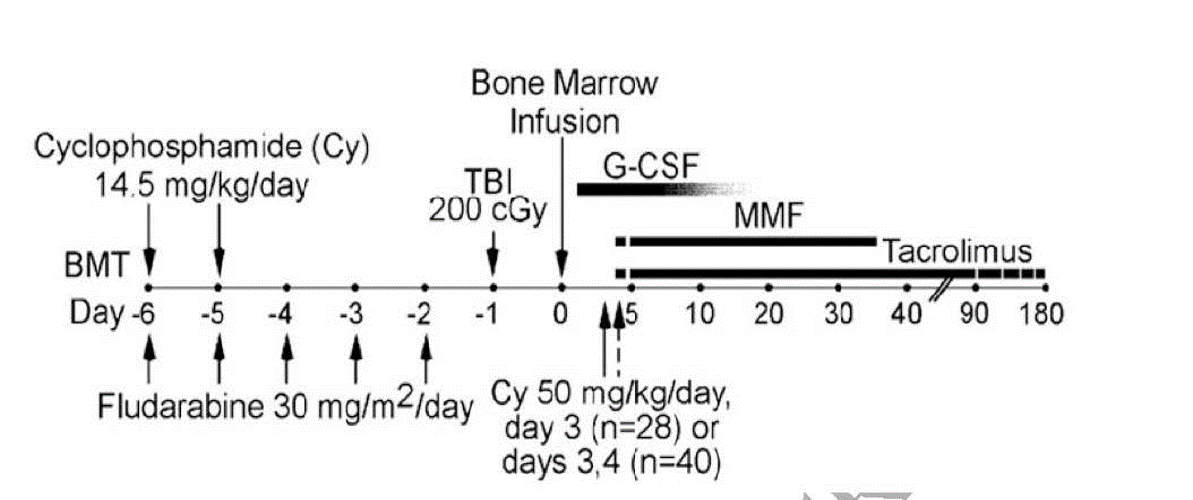
Tratamentul imunosupresor posttransplant a constat din inhibitori de calcineurină și micofenolat mofetil. După obţinerea unor rezultate promiţătoare cu regimuri de condiţionare nonmieloablative, mai multe grupuri au aplicat și regimuri mai intense mieloablative, în scopul reducerii procentului de recăderi ale bolii hematologice (1,3,4,12), cu menţiunea unor precauţii aparte în cazul aplicării acestora la pacienţii ≥55 de ani (7).
Prin introducerea PTCy în procedura de TCSH haploidentic a devenit posibilă menţinerea conţinutului normal de limfocite T în cadrul grefei. Acest lucru a permis, prin efectul lor de grefă-contra-celulă tumorală, o utilizare mai largă a regimurilor de condiţionare nonmieloablative, ceea ce a făcut posibilă o creștere semnificativă a numărului și vârstei pacienţilor care pot beneficia de TCSH. PTCy a determinat o reducere a incidenţei respingerii grefei și a BGcG, cu ameliorări semnificative ale mortalităţii nelegate de procedură.
Toate studiile ulterioare au confirmat eficacitatea, siguranţa și aplicabilitatea metodologiei de utilizare a PTCy, care a făcut din transplantul haploidentic o procedură acceptată pe plan internaţional, cu rezultate similare celor obţinute cu transplantul medular de la donatori HLA-compatibili, aplicabilă atât la pacienţii adulţi, cât și la cei pediatrici (11).
Bibliografie
1. Bashey A, Solomon SR. T-cell replete haploidentical donor transplantation using post-transplant CY: an emerging standard-of-care option for patients who lack an HLA-identical sibling donor. Bone Marrow Transplantation (2014) 49, 999
2. Luznik L. et al. HLA-Haploidentical bone marrow transplantation for hematologic malignancies using nonmyeloablative conditioning and high-dose, posttransplantation cyclophosphamide. Biol Blood Marrow Transplant. 2008;14(6):641, doi:10.1016/j.bbmt.2008.03.005.
3. Bayraktar U.D., Champlin R.E., Ciurea S.O. Progress in haploidentical stem cell transplantation. Biol Blood Marrow Transplant. 2012; 18(3): 372. doi:10.1016/j.bbmt.2011.08.001.
4. Ciurea S.O. et al. Improved early outcomes using a T cell replete graft compared with T cell depleted haploidentical hematopoietic stem cell transplantation. Biol Blood Marrow Transplant. 2012;18(12): 1835. doi:10.1016/j.bbmt.2012.07.003.
5. Elmariah H., Fuchs E.J. Post-transplantation cyclophosphamide to facilitate HLA-haploidentical hematopoietic cell transplantation: mechanisms and results. Seminars in Hematology 2018, doi.org/10.1053/j.seminhematol.2018.09.002
6. Tanase A. et al. Haploidentical donors: Can faster transplantation be life-saving for patients with advanced disease? Acta Haematol 2016;135:211
7. Tănase A. et al. First successful haploidentical stem cell transplantation in Romania. Rom. J. Intern. Med., 2016, DOI: 10.1515/rjim-2016-0021
8. Dubois V. et al. Greffe de cellules souches hématopoïétiques haplo-identiques avec cyclophosphamide en post-greffe : comment choisir le meilleur donneur en 2019 ? Recommandations de la Société francophone de greffe de moelle et de thérapie cellulaire (SFGM-TC). Bull Cancer 2020,107:S72–S84
9. Pitombeira de Lacerda M. et al. Human Leukocyte Antigen–haploidentical transplantation for relapsed/refractory Hodgkin lymphoma: A multicenter analysis. Biol Blood Marrow Transplant 2017,23:691
10. McCurdy S.R, Luznik L. Immune reconstitution after T-cell replete HLA-haploidentical transplantation. Seminars in Hematology 2019,56:221
11. Kongtim P., Ciurea S.O. Who is the best donor for haploidentical stem cell transplantation? Seminars in Hematology 2019,56(3):194, doi.org/10.1053/j.seminhematol.2018.08.003
12. Shabbir-Moosajee M. et al. An overview of conditioning regimens for haploidentical stem cell transplantation with post-transplantation cyclophosphamide. American Journal of Hematology 2015,90( 6):541. doi:10.1002/ajh.23995.
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe