Sindromul
Prader-Willi (SPW) este o boală genetică rară (cu prevalenţa de 1:10.000 –
1:30.000 nou-născuţi), multisistemică, cu mare variabilitate din punct de
vedere genetic, clinic şi endocrinologic. Afectează ambele sexe, toate rasele şi
reprezintă cea mai frecventă formă de obezitate sindromică.
În 1887, John Langdon
Down a descris primul pacient cu sindromul Prader-Willi – o adolescentă cu
deficienţe mintale, mică de statură, cu hipogonadism şi obezitate, dar a
atribuit aceste simptome obezităţii morbide. SPW a fost descris pentru prima
dată de medicii suedezi Andrea Prader, Alexis Labhart şi Heinrich Willi în
1956, pe baza caracteristicilor clinice prezente la nouă copii examinaţi.
Caracteristicile comune definite în raportul iniţial au inclus mâini şi
picioare mici, creştere şi structură constituţională anormală (statură mică şi
obezitate cu debut în copilărie), hipotonie la naştere, foame nesăţioasă,
obezitate extremă şi handicap intelectual.
Etiologie
Există
o serie de modificări genice importante pentru SPW. În etiologia acestui
sindrom sunt implicate mai multe gene, toate situate pe braţul lung al
cromozomului 15, în regiunea marcată 15q11-q13. Genele critice sunt de
etiologie paternă, cele provenite de la mamă corespunzătoare acestei regiuni
sunt inactivate prin fenomenul de imprimare genomică. Există cel puţin trei
erori congenitale diferite care împiedică aceste gene să funcţioneze corespunzător,
având ca rezultat final sindromul Prader-Willi.
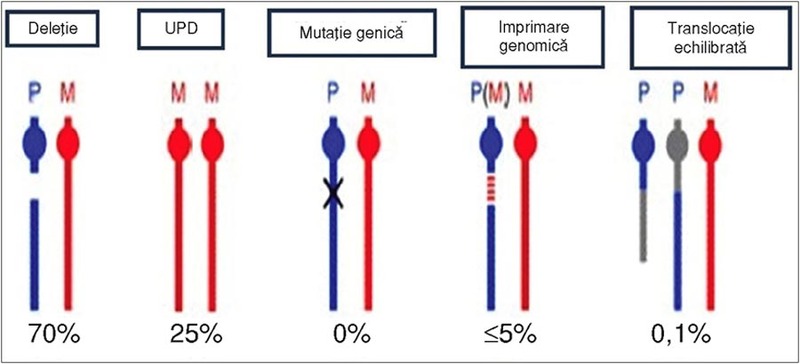
Astfel,
SPW este cauzat cel mai frecvent de deleţia sau translocaţia unei gene de la
nivelul braţului proximal al cromozomului 15 patern (P) – 70% din cazuri – sau
disomia uniparentală (UPD) maternă a cromozomului 15 (M, ambii cromozomi 15 ai
copilului sunt de origine maternă) - 25% din cazuri.
Aceste
modificări genice apar aleatoriu, izolat, pacieţii neprezentând istoric
familial de boală.
Tabloul clinic
Manifestările clinice sunt complexe, SPW determinând modificări
fenotipice variate, astfel încât abordarea pacienţilor necesită o echipă
multidisciplinară.
Boala este vizibilă din primele zile de viaţă, nou-născuţii sunt mici
pentru vârsta gestaţională, cu hipotonie marcată. Hipotonia este de origine
centrală, studiul biopsiei musculare având rezultate normale, şi se atenuează
cu înaintarea în vârstă, dar este reziduală şi la adulţi. Multiple studii de
specialitate au raportat o greutate la naştere a fătului cu sindrom
Prader-Willi mai scăzută decât media în populaţia generală (2.945 ± 570 g la băieţi
şi 2.782 ± 594 g la fetiţe), contrastând cu lungimea la naştere în parametri
normali (50,2 ± 2,8 cm la băieţi şi 48,9 ± 3,3 cm la fetiţe).
Alte
manifestări includ:
– În perioada
neonatală şi de sugar: supt dificil (adesea
necesitând alimentaţie enterală), plâns slab, hipoplazia organelor genitale
(hipoplazia clitorisului sau scrotului, criptorhidie), creştere deficitară.
Activitatea motorie se îmbunătăţeşte, dar dezvoltarea motorie generală este
întârziată la mai mult de 90% din pacienţi comparativ cu sugarii normali.
Dificultăţile limbajului articulat şi expresiv conduc la întârzieri de limbaj şi
voce piţigăiată. Este foarte importantă recunoaşterea precoce a bolii: mişcările
fetale reduse pot ridica suspiciunea dezvoltării unui produs de concepţie cu
sindrom Prader-Willi; la fel de importantă este recunoaşterea sindromului de
neonatolog sau pediatru.
întârzieri de limbaj şi
voce piţigăiată. Este foarte importantă recunoaşterea precoce a bolii: mişcările
fetale reduse pot ridica suspiciunea dezvoltării unui produs de concepţie cu
sindrom Prader-Willi; la fel de importantă este recunoaşterea sindromului de
neonatolog sau pediatru.
– În
perioada copilăriei: creşterea poftei de
mâncare (hiperfagie) şi apariţia obezităţii, care poate deveni morbidă în lipsa
unui management corect, deficit statural, tulburări de somn mergând până la
narcolepsie, tulburări de comportament (isterie, încăpăţânare), dizabilităţi
cognitive, retard mintal. Testele efectuate la pacienţii cu SPW au evaluat
media coeficientului de inteligenţă la 60–70, plasând bolnavii în categoria
retard mintal uşor, dar aproximativ 40% au intelectul la limita normalului şi
20% au retard mintal moderat. Totuşi, indiferent de nivelul intelectului, aceşti
pacienţi au dificultăţi de învăţare, şi chiar dacă prezintă afectarea
limbajului, capacitatea de vorbire este menţinută.
Hiperfagia
este de cauză hipotalamică, prin lipsa saţietăţii. Rolul grelinei în cadrul
deficitului de saţietate este foarte mult studiat la ora actuală, nivelul
acesteia în sânge fiind raportat de 4,5 ori mai ridicat la pacienţii cu SPW. O
scădere a nivelului sanguin al grelinei
a fost observată la administrarea de octreotid, dar foarte puţin postprandial,
astfel că alte studii au concluzionat că nivelul acesteia à jeun şi postprandial sunt parţial influenţate de hipoinsulinemia
corelată sindromului.
– În
adolescenţă şi perioada de adult: statură scundă în lipsa tratamentului cu
hormon somatotrop, hipogonadism; inactivitatea asociată cu obezitatea conduce
la anomalii ale somnului şi respiraţiei – cum sunt hipoventilaţia, saturaţia scăzută
în oxigen, apneea centrală şi obstructivă –, diabet zaharat
non-insulinodependent, cu o vârstă de debut de aproximativ 20 de ani (25% din
cazuri), comportament caracteristic (70–90%) cu crize de isterie, încăpăţânare,
atitudine manipulatoare şi tendinţe obsesiv-compulsive.
Pacienţii
cu SPW prezintă un fenotip particular caracterizat prin diametru bifrontal
îngustat, ochi migdalaţi, salivă vâscoasă, comisuri bucale coborâte, gură mică,
buza superioară subţire. O treime din indivizi prezintă hipopigmentarea părului,
ochilor şi a pielii din cauza unui albinism tirozinază-pozitiv.
Diagnosticul pozitiv
Diagnosticul
clinic
se stabileşte pe baza unui scor clinic de diagnostic care presupune evaluarea
riguroasă a pacienţilor pe baza unor criterii minore şi majore (tabelul 1).
Acumularea
unui scor diagnostic egal sau mai mare de 5 puncte (minimum patru criterii
majore) sub vârsta de trei ani, egal sau mai mare de 8 peste trei ani (cinci
criterii majore) indică SPW.
Testele
genetice sunt
singurele metode de certitudine care stabilesc diagnosticul pozitiv.
Analizele
citogenetice includ analiza cromozomială prin bandare convenţională şi de înaltă
rezoluţie, precum şi analiza citogenetică-moleculară FISH (hibridizare in situ cu fluorescenţă). Acestea îşi găsesc
utilitatea diagnostică datorită faptului că aproximativ 70% din  pacienţii cu
SPW prezintă deleţia cromozomului 15 patern implicând regiunea 15q11.2-q13,
care poate fi identificată folosind tehnica de bandare de înaltă rezoluţie sau
tehnica FISH.
pacienţii cu
SPW prezintă deleţia cromozomului 15 patern implicând regiunea 15q11.2-q13,
care poate fi identificată folosind tehnica de bandare de înaltă rezoluţie sau
tehnica FISH.
Analizele
moleculare implică studiul ADN-ului genomic al pacienţilor, până la ora actuală
fiind dezvoltate multiple metode de analiză. Deoarece aproximativ 99% din
pacienţii cu SPW prezintă o modificare în metilarea amprentării parentale,
specifică în regiunea critică Prader-Willi (PWCR), analiza metilării este
importantă pentru diagnostic. Testul metilării va oferi informaţii despre
expresia genelor paterne din regiunea 15q11-q13. În majoritatea laboratoarelor
este folosită analiza MS-PCR (methylation-specific
polymerase chain reaction) cu primeri parentali specifici (sensibili la
metilare) care amplifică exonul 1 al genei SNRPN (small nuclear ribonucleoprotein-associated protein N). O metodă
screening rapidă de detectare este reprezentată de MS-MA (methylation-specific melting analysis); o altă metodă de
diagnostic molecular este MS-MLPA (methylation-specific
multiplex ligation-dependent probe amplification). UPD poate fi detectată
prin studii ale disomiei care se bazează pe analiza markerilor microsateliţi.
Strategia de testare a sindromului
presupune două moduri de abordare:
–
Dacă individul îndeplineşte criteriile clinice ale sindromului se poate face
prima dată testul metilării.
–
Dacă SPW este unul din diagnosticele posibile, ar trebui să se efectueze iniţial
analiza FISH pentru identificarea deleţiei 15q11.2-q13. Dacă nu este
identificată deleţia şi nici altă anomalie citogenetică, trebuie efectuat testul
metilării. Dacă este posibilă, trebuie făcută şi analiza mutaţiei.
Pentru
fiecare grup de vârstă se definesc criteriile clinice esenţiale pentru indicaţia
de efectuare a testelor genetice (tabelul 2)
Diagnosticul diferenţial
Diagnosticul
diferenţial al SPW în perioada de nou-născut include principalele afecţiuni
care prezintă hipotonie, în special bolile neuromusculare centrale şi
periferice: sepsisul neonatal, afectarea neuronală, distrofia congenitală
miotonică tipul 1, câteva miopatii, sindromul Angelman, sindromul X fragil,
sindromul Rett.
Ulterior,
în evoluţie, întârzierea dezvoltării/retardul mintal şi obezitatea cu sau fără
hipogonadism impun diagnosticul diferenţial cu următoarele afecţiuni: disomia
uniparentală a cromozomului 14, osteodistrofia Albright, sindromul
Biedl-Bardet, sindromul Cohen, sindromul Borjeson-Forssman-Lehmann, sindromul
Alström. Şi sindromul Angelman, sindromul X fragil, sindromul Down pot fi luate
în discuţie pentru diagnosticul diferenţial. Craniofaringiomul şi rezultatele
în tratamentul său deţin cele mai multe semne fenotipice care se suprapun pe
sindromul Prader-Willi. De asemenea, afectarea hipotalamică cauzată de diferite
accidente, tumori sau complicaţii chirurgicale poate mima aspectele
endocrinologice ale SPW. Diagnosticul diferenţial se face prin testul metilării.
De asemenea, obezitatea familială trebuie exclusă prin ancheta familială.
Tratamentul
Tratamentul este simptomatic şi presupune o
abordare multidisciplinară. Acesta vizează corectarea obezităţii (dietă, exerciţii
fizice zilnice, monitorizarea greutăţii) şi prevenirea apariţiei complicaţiilor
cardiovasculare şi respiratorii cauzate de excesul ponderal, corectarea
osteoporozei (terapia cu calciu), a tulburărilor de somn, supraveghere
neuro-psihiatrică pentru tulburările de comportament şi limbaj. Terapia
comportamentală este mai degrabă un management corect decât un tratament al
crizelor comportamentale, care presupune pentru fiecare caz în parte
identificarea factorilor predispozanţi, precipitanţi sau care menţin
comportamentul respectiv. Intervenţiile se bazează pe strategii care minimizează
frecvenţa comportamentelor şi le administrează când apar. Astfel, familiile
necesită suport din partea psihologilor şi a altor persoane calificate pentru
un management corect al crizelor temperamentale.
La pubertate este necesară terapie hormonală
de substituţie cu hormoni steroizi pentru sexualizare secundară corespunzătoare,
dar şi din cauza densităţii minerale osoase scăzute care predispune la
fracturi. Nu există la ora actuală protocoale bine stabilite privind terapia  cu
hormoni sexuali, dar nivelul estrogenilor şi testosteronului, precum şi
densitatea minerală osoasă trebuie evaluate anual pe perioada adolescenţei şi
maturităţii.
cu
hormoni sexuali, dar nivelul estrogenilor şi testosteronului, precum şi
densitatea minerală osoasă trebuie evaluate anual pe perioada adolescenţei şi
maturităţii.
Un
aspect important îl constituie instituirea terapiei cu hormon somatotrop pentru
creşterea înălţimii şi totodată reducerea masei corporale. Statura scundă a
pacienţilor este cauzată de deficitul de hormon de creştere şi de IGF-1 (insulin-like growth factor 1), astfel
încât fără intervenţie, înălţimea maximă la care ajung este de 155 cm pentru băieţi
şi 148 cm la fete. Această terapie este larg utilizată la ora actuală la copii
cu sindrom Prader-Willi şi s-a dovedit că îmbunătăţeşte talia, masa musculară,
dismorfia facială, precum şi dimensiunea mâinilor şi picioarelor. De asemenea,
funcţia respiratorie este îmbunătăţită. Aceasta se administrează de obicei
seara, injectabil subcutanat în doza recomandată de 0,2 mg/kgc/zi în cazul
copiilor, 0,15–0,3 mg/kgc/zi la adulţi, putând fi crescută progresiv, cu câte
0,2 mg/zi până la o doză maximă de 1 mg/zi, în funcţie de toleranţa individuală
şi pentru a menţine nivelul de IGF-1 în limite normale pentru vârstă şi sex.
Chiar dacă beneficiile terapiei cu hormon de creştere sunt de necontestat, trebuie
luate anumite precauţii la iniţierea terapiei şi trebuie efectuată o evaluare
completă a pacientului, deoarece au fost raportate decese neaşteptate după
începerea tratamentului. Dintre complicaţiile acestei terapii, menţionăm apariţia
rezistenţei la insulină şi a diabetului zaharat tip 2, a complicaţiilor
cardiorespiratorii, apneei de somn.
Terapia
cu hormon somatotrop nu este indicată în cazuri de: hipersensibilitate la
substanţa activă, existenţă a unei tumori intracraniene sau afecţiuni acute în
stadiu critic. De asemenea, se recomandă întreruperea tratamentului în caz de
apariţie a efectelor adverse menţionate, neoplasmelor sau tumorilor
intracraniene.
Pentru
includerea sau excluderea pacienţilor de la tratamentul cu somatotropin sunt
elaborate criterii precise de includere sau de excludere.
Criterii de includere
pentru copilul peste trei ani:
1. Confirmarea diagnosticului prin teste
genetice sau criterii clinice;
2. Talia ≤–2 DS (deviaţia standard), sau
viteza de creştere în ultimul an <2 DS, sau în ultimii doi ani <1,5 DS
(viteza de creştere să fie măsurată de două ori/an);
3. IMC să nu fie cu >3 DS faţă de valorile normale pentru vârstă şi sex;
4. Fără prezenţa apneei de somn obstructivă
severă (trebuie documentată);
5. Fără DZ tip 1. Dacă este prezent DZ tip
2, glicemia trebuie normalizată înainte de începerea tratamentului;
6. Examen IRM/CT cerebral în limite normale.
Criterii
de excludere din tratament:
1. Vârsta ososasă (VO) >14 ani la fete şi
>16 ani la băieţi;
2. Viteza de creştere <2 cm/ultimele şase
luni la doza maximă admisă pentru tratament;
3. Creşterea DS al IMC cu 0,5 în timpul
terapiei raportat la valoarea pentru vârstă şi sex;
4. Apariţia DZ tip I;
5. Dacă apare apnee obstructivă, până la
rezolvarea acesteia;
6. Valori ale IGF-1 repetat crescute peste
limita superioară a normalului raportat la vârstă şi sex (două determinări).
Pentru pacienţii aflaţi în tratament cu
hormon de creştere, fişa de urmărire va cuprinde: talia, DS; greutatea, DS;
IMC, DS; VO – anual până la 12 ani şi la şase luni după 12 ani; IGF-1 – o dată
la şase luni; HbA1c – o dată la şase luni; polisomnografie – o dată la şase luni; evaluarea funcţiei
tiroidiene – o dată la şase luni; HLG, VSH.
Pacienţii care îndeplinesc criteriile pentru
terapia cu hormon de creştere pot obţine acest tratament prin serviciile
medicale care dispensarizează pacientul (pediatrie, genetică, endocrinologie),
el fiind asigurat prin Programul naţional de sănătate pentru bolile rare.
Terapia suportivă de grup este binevenită
pentru adulţi, dar trebuie iniţiată mai precoce. Trebuie avută în vedere
prevenirea complicaţiilor, astfel prin controlul greutăţii se poate face
prevenirea diabetului zaharat, iar osteoporoza se previne prin administrare de
calciu. De asemenea, odată cu prevenirea cauzelor mortalităţii precoce, speranţa
de viată a pacienţilor cu SPW a crescut, astfel încât trebuie să existe o echipă
multidisciplinară pentru managementul adulţilor.
Speranţa de viaţă
Speranţa de viaţă a pacienţilor cu boli rare
este semnificativ redusă şi mulţi au dizabilităţi care devin sursă de
discriminare şi reduc sau distrug orice oportunităţi educaţionale, profesionale
sau sociale. Un diagnostic corect şi precoce însoţit de un sfat genetic adecvat
permit evitarea recurenţei bolii în familie şi profilaxia ei, deci o scădere
semnificativă a costurilor asupra sistemului sanitar, iar în plan familial şi
social, evitarea unei noi drame.
În
cazul SPW, o mare parte din pacienţi ajung la vârsta adultă, obezitatea
reprezentând principala cauză de morbiditate şi mortalitate. Complicaţii precum
afectarea cardiorespiratorie, apneea obstructivă de somn, au fost cel mai
frecvent incriminate ca răspunzătoare pentru moartea subită în SPW.
Reproducerea la pacienţii cu SPW este rară, iar şansele de a avea un copil
afectat sunt de 50% (dacă tatăl este bolnav).
Sfatul genetic
Sfatul genetic este indicat pentru identificarea purtătorilor sănătoşi ai mutaţiei,
precum şi pentru consilierea părinţilor în vederea unei noi sarcini.
Pentru estimarea riscului de recurenţă, dacă
modelul de metilare este caracteristic moştenit doar matern, trebuie determinat
mecanismul cauzator (deleţie, UPD sau mutaţie a amprentării) pentru a putea
acorda un sfat genetic adecvat. Analiza FISH este prima tehnică ce ar trebui
efectuată ulterior metilării pozitive pentru identificarea deleţiei
15q11.2-q13. Concomitent trebuie efectuată analiza citogenetică convenţională,
care permite identificarea translocaţiilor sau a altor anomalii implicând
cromozomul 15. Dacă aceste analize citogenetice sunt negative, se va efectua
studiul disomiei, care presupune probe de sânge de la ambii părinţi. Dacă nu
este detectată nici disomia, se presupune un defect al amprentării a cărui
testare se poate efectua în puţine laboratoare. Totuşi, aceşti pacienţi având
un defect al centrului de amprentare sunt cei cu un risc semnificativ pentru
recurenţă.
Pentru sarcinile cu risc mai ales familial,
dar şi posibil estimat ecografic, se poate oferi diagnostic antenatal prin
analize genetice, fiind posibilă identificarea tuturor mecanismelor patogenice
descrise în clasele moleculare ale regiunii 15q11.2-q13 cauzatoare de SPW.
Între săptămânile 10 şi 12 de sarcină se pot preleva vilozităţile coriale, iar
între săptămânile 15 şi 18 i.u. se poate face puncţie de lichid amniotic. Se
poate efectua analiza FISH din celulele fetale prelevate sau se extrage ADN din
celule fetale şi se efectuează analiza metilării, cu atenţie asupra unor
markeri care pot fi în mod normal hipometilaţi într-o perioadă incipientă de
dezvoltare (vilozităţi coriale).
Situaţia pacienţilor
cu SPW în România
Deşi este o boală rară, SPW este relativ
bine cunoscut în presa românească, datorită Asociaţiei Prader Willi România (APWR), o emblemă a intervenţiei asociaţiilor
de pacienţi în politicile legate de bolile rare în România. Centrul NoRo, creat
de APWR la Zalău, printr-un proiect româno-norvegian, oferă pacienţilor cu boli
rare şi familiilor lor posibilităţi de informare, recuperare, instruire,
întâlniri cu specialiştii.
Afecţiunea este cunoscută şi în rândul
specialiştilor, ea făcând obiectul unui proiect naţional de cercetare –
„Corelarea aspectelor clinice, genetice şi epigenetice în înţelegerea
etiologiei bolilor genomice Prader-Willi/Angelman: model de abordare
multidisciplinară a bolilor rare în România“ – cu opt parteneri din cinci
centre universitare din ţară.
O mai bună
cunoaştere şi înţelegere a bolii de medicii de familie, pediatri, neonatologi,
endocrinologi va duce la un diagnostic precoce, la informarea părinţilor privind
măsurile dietetice necesare şi astfel s-ar evita instalarea obezităţii severe şi
a celorlalte complicaţii majore.
|
Tabelul
1. Criteriile de diagnostic ale lui Holm (1993)
Criterii
majore (1 criteriu=1 punct)
1. ‑Hipotonie în perioada de nou-născut şi
sugar cu supt deficitar, care scade în intensitate
cu vârsta;
2. ‑Dificultăţi de alimentare şi creştere în
greutate deficitară în perioada de sugar,necesitând alimentare asistată;
3. ‑Debutul creşterii bruşte în greutate
între vârsta de 12 luni şi 6 ani, determinând în general obezitate centrală;
4. Hiperfagie;
5. ‑Trăsături faciale caracteristice:
dolicocefalie în perioada de sugar, diametrul bifrontal îngust, fante palpebrale
migdalate, gură mică cu buză superioară subţire, comisuri bucale coborâte (mai
mult de trei);
6. ‑Hipogonadism, dependent de vârstă şi sex,
manifestat astfel (oricare din elemente):
• Hipoplazie
genitală: labii mici şi clitorisul de dimensiuni reduse la fetiţe, scrot
hipoplazic, micropenis şi criptorhidie la băieţi;
• Pubertate
întârziată (după 16 ani) şi incomplet instalată, infertilitate;
7. ‑Dezvoltare întârziată/retard mintal uşor
sau moderat/dificultăţi de învăţare.
Criterii minore (1
criteriu=1/2 punct)
1. Mişcări fetale reduse şi letargie infantilă
care se îmbunătăţesc cu vârsta;
2. ‑Comportament specific, incluzând crize
istericale, reacţii violente, încăpăţânare,
atitudine manipulatoare şi tendinţe obsesiv-compulsive, opoziţie, rigiditate, posesivitate, furt, minciună (cel puţin
cinci);
3. Perturbări ale somnului/apnee de somn;
4. Statură mai scundă decât membrii familiei
până la vârsta de 15 ani;
5. Hipopigmentarea pielii;
6. Mâini şi picioare mici în comparaţie cu înălţimea
vârstei;
7. Mâini înguste, lipsind incizura ulnară;
8. Strabism convergent şi miopie;
9. Salivă vâscoasă;
10. Dificultăţi în articularea cuvintelor;
11. Ciupire compulsivă a pielii.
Semne
• Prag crescut la durere;
• Reflex de vomă diminuat;
• Scolioză sau cifoză;
• Adrenarhă precoce;
• Osteoporoză;
• Abilităţi excesive
de a rezolva puzzle;
• Evaluări
neuromusculare normale (biopsie musculară, EMG) |
 întârzieri de limbaj şi
voce piţigăiată. Este foarte importantă recunoaşterea precoce a bolii: mişcările
fetale reduse pot ridica suspiciunea dezvoltării unui produs de concepţie cu
sindrom Prader-Willi; la fel de importantă este recunoaşterea sindromului de
neonatolog sau pediatru.
întârzieri de limbaj şi
voce piţigăiată. Este foarte importantă recunoaşterea precoce a bolii: mişcările
fetale reduse pot ridica suspiciunea dezvoltării unui produs de concepţie cu
sindrom Prader-Willi; la fel de importantă este recunoaşterea sindromului de
neonatolog sau pediatru. pacienţii cu
SPW prezintă deleţia cromozomului 15 patern implicând regiunea 15q11.2-q13,
care poate fi identificată folosind tehnica de bandare de înaltă rezoluţie sau
tehnica FISH.
pacienţii cu
SPW prezintă deleţia cromozomului 15 patern implicând regiunea 15q11.2-q13,
care poate fi identificată folosind tehnica de bandare de înaltă rezoluţie sau
tehnica FISH. cu
hormoni sexuali, dar nivelul estrogenilor şi testosteronului, precum şi
densitatea minerală osoasă trebuie evaluate anual pe perioada adolescenţei şi
maturităţii.
cu
hormoni sexuali, dar nivelul estrogenilor şi testosteronului, precum şi
densitatea minerală osoasă trebuie evaluate anual pe perioada adolescenţei şi
maturităţii.