Spre deosebire de populaţia generală, pacienţii cu boli autoimune au un risc crescut de a dezvolta multiple comorbidităţi. Dintre acestea, comorbidităţile cardiovasculare sunt cele mai frecvente și au cel mai mare impact asupra ratei de morbiditate și mortalitate.
Mult timp, manifestările cardiovasculare ale bolilor autoimune sistemice au fost insuficient cunoscute, în ciuda dovezilor clare că afectarea extraarticulară la acești pacienţi, inclusiv cea cardiovasculară, determină o creștere semnificativă a riscului de deces. Astfel, atenţia a fost îndreptată către „actorii” principali: articulaţiile (în poliartrita reumatoidă, PR), pielea, rinichiul și plămânul (în scleroza sistemică), rinichiul și creierul (în lupusul eritematos sistemic, LES). În ultima perioadă, însă, manifestările cardiovasculare ale bolilor autoimune au devenit un subiect de actualitate în literatura de specialitate, cu atât mai mult cu cât aceste manifestări pot constitui tabloul iniţial întâlnit la astfel de pacienţi. Se impune, astfel, recunoașterea factorilor de risc cardiovascular, diagnosticul precoce al complicaţiilor cardiovasculare, precum și managementul adecvat al acestora, cu scopul de a îmbunătăţi prognosticul pe termen lung al acestor pacienţi.
Ratele standardizate de mortalitate la pacienţii cu boală autoimună sistemică (BAS) sunt semnificativ mai mari în comparaţie cu cele întâlnite în populaţia generală (1,3-2,3 în PR, 1,6-1,9 în spondilita anchilozantă), acest lucru fiind determinat în principal de boala cardiovasculară. Un studiu efectuat pe un grup de pacienţi cu BAS care au fost monitorizaţi periodic a arătat că, în ciuda unui scor de activitate a bolii scăzut, prevalenţa bolii cardiovasculare în rândul acestor pacienţi rămâne crescută, spre deosebire de populaţia fără BAS. O metaanaliză a arătat că mortalitatea prin boli cardiovasculare la pacienţii cu PR a fost cu 50% mai mare decât cea din rândul populaţiei generale. Boala cardiacă ischemică și accidentul vascular cerebral reprezintă principalii factori ce au dus la această creștere.
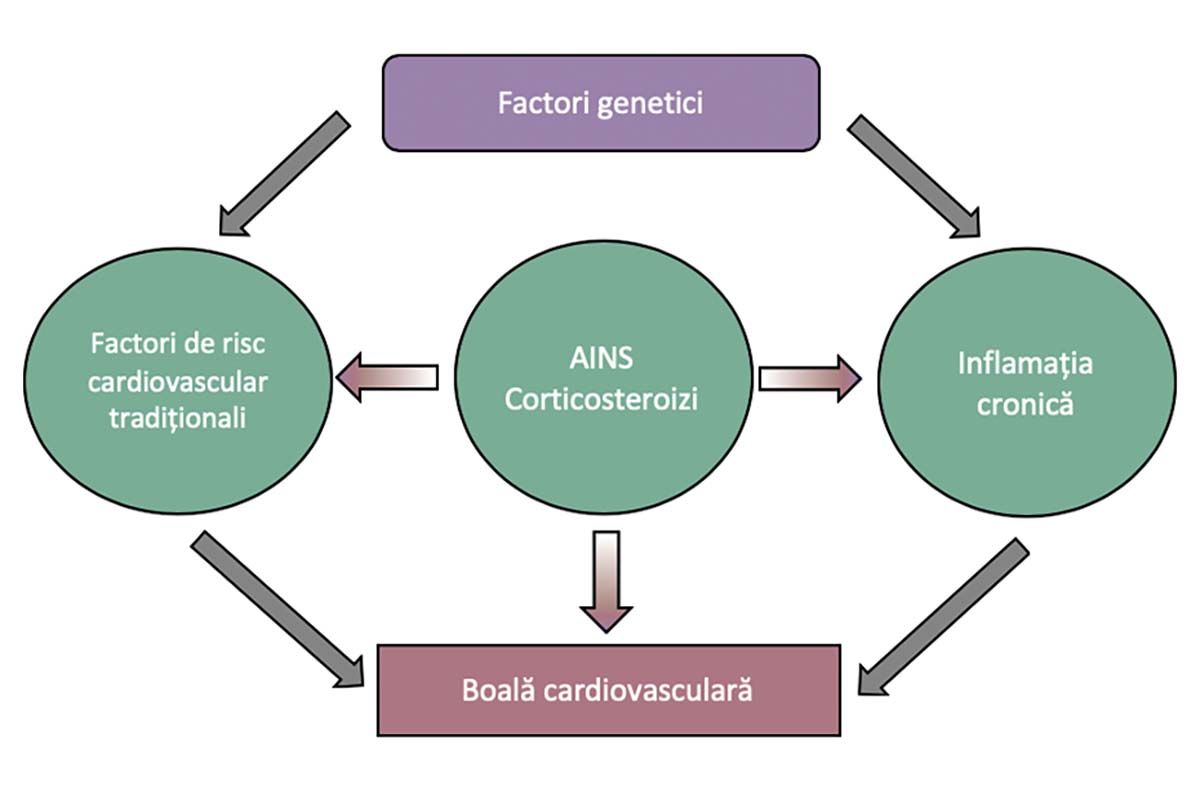
Printre factorii implicaţi în afectarea cardiovasculară din bolile autoimune se numără inflamaţia și ateroscleroza, factorii de risc cardiovascular tradiţionali, terapia cu antiinflamatoare nesteroidiene și corticosteroizi, factorii specifici tipului de boală autoimună și factorii genetici (fig. 1).
Există numeroase dovezi care indică faptul că inflamaţia este implicată în patogeneza aterosclerozei și a bolii cardiovasculare, citokine inflamatorii precum TNF, IL-6, IL-1 jucând un rol esenţial în dezvoltarea aterosclerozei la pacienţii cu BAS. Inflamaţia este implicată în toate etapele aterosclerozei, de la formarea plăcii de aterom la instabilitatea și, în final, ruptura acesteia, având o contribuţie importantă în dezvoltarea bolii cardiovasculare la pacienţii cu BAS.
Factorul reumatoid și anticorpii antinucleari sunt consideraţi factori de risc pentru infarctul miocardic, insuficienţa cardiacă congestivă și boala arterială periferică, chiar și la pacienţii fără artrită reumatoidă. Goodson et al au arătat faptul că pacienţii cu PR seropozitivă au un risc mai mare de deces prin boală cardiovasculară în comparaţie cu subiecţii seronegativi.
Antiinflamatoarele nesteroidiene (AINS, inclusiv coxibii), utilizate pe scară largă în bolile reumatice autoimune, au fost asociate cu un risc crescut de deces prin boală cardiovasculară. Cu toate acestea, un studiu longitudinal ce a inclus 17.320 de pacienţi cu artrită reumatoidă, care au fost monitorizaţi pe o perioadă de cinci ani, a arătat o creștere minimă a riscului cardiovascular, risc ce a fost mai mic decât cel întâlnit în populaţia generală.
Afectarea cardiacă la pacienţii cu BAS poate include toate structurile cardiace: pericardul, miocardul, aparatul valvular, sistemul excito-conductor, dar și vascularizaţia coronariană și pulmonară.
Patologia pericardului
Afectarea pericardului în BAS este des întâlnită, cel mai frecvent prezentându-se ca pericardită acută (sau recurentă) sau revărsat pericardic asimptomatic. În timp ce unii pacienţi pot prezenta semne și simptome tipice de pericardită (febră, durere toracică) sau de revărsat pericardic semnificativ hemodinamic (dispnee, fatigabilitate, hipotensiune arterială), mulţi pacienţi sunt în mod accidental diagnosticaţi cu afectare pericardică. Tabloul clinic poate debuta atât insidios, cât și brusc, cu progresie rapidă a bolii. Tamponada cardiacă și pericardita constrictivă sunt complicaţii rare.
Pericardita reprezintă cea mai frecventă manifestare cardiacă la pacienţii cu PR. Între 30 și 50% dintre pacienţii cu forme severe de PR au pericardită obiectivată fie prin ecocardiografie, fie la autopsie. Cu toate acestea, manifestările clinice de pericardită se întâlnesc la mai puţin de 10% dintre pacienţi. Cel mai frecvent, pericardita apare la pacienţii de sex masculin cu PR seropozitivă fiind însoţită și de alte manifestări extraarticulare.
Afecţiunea autoimună care în mod clasic se asociază cu tablou clinic de pericardită este LES. Simptome tipice precum febra, tahicardia, durerea toracică, ce se modifică cu poziţia, și frecătura pericardică pot fi întâlnite la 25% dintre pacienţii cu LES. Afectarea pericardică poate precede semnele clinice de LES. Revărsatul pericardic este cea mai frecventă modificare patologică ecocardiografică. Revărsatele pericardice masive complicate cu tamponadă cardiacă sunt rare în LES. De cele mai multe ori, pericardita însoţește perioadele de exacerbare a bolii și se poate asocia cu alte serozite (ascită, revărsat pleural). În majoritatea cazurilor, evoluţia este favorabilă, cu răspuns bun la AINS. Colchicina poate fi administrată pentru a reduce riscul de pericardită recurentă.
Afectarea pericardică cel mai frecvent întâlnită în scleroza sistemică este revărsatul pericardic asimptomatic. Au fost descrise în literatura de specialitate cazuri de pacienţi, ulterior diagnosticaţi cu scleroză sistemică, a căror primă manifestare a bolii a fost revărsatul pericardic masiv însoţit de tamponadă cardiacă. Sindromul lichidian pericardic este asociat frecvent cu hipertensiunea pulmonară și poate reprezenta forma de manifestare a hipertensiunii pulmonare la pacientul cu sclerodermie.
Patologia vasculară
Una dintre manifestările cardiovasculare ale PR este ateroscleroza precoce, care apare independent de factorii de risc cardiovascular clasici. Riscul cardiovascular scăzut al pacienţilor cu PR trataţi cu anti-TNF și metotrexat susţine ipoteza că ateroscleroza accelerată din PR este declanșată de inflamaţia cronică și nu de factorii de risc cardiovascular tradiţionali. Mai mult decât atât, numeroase studii au arătat dublarea riscului de infarct miocardic la pacienţii cu PR faţă de grupul control. Evaluarea disfuncţiei endoteliale, a indicelui intimă-medie carotidian și a plăcilor de aterom poate detecta prezenţa aterosclerozei într-un stadiu preclinic, înaintea apariţiei bolii clinic manifeste, permiţând astfel adoptarea unor măsuri de scădere a riscului cardiovascular la pacienţii cu PR.
Similiar pacienţilor cu PR, pacienţii cu LES prezintă ateroscleroză precoce și accelerată, secundară procesului inflamator. În plus, pacienţii cu anticorpi antinucleari și/sau antifosfolipidici pozitivi au un risc crescut de mortalitate prin boli cardiovasculare. Nivelul crescut de homocisteină la pacienţii cu LES reprezintă un factor de risc independent și semnificativ pentru accidentul vascular cerebral și tromboza arterială. Afectarea renală însoţită de proteinurie de rang nefrotic s-a asociat cu o incidenţă crescută a aterosclerozei carotidiene la pacienţii cu LES.
Scleroza sistemică este caracterizată de prezenţa anomaliilor microvasculare, cu ischemie secundară și activitate fibroblastică excesivă. Studii recente au arătat afectarea concomitentă a arterelor de calibru mare la pacienţii cu scleroză sistemică, secundar inflamaţiei sistemice cronice.
Într-o metaanaliză de studii observaţionale, Ungprasert et al au comparat riscul de boală coronariană la pacienţii cu spondilită anchilozantă faţă de grupul de control și au arătat că primii menţionaţi au avut un risc de 41 de ori mai mare de boală coronariană.
Bibliografie
1. Prasad M, Hermann J, Gabriel SE et al. Cardiorheumatology: Cardiac involvement in systemic rheumatic disease. Nat Rev Cardiol. 2015;12(3):168-76
2. Nurmohamed MT, Heslinga M, Kitas GD. Cardiovascular comorbidity in rheumatic diseases. Nat Rev Rheumatol. 2015;11(12):693-704
3. Matucci-Cerinic M, Seferović PM. Heart involvement in autoimmune rheumatic diseases: the “phantom of the opera”. Rheumatology. 2006;45(4):iv1–iv3
4. Agca R, Heslinga SC, van Halm VP, et al. Atherosclerotic cardiovascular disease in patients with chronic inflammatory joint disorders. Heart. 2016;102(10):790-795
5. Castañeda S, Martín-Martínez MA, Gonzalez-Juanatey C, et al. CARMA Project Collaborative Group. Cardiovascular morbidity and associated risk factors in Spanish patients with chronic inflammatory rheumatic diseases attending rheumatology clinics: baseline data of the CARMA Project. Semin Arthritis Rheum. 2015;44(6):618-26
6. Van den Hoek J, Roorda LD, Boshuizen HC, et al. Trend in and predictors for cardiovascular mortality in patients with rheumatoid arthritis over a period of 15 years: a prospective cohort study. Clin Exp Rheumatol. 2016;34(5):813-819
7. Aviña-Zubieta JA, Choi HK, Sadatsafavi M et al. Risk of cardiovascular mortality in patients with rheumatoid arthritis: a meta-analysis of observational studies. Arthritis Rheum. 2008;59(12):1690-7
8. Libby P, Ridker PM, Hansson GK. Progress and challenges in translating the biology of atherosclerosis. Nature. 2011;473:317-325
9. Libby P. Role of inflammation in atherosclerosis associated with rheumatoid arthritis. Am J Med. 2008;121(10 Suppl. 1):S21-31
10. de Groot L, Posthumus MD, Kallenberg CG, et al. Risk factors and early detection of atherosclerosis in rheumatoid arthritis. Eur J Clin Invest. 2010;40(9):835-842
11. Crowson CS, Nicola PJ, Maradit Kremers H, et al. How much of the increased incidence of heart failure in rheumatoid arthritis is attributable to traditional cardiovascular risk factors and ischemic heart disease? Arthritis Rheum. 2005;52:3039-3044
12. Liao KP, Solomon DH. Traditional cardiovascular risk factors, inflammation and cardiovascular risk in rheumatoid arthritis. Rheumatol (Oxford). 2013;52(1):45-52
13. Giles JT. Cardiovascular disease in rheumatoid arthritis: current perspectives on assessing and mitigating risk in clinical practice. Best Pract Res Clin Rheumatol. 2015;29(4-5):597-613
14. Liang KP, Kremers HM, Crowson CS, et al. Autoantibodies and the risk of cardiovascular events. J Rheumatol. 2009;36(11):2462-2469
15. Goodson NJ, Wiles NJ, Lunt M, et al. Mortality in early inflammatory polyarthritis: cardiovascular mortality is increased in seropositive patients. Arthritis Rheum. 2002;46(8):2010-2019
16. Trelle S, Reichenbach S, Wandel S, et al. Cardiovascular safety of non-steroidal anti-inflammatory drugs: network meta-analysis. BMJ. 2011;342:c7086
17. Lindhardsen J, Gislason GH, Jacobsen S, et al. Non-steroidal anti-inflammatory drugs and risk of cardiovascular disease in patients with rheumatoid arthritis: a nationwide cohort study. Ann Rheum Dis. 2014;73(8):1515-1521
18. Knockaert DC. Cardiac involvement in systemic inflammatory diseases. Eur Heart J. 2007;28(15):1797-1804
19. Kitas G, Banks MJ, Bacon PA. Cardiac involvement in rheumatoid disease. Clin. Med. (Lond.). 2001;1(1):18–21
20. Cojocaru M, Cojocaru IM, Silosi I, et al. Extra-articular manifestations in rheumatoid arthritis. Maedica. 2010;5(4):286–291
21. Coblyn JS, Weinblat ME. Rheumatic diseases and the 78 heart. In: Braunwald E, ed. Heart disease. 5th ed. Philadelphia: Saunders; 1997:1776-1783
22. Doria A, Iaccarino L, Sarzi-Puttini P, et al. Cardiac involvement in systemic lupus erythematosus. Lupus. 2005;14(9):683-686
23. Gowda R, Khan I, Sacchi T, et al. Scleroderma pericardial disease presented with a large pericardial effusion--a case report. Angiology. 2001;52(1):59-62
24. Peronato G, De Sandre P, Podswiadek M, et al. Tamponamento cardiaco come manifestazione di esordio della sclerosi sistemica progressiva (Cardiac tamponade preceding skin involvement in progressive systemic sclerosis). Reumatismo. 2002;54(3):257-260
25. Steen V. The heart in systemic sclerosis. Curr Rheumatol Rep. 2004;6:137-140
26. Villa-Forte A, Mandell BF. Cardiovascular disorders and rheumatic disease (Spanish). Rev. Esp. Cardiol. 2011;64(9):809–817
27. Zuily S, Regnault V, Selton-Suty C, et al. Increased risk for heart valve disease associated with antiphospholipid antibodies in patients with systemic lupus erythematosus: meta-analysis of echocardiographic studies. Circulation. 2011;124(2):215-224
28. Roldan C, Chavez J, Wiest P, et al. Aortic root disease and valve disease associated with ankylosing spondylitis. J Am Coll Cardiol. 1998;32(5):1397–1404
29. Nicola PJ, Maradit-Kremers H, Roger VL, et al. The risk of congestive heart failure in rheumatoid arthritis: a population-based study over 46 years. Arthritis Rheum. 2005;52(2):412-420
30. Ethayiem B, Pavitt S, Baxter P, et al. Coronary artery disease evaluation in rheumatoid arthritis (CADERA): study protocol for a randomized controlled trial. Trials. 2014;15:436
31. Roman MJ, Salmon JE. Cardiovascular manifestations of rheumatologic diseases. Circulation. 2007;116(20):2346–2355
32. Bulkley BH, Roberts WC. The heart in systemic lupus erythematosus and the changes induced in it by corticosteroid therapy. A study of 36 necropsy patients. Am J Med. 1975;58(2):243–264
33. Cho JH, Feldman M. Heterogeneity of autoimmune diseases: pathophysiologic insights from genetics and implications for new therapies. Nat Med. 2015;21(7):730–738
34. Yogasundaram H, Putko BN, Tien J, et al. Hydroxychloroquine-induced cardiomyopathy: case report, pathophysiology, diagnosis, and treatment. Can J Cardiol. 2014;30(12):1706–1715
35. Evrengul H, Dursunoglu D, Cobankara V, et al. Heart rate variability in patients with rheumatoid arthritis. Rheumatol Int. 2004;24(4):198–202
36. Seferović P, Ristić AD, Maksimović R, et al. Cardiac arrhythmias and conduction disturbances in autoimmune rheumatic diseases. Rheumatology (Oxford). 2006;45(4):iv39–iv42
37. Parnes E, Krasnosel’skii M, Tsurko VV, Striuk RI. Long-term prognosis in patients with rheumatoid arthritis depending on baseline variability of cardiac rhythm. Terapevticheskiiarkhiv. 2005;77:77–80
38. Teixeira RA, Borba EF, Pedrosa A, et al. Evidence for cardiac safety and antiarrhythmic potential of chloroquine in systemic lupus erythematosus. Europace. 2014;16(6):887–992
39. Kostis JB, Seibold JR, Turkevich D, et al. Prognostic importance of cardiac arrhythmias in systemic sclerosis. Am J Med. 1988;84(6):1007–1015
40. Bergfeldt L, Vallin H, Edhag O. Complete heart block in HLA B27 associated disease. Electrophysiological and clinical characteristics. Br Heart J. 1984;51(2):184–188
41. Thachil A, Christopher J, Sastry BK, et al. Monomorphic ventricular tachycardia and mediastinal adenopathy due to granulomatous infiltration in patients with preserved ventricular function. J Am Coll Cardiol. 2011;58(1):48-55
42. Salmon JE, Roman MJ. Subclinical atherosclerosis in rheumatoid arthritis and systemic lupus erythematosus. Am J Med. 2008;121(10 Suppl 1):S3–S8
43. Petri M, Roubenoff R, Dallal GE, et al. Plasma homocysteine as a risk factor for atherothrombotic events in systemic lupus erythematosus. Lancet. 1996;348(9035):1120–1124
44. Falaschi F, Ravelli A, Martignoni A, et al. Nephrotic-range proteinuria, the major risk factor for early atherosclerosis in juvenile-onset systemic lupus erythematosus. Arthritis Rheum. 2001;43(6):1405–1409
45. Ungprasert P, Srivali N, Kittanamongkolchai W. Risk of coronary artery disease in patients with ankylosing spondylitis: A systematic review and meta-analysis. Ann. Transl. Med. 2015;3(4):51
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe