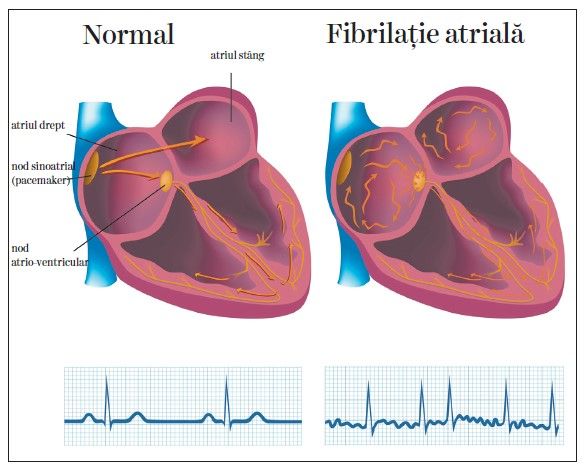
Tahicardiile prin macroreintrare atrială sunt caracterizate de activări prin reintrare în atriul drept sau stâng, în jurul unui obstacol cu diametru de câţiva centimetri, constând din structuri normale sau anormale.
dr. Istvan Neuhoff
Rata depolarizării atriale este de 240–320/min, cu variaţii mai mici de 2% din lungimea de ciclu, iar frecvenţa activării ventriculare este de obicei jumătate din ritmul atrial, în absenţa tratamentului cu antiaritmice sau a afectării nodului atrio-ventricular (1). Termenul de „flutter” se referă la un model al undelor atriale pe electrocardiogramă, cu absenţa intervalului izoelectric în cel puţin o derivaţie, oricare ar fi lungimea de ciclu.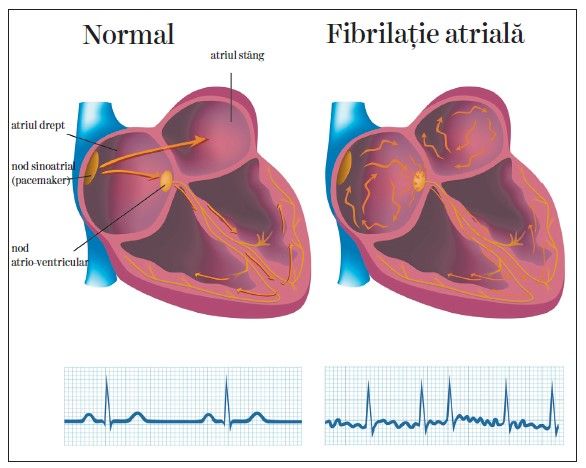
Deși există multiple clasificări care pot fi aplicate în cazul flutterelor atriale, cea mai comună și practică din punct de vedere clinic este clasificarea flutterului ca fiind „tipic” sau „atipic” pe baza caracteristicilor sale anatomice și electrofiziologice (1).
Flutterul tipic este o macroreintrare atrială dreaptă, dependentă de istmul cavo-tricuspidian, structură anatomică situată între vena cavă inferioară și inelul tricuspidian. Aceasta este și cea mai frecventă formă în cadrul macroreintrărilor atriale și reprezintă aproximativ 90% din toate tipurile de flutter. Secvenţa de depolarizare atrială se face antiorar (în sens craniocaudal la nivelul peretelui lateral al atriului drept și în sens caudocranial la nivelul septului interatrial) și mult mai rar orar (în cazul flutterului atrial tipic inversat) în jurul valvei tricuspide, care reprezintă bariera anatomică anterioară a circuitului de reintrare. Posterior, are ca bariere anatomice și/sau funcţionale crista terminalis cu prelungirea sa cu valva lui Eustachio până la ostiumul sinusului coronar, având o zonă critică, de conducere lentă, reprezentată de istmul cavo-tricuspidian (2, 3).
Flutterul atrial atipic este o macroreintrare al cărei circuit nu implică istmul cavo-tricuspidian. Poate apărea atât în atriul drept, cât și în cel stâng și reprezintă aproximativ 10% din flutterele atriale. Nu are caracteristici specifice pe electrocardiogramă. Flutterul atrial atipic este mai frecvent pericicatriceal și poate implica diferite structuri atriale ca substrat. Substratul poate fi identificat cu ajutorul tehnicilor de reconstrucţie tridimensională prin vizualizarea directă a frontului de depolarizare atrială și identificarea zonei lente a circuitului de reintrare.
Flutterul atrial este o aritmie relativ frecventă la populaţia adultă, cu o incidenţă globală de aproximativ 88/100.000 de persoane pe an (4). Dincolo de simptomatologie, flutterul se poate complica cu tahicardiomiopatie și tromboembolie sistemică. Tratamentul pacienţilor cu flutter atrial se concentrează pe identificarea și tratarea cauzelor reversibile, controlul frecvenţei ventriculare și/sau obţinerea ritmului sinusal, precum și reducerea riscului de complicaţii cardioembolice.
Controlul frecvenţei ventriculare în flutterul atrial este mai puţin eficient decât în fibrilaţia atrială și, prin urmare, mai puţin recomandat, mai ales când procedurile ablative au o rată de succes foarte ridicată. Medicamentele utilizate pentru controlul frecvenţei ventriculare sunt blocantele canalelor de calciu nondihidropiridinice (verapamil sau diltiazem) și betablocantele. Digoxina este utilizată în general ca terapie adjuvantă, nu ca terapie unică. De obicei, sunt necesare doze mari dintr-un singur medicament și în multe cazuri terapia combinată (5).
Conversia la ritm sinusal este „piatra de temelie” a managementului pacienţilor cu flutter atrial. Acesta se poate obţine fie prin conversie electrică cu șoc electric extern, sincron, stimulare atrială rapidă („overdrive pacing”) și mai rar prin medicaţie antiaritmică (deseori ineficientă). Controlul ritmului pe termen lung reprezintă strategia de elecţie. Aceasta se obţine prin ablaţia istmului cavo-triscupidian cu curent de radiofrecvenţă și, mai rar, prin utilizarea crioenergiei.
Cardioversia electrică în urgenţă se impune în caz de instabilitate hemodinamică sau în prezenţa unui fascicul accesor cu preexcitaţie ventriculară (sindromul Wolff-Parkinson-White). Cardioversia electrică electivă poate fi luată în considerare în cazul pacienţilor cu flutter cu debut nou sau simptomatici. Este o metodă rapidă și eficientă (rată de succes 96%) de restabilire a ritmului sinusal. Cardioversia electrică se realizează sub sedare, cu șoc electric cu energie mică (≤ 50 J-bifazic), sincron (6).
La pacienţii cu stimulatoare cardiace implantate (AAI sau DDD), conversia flutterului poate fi obţinută prin stimulare atrială cu o frecvenţă peste rata atrială a flutterului, fiind posibilă prin programarea dispozitivului. Această tehnică are avantajul de a evita sedarea profundă sau anestezia, deoarece stimularea este nedureroasă și este asociată cu o rată mare de succes (7).
Medicamentele antiaritmice au o rată de succes a cardioversiei mult mai scăzută și pot fi asociate cu toxicitate semnificativă. Rata de succes a conversiei la ritm sinusal este de aproximativ 19% pentru sotalol și 29% pentru amiodaronă.
Ibutilid și dofetilid administrate intravenos pentru conversia la ritm sinusal sunt superioare sotalolului și amiodaronei, având succes în 30–70% din cazuri (8–10). Pot determina alungirea intervalului QT și tahicardie ventriculară polimorfă (torsada vârfurilor), de aceea sunt contraindicate în caz de bradicardie și QT lung.
Antiaritmicele de clasa I sunt adesea ineficiente (11). Riscul asociat constă în transformarea în flutter atrial cu un răspuns ventricular rapid (prin scăderea frecvenţei undelor de flutter, cu conducere AV de 1:1); asocierea unui betablocant previne această complicaţie atât pentru flecainidă, cât și pentru propafenonă. Utilizarea antiaritmicelor de clasă I este limitată la cei cu disfuncţie de ventricul stâng (prin efectele adverse hemodinamice) și cardiopatie ischemică (prin efectele proaritmice), fiind dovedită creșterea mortalităţii în aceste cazuri (5).
Deși flutterul atrial este o tahicardie supraventriculară, adenozina nu este utilă pentru tratarea acestei aritmii, ci poate avea doar un rol în cazurile în care diagnosticul electrocardiografic nu este evident. Adenozina administrată intravenos poate crește gradul de bloc atrioventricular și poate demasca undele de flutter (5).
Prevenirea complicaţiilor cardioembolice. Deși există puţine studii dedicate exclusiv pacienţilor cu flutter atrial, se consideră că riscul tromboembolic este similar cu cel al pacienţilor cu fibrilaţie atrială. În consecinţă, aceștia necesită tratament anticoagulant în funcţie de riscul apreciat prin scorul CHA2DS2VASc și în absenţa contraindicaţiilor (12). În cazul unui flutter atrial cu debut de peste 48 de ore, cardioversia electivă se va realiza după efectuarea ecografiei transesofagiene pentru a exclude prezenţa trombilor intracardiaci sau anticoagulare eficientă timp de cel puţin trei-patru săptămâni. În caz de instabilitate hemodinamică este necesară cardioversie imediată și se impune anticoagulare cu heparină nefracţionată. Odată ce ritmul sinusal a fost restabilit, se recomandă continuarea tratamentului cu anticoagulant pentru o perioadă de minimum patru săptămâni sau pe termen nelimitat dacă pacientul are factori de risc (5).
Ablaţia istmului cavo-tricuspidian, zona critică a circuitului de reintrare, constă în realizarea, prin aplicarea de curent de radiofrecvenţă, a unei linii care unește valva tricuspidă cu vena cavă inferioară. Această procedură a fost demonstrată a fi tratamentul eficient de obţinere a ritmului sinusal și de prevenire a recurenţei aritmiei, fiind recomandată ca primă linie de terapie (în special dacă flutterul este recurent) (5). Procedural, primul obiectiv de atins este întreruperea macroreintrării în timpul aplicaţiei de curent de radiofrecvenţă, însă obiectivul final îl constituie blocarea bidirecţională a istmului cavo-tricuspidian. Acest concept permite ablaţia istmică și la pacientul în ritm sinusal, ghidată prin metode de pacing care evaluează conducerea istmică, atunci când există argumente electrocardiografice de flutter atrial tipic (vezi figura). Blocul istmic bidirecţional complet garantează noninductibilitatea flutterului atrial (13, 14). Rata de succes a ablaţiei în flutterul atrial depășește 90% (15), cu recidive de până la 10% după obţinerea blocului istmic complet. Succesul s-a îmbunătăţit la 95%, iar rata complicaţiilor a scăzut odată cu introducerea cateterelor de ablaţie cu irigaţie externă (16). Complicaţiile sunt extrem de rare, sub 1%, și sunt de obicei limitate la accesul vascular. Extrem de rar, procedura poate determina complicaţii: bloc atrioventricular, perforaţie cardiacă sau obstrucţia arterei coronare drepte (15).
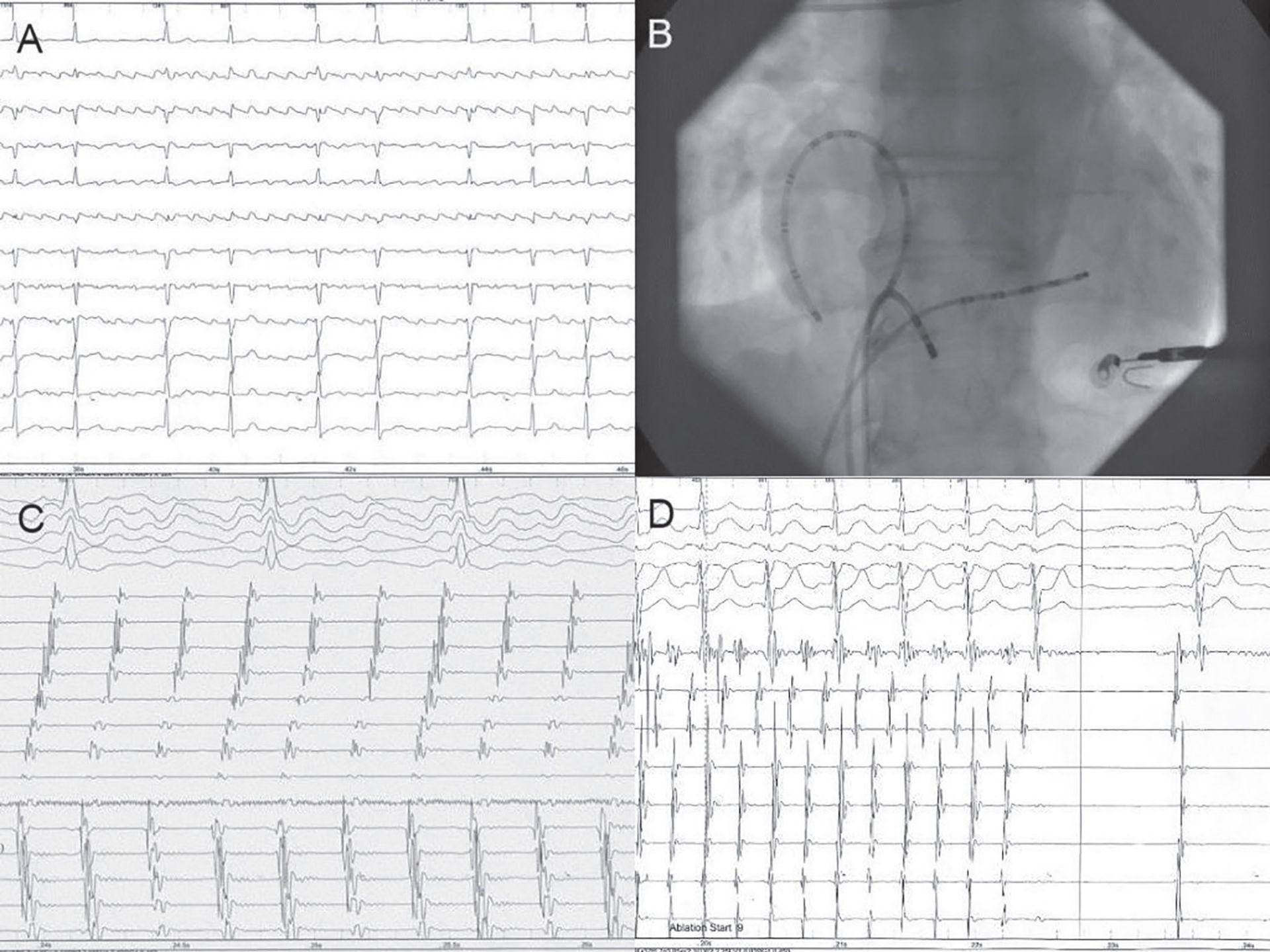
B. Cateter duodecapolar (Halo) în atriul drept poziţionat paralel cu valva tricuspidă, cateter decapolar la nivelul sinusului coronar și cateter de ablaţie la nivelul istmului cavo-tricuspidian (imagine fluoroscopică în vedere anteroposterioară);
C. Demonstrarea activării atriale în sens craniocaudal la nivelul peretelui lateral al atriului drept și în sens caudocranial la nivelul septului interatrial și de la dreapta la stânga în timpul flutterului tipic antiorar;
D. Oprirea flutterului atrial în timpul aplicaţiei de radiofrecvenţă, la nivelul istmului cavo-tricuspidian, ca prim obiectiv în terapia ablativă a istmului cavo-tricuspidian
Prognosticul pe termen lung al pacienţilor cu flutter la care s-a efectuat ablaţia istmului cavo-tricuspidian este afectat de apariţia fibrilaţiei atriale, care poate atinge o incidenţă de până la 50%. Aceasta este mai frecventă la pacienţii cu episoade de fibrilaţie atrială documentate anterior și la cei care se asociază dilataţie atrială stângă (17). Astfel, prezenţa fibrilaţiei atriale postablaţie istmică pare a fi consecinţa evoluţiei naturale a substratului cardiac preexistent la acești pacienţi.
Pe baza acestor considerente, tratamentul eficient pe termen lung al flutterului atrial trebuie condus similar celui pentru fibrilaţia atrială și ar trebui să includă măsuri de prevenţie secundară a factorilor patogeni (controlul tensiunii arteriale, corectarea apneei în somn etc.). Există dovezi că unii pacienţi cu fibrilaţie atrială preexistentă nu mai dezvoltă recurenţe ale acesteia după ablaţia flutterului, sugerând faptul că flutterul atrial ar putea reprezenta factorul declanșator pentru fibrilaţia atrială (18).
Strategiile de tratament al flutterului atrial atipic
Tratamentul acestuia nu diferă de cel al flutterului tipic, însă asocierea mai frecventă cu boala cardiacă structurală este un factor important, care trebuie luat în considerare înainte de luarea deciziilor terapeutice.
Ablaţia flutterului atrial atipic este o procedură mult mai complexă din punct de vedere tehnic. Introducerea tehnicilor de „mapping” 3D a permis identificarea și vizualizarea macrocircuitelor de reintrare nonistmice în atriul drept și stâng, astfel încât tratamentul prin ablaţie al flutterului atrial atipic a devenit posibil și a deschis perspectiva extinderii indicaţiei de ablaţie prin radiofrecvenţă la aritmii care altădată erau inabordabile prin tehnici convenţionale. Prin combinarea tehnicilor de „mapping” 3D cu tehnicile de stimulare (antrenare) se obiectivează zonele lente ale macroreintrărilor atriale atipice, acestea fiind ţinta ablaţiei prin radiofrecvenţă. Flutterul atrial drept incizional are ca substrat anatomic atriotomia atrială dreaptă după procedurile chirurgicale de corecţie a maladiilor cardiace congenitale (închidere a defectelor septale) sau după chirurgie valvulară și, mult mai rar, materialul protetic ce închide defectul septal. Flutterul atrial stâng este fie consecinţa reintrării perimitrale, cu participarea istmului mitral, fie apare ca o complicaţie după procedurile de izolare a venelor pulmonare pentru fibrilaţie atrială în aproximativ 26% din cazuri (18). Ablaţia flutterului atipic este, în general, recomandată pacienţilor cu flutter recurent, prost tolerat, sau la care farmacoterapia este ineficientă. Ratele de succes ale ablaţiei în cazul flutterelor atipice variază între 50% și 88%, în funcţie de complexitatea leziunilor și experienţa centrului. Rata de recurenţă este mai mare în comparaţie cu ablaţia istmului cavo-tricuspidian (5).
1. Saoudi N et al. A classification of atrial flutter and regular atrial tachycardia according to electrophysiological mechanisms and anatomical bases; a Statement from a Joint Expert Group from The Working Group of Arrhythmias of the European Society of Cardiology and the North American Society of Pacing and Electrophysiology. Eur Heart J. 2001 Jul;22(14):1162-82
2. Olgin JE et al. Role of right atrial endocardial structures as barriers to conduction during human type I atrial flutter. Activation and entrainment mapping guided by intracardiac echocardiography. Circulation. 1995 Oct 1;92(7):1839-48
3. Olgin JE et al. Conduction barriers in human atrial flutter: correlation of electrophysiology and anatomy. J Cardiovasc Electrophysiol. 1996 Nov;7(11):1112-26
4. Granada J et al. Incidence and predictors of atrial flutter in the general population. J Am Coll Cardiol. 2000 Dec;36(7):2242-6
5. Katritsis DG et al. European Heart Rhythm Association (EHRA) consensus document on the management of supraventricular arrhythmias, endorsed by Heart Rhythm Society (HRS), Asia-Pacific Heart Rhythm Society (APHRS), and Sociedad Latinoamericana de Estimulación Cardiaca y Electrofisiologia (SOLAECE). Europace. 2017 Mar 1;19(3):465-511
6. Crijns HJ et al. Long-term outcome of electrical cardioversion in patients with chronic atrial flutter. Heart. 1997 Jan;77(1):56-61
7. Goicolea A et al. Conversion of recurrent atrial flutter with implanted pacemakers programmable to high rate AOO mode. Eur J Card Pacing Electrophysiol. 1992;2:19-21
8. Vos MA et al. Superiority of ibutilide (a new class III agent) over DL-sotalol in converting atrial flutter and atrial fibrillation. The Ibutilide/Sotalol Comparator Study Group. Heart. 1998 Jun;79(6):568-75.
9. Kafkas NV et al. Conversion efficacy of intravenous ibutilide compared with intravenous amiodarone in patients with recent-onset atrial fibrillation and atrial flutter. Int J Cardiol. 2007 Jun 12;118(3):321-5
10. Stambler BS et al. Antiarrhythmic actions of intravenous ibutilide compared with procainamide during human atrial flutter and fibrillation: electrophysiological determinants of enhanced conversion efficacy. Circulation. 1997 Dec 16;96(12):4298-306.
11. Crijns HJ et al. Atrial flutter can be terminated by a class III antiarrhythmic drug but not by a class IC drug. Eur Heart J. 1994 Oct;15(10):1403-8
12. European Heart Rhythm Association et al. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J. 2010 Oct;31(19):2369-429
13. Poty H et al. Radiofrequency catheter ablation of atrial flutter. Further insights into the various types of isthmus block: application to ablation during sinus rhythm. Circulation. 1996 Dec 15;94(12):3204-13
14. Cosío FG et al. Determining inferior vena cava-tricuspid isthmus block after typical atrial flutter ablation. Heart Rhythm. 2005 Mar;2(3):328-32
15. Spector P et al. Meta-analysis of ablation of atrial flutter and supraventricular tachycardia. Am J Cardiol. 2009 Sep 1;104(5):671-7
16. Jaïs P et al. Prospective randomized comparison of irrigated-tip versus conventional-tip catheters for ablation of common flutter. Circulation. 2000 Feb 22;101(7):772-6
17. Gilligan DM et al. Long-term outcome of patients after successful radiofrequency ablation for typical atrial flutter. Pacing Clin Electrophysiol. 2003 Jan;26(1 Pt 1):53-8
18. Haïssaguerre M et al. Catheter ablation of long-lasting persistent atrial fibrillation: clinical outcome and mechanisms of subsequent arrhythmias. J Cardiovasc Electrophysiol. 2005 Nov;16(11):1138-47
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe