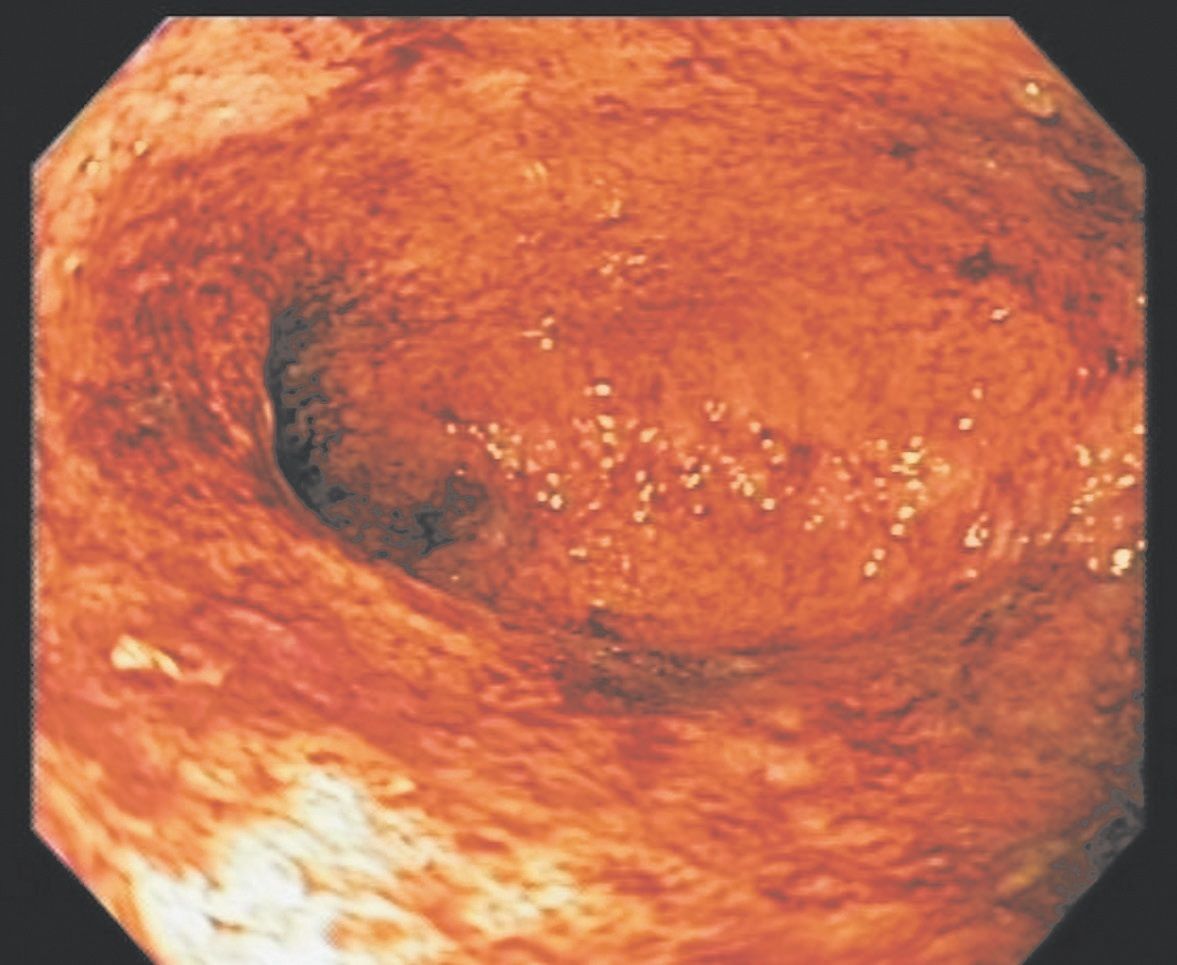
Endoscopia joacă un rol extrem de important în diagnosticul și managementul pacienţilor cu colită ulcerativă (CU), în evaluarea activităţii endoscopice, care este esenţială pentru monitorizarea obiectivă a răspunsului la tratament.
În plus, supravegherea endoscopică are scopul de a reduce incidenţa cancerului colorectal la pacienţii cu colită ulcerativă și este esenţială după o evoluţie lungă a bolii (1, 2).
Colita ulcerativă poate fi diagnosticată aproape întotdeauna prin examinarea rectului și colonului sigmoid. Este o afecţiune difuză, cu inflamaţie continuă care începe în rect cu extindere proximală ce variază de la caz la caz. Mucoasa prezintă edem, eritem, cu ulceraţii fine, depuneri de puroi și este friabilă – sângerează ușor, spontan sau la atingerea cu endoscopul. Ulceraţiile mai profunde, care pot conduce la o totală denudare a mucoasei, se asociază cu boală mai severă. Delimitarea mucoasei afectate de mucoasa normală este netă (3).

Pe măsură ce leziunile din colita ulcerativă se vindecă, modificările mucoasei pot deveni focale. Regenerarea mucoasei colonice se face eventual prin restituţia patternului vascular normal. În ariile cu leziuni mai severe, ţesutul de granulaţie se reepitelizează, conducând la formarea pseudopolipilor inflamatori. Acești pseudopolipi nu au potenţial de transformare neoplazică, dar pot fi greu de diferenţiat de polipii adenomatoși (2).
În mod normal, leziunile caracteristice colitei ulcerative respectă rectul. La adulţi, aspectul normal al rectului sau inflamaţia parţială a acestuia se poate observa mai ales după administrarea terapiei topice (4).
Inflamaţia parţială a cecului poate fi observată în cazul pacienţilor cu colită stângă. În cazurile fără afectarea rectului și cu afectare parţială a cecului se impune și evaluarea intestinului subţire. Evoluţia naturală a pacienţilor cu afectare discontinuă a colonului drept pare să fie similară cu cea a pacienţilor cu colită stângă (5).
Afectarea apendicelui este raportată ca leziune izolată în până la 75% din pacienţii cu CU. Aceasta s-a asociat cu un răspuns mai bun la tratament și un risc mai mare de pouchită după anastomoza pouch-ileală (5).
Extinderea leziunilor din cec la nivelul ileonului terminal este cunoscută și sub numele de „backwash ileitis” și poate fi observată până la 20% din pacienţii cu colită extinsă. Rareori, eroziunile ileale pot să apară fără afectare cecală. Acest subgrup de pacienţi prezintă o boală mai refractară, cu un risc mai mare de cancer colonic. În prezenţa acestor modificări se impune completarea examinărilor cu alte metode imagistice pentru diferenţierea colitei ulcerative de boala Crohn (6).
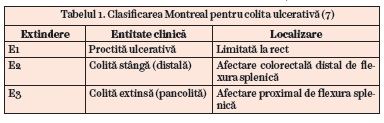
Grupul de lucru al specialiștilor de la Montreal a subliniat importanţa unui sistem de subclasificare pentru CU, iar aceasta este cea mai larg utilizată (tabelul 1). Această clasificare oferă informaţii atât despre extinderea bolii, cât şi despre severitate, ambele având un important rol prognostic. Extinderea bolii este clasificată ca fiind limitată la nivelul rectului (E1), distal de flexura dreaptă a colonului (E2) sau proximal de flexura splenică (E3) (7).
Există mai multe scoruri propuse pentru măsurarea activităţii endoscopice din colita ulcerativă, dar acestea sunt rar utilizate în practica zilnică și nu toate sunt validate. Scorul Mayo a fost folosit extensiv în trilalurile randomizate ce evaluau răspunsul endoscopic la tratament. Remisia endoscopică a fost definită ca un scor Mayo ≤ 1. Dintre toate scorurile prezentate mai jos, doar scorul endoscopic de severitate a colitei ulcerative (UCEIS) și scorul colonoscopic de severitate a colitei ulcerative (UCCIS) au fost validate (tabelul 2) (3, 8).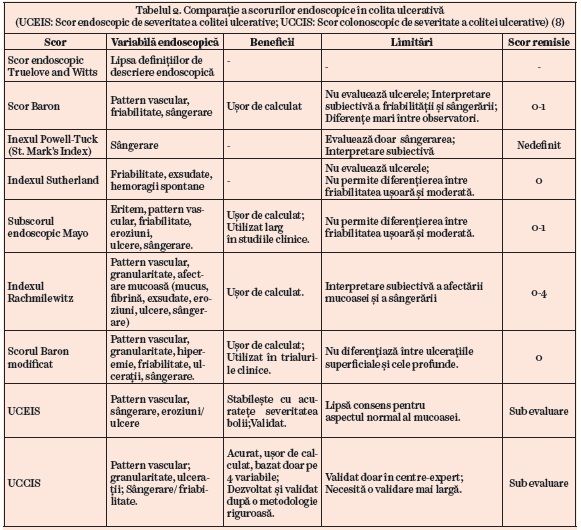
Nu există caracteristici endoscopice specifice colitei ulcerative sau bolii Crohn. Totuși, afectarea colonică continuă, cu delimitarea netă a zonei de inflamaţie și afectarea rectală sunt întâlnite în colita ulcerativă. Pentru boala Crohn pledează leziunile discontinue, prezenţa stenozelor sau fistulelor și afectarea perianală (9).
Pacienţii cu alte tipuri de colite pot avea aspecte endoscopice similare cu cei cu boli inflamatorii intestinale. Cel mai frecvent, diagnosticul diferenţial trebuie făcut cu colitele infecţioase, cu cele ischemice, medicamentoase sau cele de iradiere.
Chiar și în condiţiile utilizării tehnicilor noi endoscopice și a unui diagnostic histologic bine efectuat, există situaţii când sunt dificil de diferenţiat infecţiile digestive de bolile inflamatorii intestinale. În special infecţiile cu Salmonella, Shigella sau Campylobacter pot avea aspect endoscopic similar cu colita ulcerativă (10).
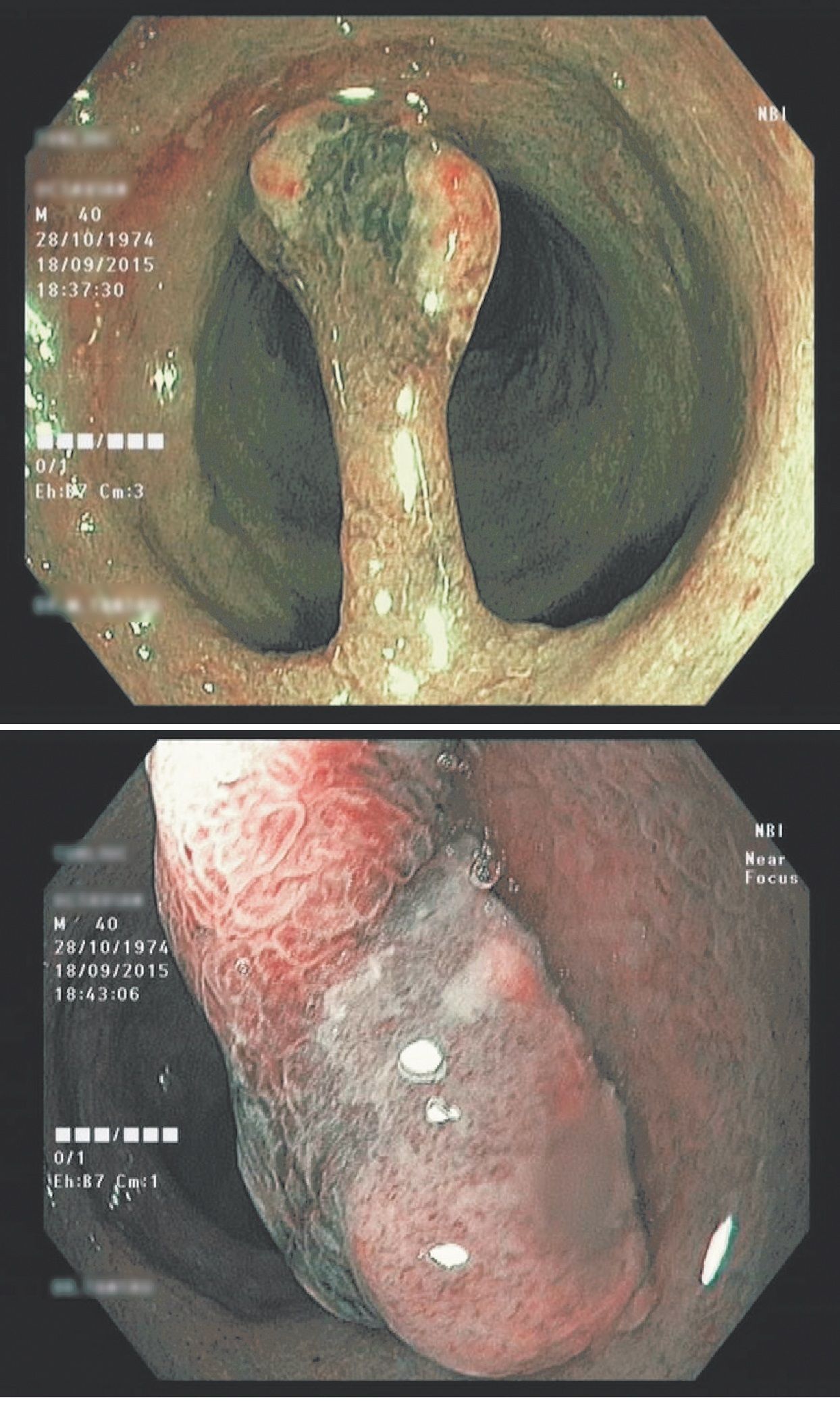
Infecţia cu citomegalovirus trebuie și ea diferenţiată de colita ulcerativă, putând avea un spectru endoscopic extrem de variabil, de la eritem parcelar, edem al mucoasei, microeroziuni la ulceraţii profunde sau aspect pseudotumoral. Suprapunerea infecţiilor cu Clostridium difficile sau citomegalovirus poate face diferenţierea mai dificilă în anumite situaţii. Aproximativ 5% din leziunile produse de tuberculoza intestinală pot mima un aspect de pancolită (11, 12).
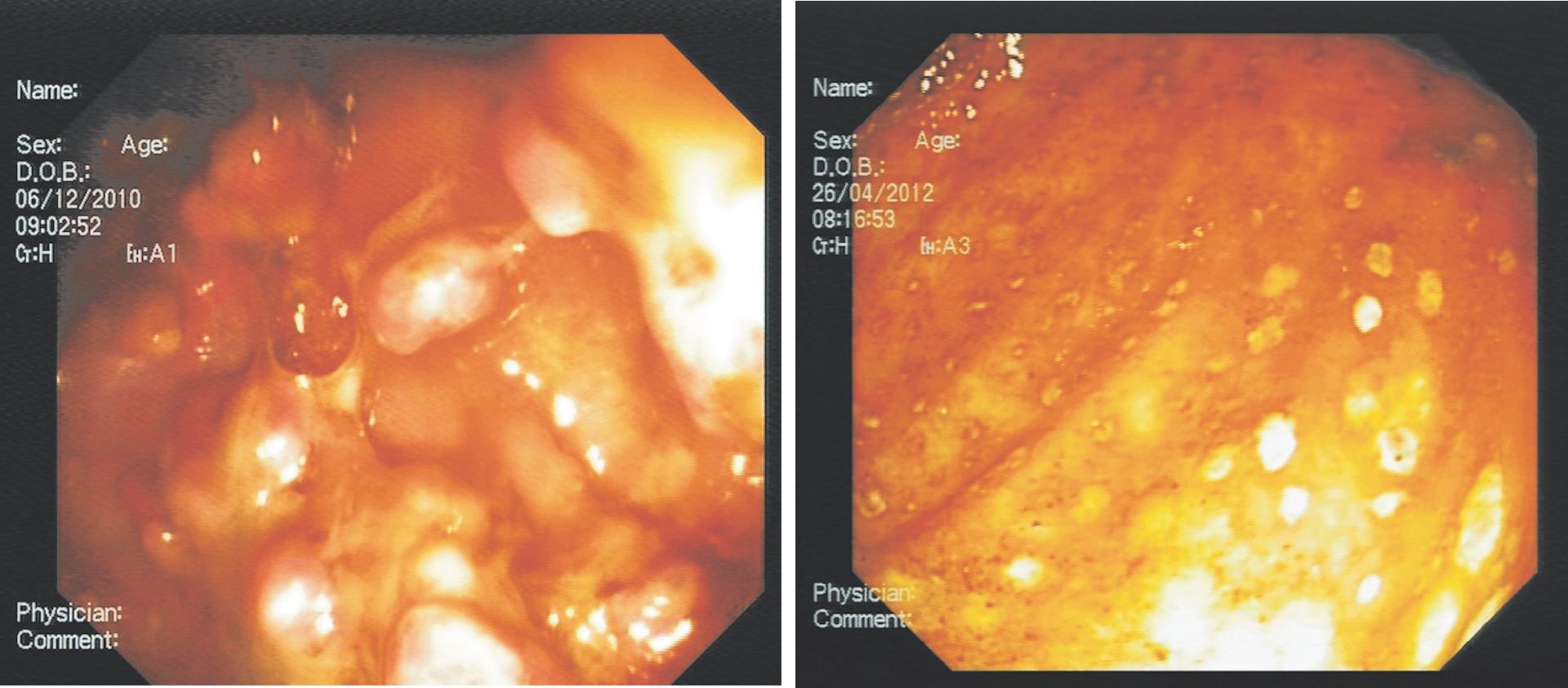
Dreapta: aspect endoscopic în colita ulcerativă cu infecţie suprapusă cu Clostridium difficile (colecţia Marcel Tanţău)
Colita ischemică reprezintă un alt diagnostic diferenţial important cu colita ulcerativă. Modificările endoscopice induse de ischemie includ: aspectul normal al rectului, delimitare netă a teritoriului afectat, în special de la colonul sigmoid la flexura splenică, hemoragie peteșială, ulceraţii longitudinale și rezoluţia rapidă a modificărilor la examinări seriate. Deoarece colonoscopia este metoda de stabilire a diagnosticului de colită ischemică în peste 90% din cazuri, aceasta rămâne procedura de elecţie, dar poate prezenta anumite riscuri în situaţii acute, putând fi înlocuită cu sigmoidoscopia asociată cu examinări radiologice - CT abdominal. Din păcate, niciuna dintre tehnicile noi endoscopice nu poate preciza cu certitudine un diagnostic diferenţial între bolile inflamatorii intestinale și alte colite (13).
Colopatia indusă de antiinflamatoarele nonsteroidiene poate afecta tot cadrul colic, dar cu o ușoară predominanţă este afectat colonul drept. Modificările constau în ulceraţii și stricturi (14).
Efectuarea endoscopiei de rutină la pacienţii în remisiune clinică nu este necesară decât dacă se presupune că poate schimba managementul acestui pacient. Endoscopia trebuie însă efectuată în cazurile de recădere, refractaritate la tratament, reapariţia unor noi simptome sau când se indică intervenţia chirurgicală (3).
Dat fiind riscul de potenţiale complicaţii, câteva reguli trebuie aplicate când se efectuează colonoscopia la pacienţii ce se prezintă cu puseuri severe de colită ulcerativă. Acestea constau în: evaluare radiologică înainte de efectuarea endoscopiei pentru excluderea megacolonului toxic, limitarea examinării la rectosigmoidoscopie, fără pregătire colonică prealabilă, cu minimă insuflare, oprirea examinării când sunt detectate leziuni severe. Evaluarea endoscopică cu prelevarea de biopsii este esenţială pentru diagnosticul colitei ulcerative active și pentru excluderea altor cauze de colită active (2).
Nu există încă un consens pentru definiţia vindecării mucoasei în colita ulcerativă. Există însă câteva criterii propuse: absenţa friabilităţii, a eroziunilor sau a ulceraţiilor la nivelul mucoasei. Astfel, absenţa pattern-ului vascular normal este compatibilă cu vindecarea mucoasei. Nu există o relaţie clară între vindecarea mucoasei și riscul de colectomie la pacienţii cu colită ulcerativă. Există însă o corelaţie clară între gradul și persistenţa inflamaţiei colonice și riscul de dezvoltare a cancerului colorectal (CCR) la acești pacienţi. Un mai bun control al inflamaţiei, demonstrat de vindecarea mucoasei, se asociază cu un risc mai scăzut de CCR (15).
Supravegherea colonoscopică permite detecţia modificărilor displazice și detecţia precoce a CCR, ceea ce duce la un prognostic mai bun, cu reducerea incidenţei CCR și a mortalităţii prin această complicaţie (16).
Supravegherea colonoscopică trebuie iniţiată la opt-zece ani de la debutul simptomatologiei și trebuie efectuată în cazul pacienţilor cu colită stângă sau colită extinsă. Din moment ce nu există o evidenţă clară a intervalelor de supraveghere, individualizarea acestor intervale trebuie făcută în funcţie de stratificarea riscului (3, 17).
Pacienţii cu risc crescut (stenoză sau displazie detectată în ultimii cinci ani, asocierea colangitei sclerozante primitive, colită extinsă cu inflamaţie severă sau istoric familial de CCR la o rudă de gradul I la vârstă sub 50 de ani) necesită efectuarea colonoscopiei de supraveghere la un an (18).
Pacienţii cu risc intermediar (colită extinsă cu activitate minimă sau moderată, pseudopolipi inflamatori sau istoric familial de CCR la o rudă de gradul I la vârstă peste 50 de ani) necesită efectuarea colonoscopiei de supraveghere o dată la doi-trei ani.
Pacienţii care nu prezintă risc crescut sau intermediar necesită efectuarea colonoscopiei de supraveghere o dată la cinci ani (3, 17).
Este necesară pregătirea corespunzătoare a colonului înaintea efectuării colonoscopiei de screening, cu o inspecţie meticuloasă a mucoasei colonice în timpul retragerii lente a endoscopului, utilizând de preferinţă endoscopie de înaltă rezoluţie pentru detectarea optimă a neoplaziei (3).
În timpul colonoscopiei de screening este de preferat a se utiliza cromoendoscopia (cu albastru de metilen sau indigo carmin) și ulterior prelevarea de biopsii din orice leziune vizibilă, aceasta reprezentând de altfel metoda preferată de screening. Dacă nu este posibilă efectuarea cromoendoscopiei, se vor preleva biopsii aleatorii – câte patru la fiecare 10 cm, minimum 32 de biopsii (19, 20).
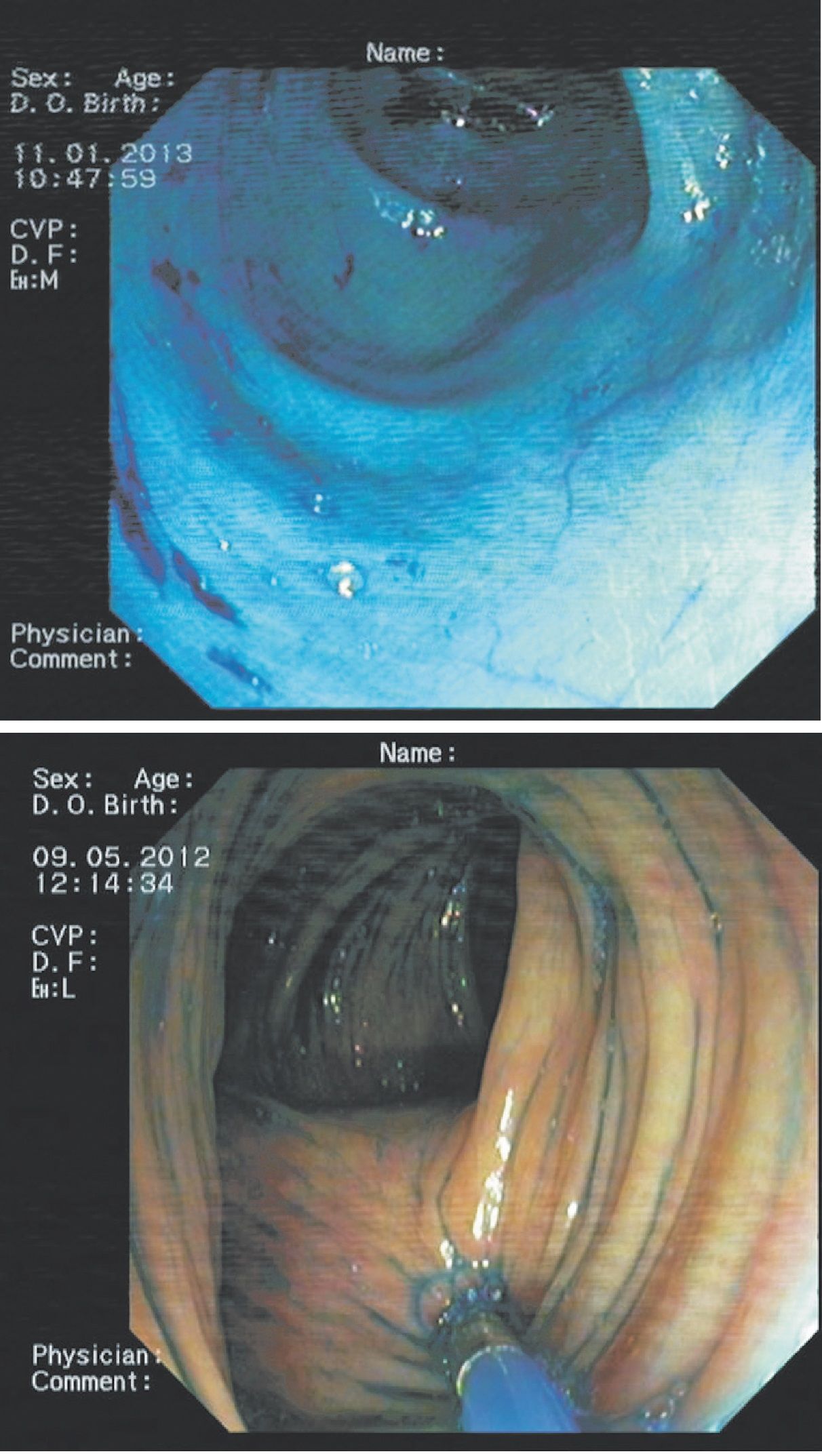
Jos: cromoendoscopie cu albastru de metilen la pacient cu colită ulcerativă (colecţia Marcel Tanţău)
Alte tehnici de endoscopie - examinarea cu lumina de bandă îngustă (NBI) sau autofluorescenţa - nu și-au dovedit superioritatea faţă de examinarea în lumina albă sau cromoendoscopia în detecţia leziunilor neoplazice, astfel încât nu pot fi recomandate pentru supravegherea colonoscopică la pacienţii cu colită ulcerativă (20).
1. Carthage P et al. Endoscopic evaluation in diagnosis and management of inflammatory bowel disease. World J Gastrointest Endosc. 2016 December; 16; 8: 723-32.
2. Shergill AK et al. The role of endoscopy in inflammatory bowel disease. Gastrointest Endosc. 2015; 81: 1101-21.
3. Annese V et al. European evidence based consensus for endoscopy in inflammatory bowel disease. J Crohns Colitis. 2013; 7: 982-1018.
4. Bernstein CN et al. Patchiness of mucosal inflammation in treated ulcerative colitis: a prospective study. Gastrointest Endosc. 1995; 42: 232-37.
5. Rubin DT et al. The peri-appendiceal red patch in ulcerative colitis: review of the University of Chicago experience. Dig Dis Sci. 2010; 55: 3495-3501.
6. Goldstein N et al. Contemporary morphologic definition of backwash ileitis in ulcerative colitis and features that distinguish it from Crohn disease. Am J Clin Pathol. 2006; 126: 365–76.
7. Silverberg MS et al. Toward an integrated clinical, molecular and serological classification of inflammatory bowel disease: Report of a Working Party of the 2005 Montreal World Congress of Gastroenterology. Can J Gastroenterol. 2005; 19(Suppl A):5-36.
8. Corte C et al. Association between the ulcerative colitis endoscopic index of severity (UCEIS) and outcomes in acute severe ulcerative colitis. J Crohns Colitis. 2015; 9: 376-438.
9. Simpson P et al. Endoscopic evaluation of patients with inflammatory bowel disease. Inflamm Bowel Dis. 2008; 14: 1287–97.
10. Nikolaus S et al. Diagnostics of inflammatory bowel disease. Gastroenterology. 2007; 133:1670-89.
11. McCurdy JD et al. A model for identifying cytomegalovirus in patients with inflammatory bowel disease. Clin Gastroenterol Hepatol. 2015; 13: 131-37.
12. Ben-Horin S et al. Prevalence and clinical impact of endoscopic pseudomembranes in patients with inflammatory bowel disease and Clostridium difficile infection. J Crohns Colitis. 2010; 4: 194-98.
13. Sherid M et al. Ischemic colitis: A forgotten entity. Results of a retrospective study in 118 patients. J Dig Dis. 2014; 15: 606-13.
14. Aftab AR et al. NSAID-induced colopathy. A case series. J Gastrointestin Liver Dis. 2010; 19: 89-91.
15. Lemmens B et al. Correlation between the endoscopic and histologic score in assessing the activity of ulcerative colitis. Inflamm Bowel Dis. 2013; 19: 1194-1201.
16. Wang YR et al. Rate of early/ missed colorectal cancers after colonoscopy in older patients with or without inflammatory bowel disease in the United States. Am J Gastroenterol. 2013.
17. Laine L et al. SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastroenterology. 2015; 148: 639-51.
18. Zheng HH et al. Increased risk of colorectal neoplasia in patients with primary sclerosing cholangitis and inflammatory bowel disease: a meta-analysis of 16 observational studies. Eur J Gastroenterol Hepatol. 2016; 28: 383-90.
19. van den Broek FJ et al. Random biopsies taken during colonoscopic surveillance of patients with longstanding ulcerative colitis: low yield and absence of clinical consequences. Am J Gastroenterol. 2014; 109: 715-22.
20. Marion JF et al. Chromoendoscopy Is More Effective Than Standard Colonoscopy in Detecting Dysplasia During Long-term Surveillance of Patients With Colitis. Clin Gastroenterol Hepatol. 2016; 14: 713-19.
Dacă vrei să fii la curent cu tot ce se întâmplă în lumea medicală, abonează-te la „Viața Medicală”, publicația profesională, socială și culturală a profesioniștilor în Sănătate din România!
Titularii abonamentelor pe 12 luni sunt creditați astfel de:
Cookie-urile ne ajută să vă îmbunătățim experiența pe site-ul nostru. Prin continuarea navigării pe site-ul www.viata-medicala.ro, veți accepta implicit folosirea de cookie-uri pe parcursul vizitei dumneavoastră.
Da, sunt de acord Aflați mai multe