Obezitatea
se asociază cu un status inflamator cronic discret, caracterizat printr-o
producție anormală de citokine (proteina C reactivă, IL-6, TNFα) care determină
activarea unor căi de semnalizare intracelulară inflamatorii la nivelul
țesutului adipos alb (1). Adipocitele hipertrofiate și celulele stromale de la
nivelul țesutului adipos alb amplifică în mod direct răspunsul inflamator
sistemic. Țesutul adipos alb conține în mod normal macrofage în proporție de
5–10%. Creșterea ponderală determinată de dieta dezechilibrată este asociată cu
o infiltrare semnificativă a țesutului gras cu macrofage, care ajung să
reprezinte 60% din țesutul adipos alb pe modelele animale (2).
Există
mai mult ipoteze care încearcă să explice creșterea infiltrării cu macrofage a
țesutului adipos, cea mai larg acceptată fiind „ipoteza hipoxiei“, propusă în
2004 de Trayhum și Wood (3). Conform acestei ipoteze, țesutul adipos este mai
slab oxigenat în obezitate. Această hipoxie ar activa lipoliza și scăderea
preluării acizilor grași liberi de la nivelul țesutului adipos (4), cu
declanșarea consecutivă a unui răspuns inflamator pe calea receptorului TLR4.
Producerea
de citokine proinflamatorii la nivelul macrofagelor din țesutul adipos alb este
implicată în apariția insulinorezistenței din obezitate, creșterea producției
de citokine fiind paralelă cu creșterea conținutului în macrofage a țesutului
adipos (2, 5).
Structura și funcțiile TNFα
TNFα
(Tumor necrosis factor), cunoscut și sub denumirea de cașexină, este o
citokină implicată în inflamația sistemică, făcând parte din proteinele de fază
acută. Rolul său princeps este de a regla activitatea celulelor imune. TNFα
este de asemenea un pirogen endogen. Determinând reacție febrilă, poate induce
inflamația și sepsisul, cașexia și apoptoza celulară, inhibă tumorigeneza și
replicarea virală. Este implicat ca factor etiopatogenic în numeroase condiții
patologice de tipul bolii Alzheimer (6), în neoplazii (7), depresie majoră (8),
boli inflamatorii intestinale (9). Alături de proteina asociată hormonului
paratiroidian (PTHrp), TNFα este implicat în apariția hipercalcemiilor asociate
neoplaziilor.
În
ultima perioadă s-a arătat că rolurile biologice ale TNFα sunt multiple, acesta
intervenind în metabolismul lipidic, insulinorezistență și în disfuncția
endotelială.
Sinteza
TNFα este controlată de gena corespunzătoare de la nivelul brațului scurt al
cromozomului 6 (6p21.3) și este formată din patru exoni, cel de-al patrulea
codificând 80% din totalul proteinei secretate (10). TNFα este produs în
special de macrofage, dar poate fi produs și de alte celule imune, de
celulele epiteliale, endoteliale și tumorale. Este sintetizat ca o proteină
transmembranară de tip II, cu greutatea moleculară de 26 kDa, constituită
dintr-un domeniu citoplasmatic de 35 de aminoacizi, un segment transmembranar
de 21 de aminoacizi și un domeniu extracelular de 177 de aminoacizi. Formează
la suprafața celulară homotrimeri prin legături non-covalente, forma solubilă a
TNFα având o greutate moleculară de 16 kDa (fig.1).
Receptorul
pentru TNFα este de asemenea o proteină trimerică aparținând familiei
complexului major de histocompatibilitate, codificată de cromozomul 6p21.3.
Acesta este format dintr-o parte extracelulară de legare a ligandului (care la
rândul său este alcătuită din două-șase regiuni bogate în cisteină), o parte
transmembranară și o regiune intracelulară (death domain).
Există
mai mulți receptori pentru TNFα, cei mai importanți fiind TNFR1 și TNFR2. Partea
solubilă a ambelor tipuri de receptori poate circula liberă în plasmă și poate
lega TNFα, neutralizându-l. TNFR1 este prezent în majoritatea celulelor prin
intermediul cărora TNFα își exercită aproape toate funcțiile biologice. TNFR2
este prezent mai ales la suprafața celulelor imune și mediază doar câteva
roluri biologice ale TNFα.
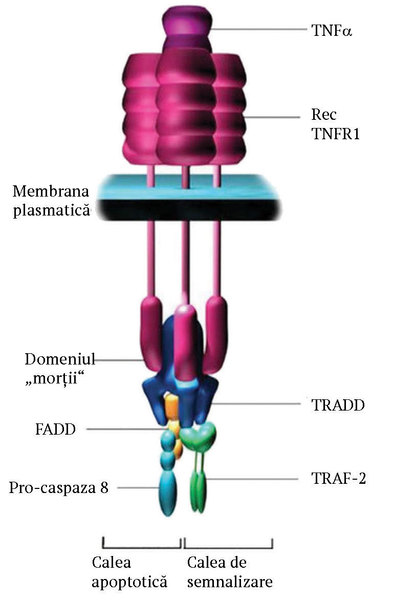
Legarea
TNFα de receptorul specific conduce la trimerizarea receptorului. Acesta suferă
o modificare conformațională care îi permite legarea de porțiunea
intracitoplasmatică a unei proteine activatoare – TRADD (TNF receptor
asociated death domain protein). Aceasta va duce la activarea a trei căi de
semnalizare (11, 12): activarea NF-κB – un factor de transcripție care este
implicat în supraviețuirea celulară, răspunsul inflamator și anti-apoptotic,
activarea căii MAPK urmată de translocarea JNK în interiorul nucleului, cu
activarea consecutivă a unor factori de transcripție de tipul c-Jun și ATF2
(această cale este implicată în diferențierea celulară și în proliferare) și activarea
căii caspazelor, prin care complexul TNFα-TNFR determină apoptoza celulară. (…)