Evoluţia
epidemică a bolii cronice de rinichi este o importantă problemă de sănătate
publică, afectând până la 10% din populaţia adultă în Marea Britanie şi 11% în
Statele Unite; în România, se estimează că aproximativ 2,3 milioane de persoane
au boală cronică de rinichi şi numai 45.240 (2%) se regăsesc în raportările
medicilor de familie (Cepoi, 2011) – probabil cei cu rata de filtrare
glomerulară (RFG) sub 30 ml/min/1,73 m2, când măsurile de profilaxie secundară
sunt foarte limitate.
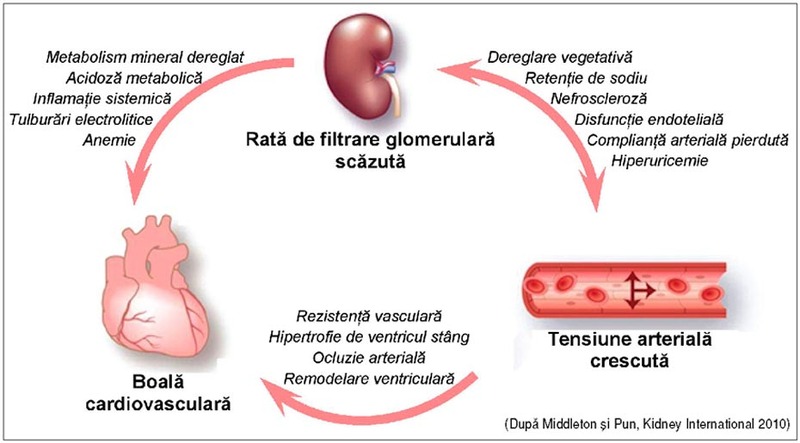
Datele
de care dispunem, în ultimii ani, consolidează importanţa bolii cardiovasculare
în determinarea calităţii vieţii şi a prognosticului pacienţilor cu boală
cronică de rinichi. Tot mai multe dovezi demonstrează că manifestările şi
complicaţiile bolii cardiovasculare diferă în prezenţa bolii cronice de
rinichi. Morbiditatea şi mortalitatea de cauză cardiovasculară la pacienţii cu
boală cronică de rinichi sunt mari, iar rezultatele obţinute în boala cronică
de rinichi sunt grevate de prezenţa bolii cardiovasculare.
Boala
cronică de rinichi (BCR) este definită prin anomalii ale structurii şi funcţiei
renale, persistente mai mult de trei luni, evidenţiate prin raportul albumină/creatinină
urinară mai mare de 30 mg/g şi alte anomalii ale unor investigaţii de laborator
sau scăderea RFG sub 60 ml/min/1,73m2.
BCR,
odată instalată, evoluează cu pierderea treptată şi definitivă a funcţiei
renale. În evoluţia sa graduală, BCR asociază hipertensiune arterială,
hipertrofie ventriculară stângă, anomalii ale metabolismului mineral şi ale
scheletului osos, anemie, dezechilibre acido-bazice şi hidro-electrolitice,
malnutriţie, inflamaţie, pericardită uremică, encefalopatie uremică etc.
Factori de risc
Cel
mai frecvent, BCR este determinată de o altă boală, care afectează rinichii,
în primul rând diabetul zaharat sau hipertensiunea arterială. Principalii
factori de risc pentru apariţia bolii cronice de rinichi sunt: diabetul
zaharat, HTA, vârsta peste 50 ani, bolile cardiovasculare, bolile structurale
ale rinichiului (litiază renală, hipertrofie a prostatei), boli sistemice (lupus
eritematos sistemic), istoric familial pozitiv (rude de gradul I cu nefropatii
sau aflate în tratament substitutiv renal: hemodializă, dializă peritoneală sau
transplant renal), insuficienţa renală acută în antecedente, hematurie sau
proteinurie descoperite întâmplător, rinichiul unic congenital sau chirurgical.
Subiecţii care prezintă unul sau mai mulţi factori de risc se află la risc de a
dezvolta boala cronică de rinichi. Programele de prevenţie trebuie să vizeze,
în primul rând, această categorie de populaţie.
BCR
este o boală cu etiologie multifactorială şi necesită o abordare
multidisciplinară. Echipa multidisciplinară pentru îngrijirea integrată a
pacienţilor cu boală cronică de rinichi trebuie să includă medici de familie,
nefrologi, diabetologi, cardiologi. Diagnosticul BCR în stadiile 1 şi 2 depinde
în mare măsură de medicii de familie şi de medicii de alte specialităţi
(diabetologi, cardiologi, urologi, reumatologi, internişti, gastroenterologi).
Depistarea BCR în stadii iniţiale necesită implicarea în mai mare măsură a
medicilor nefrologi şi modificarea cadrului de acordare a asistenţei medicale
în ambulatoriu. Creşterea eficienţei îngrijirii integrate a pacienţilor cu
boala cronică de rinichi presupune colaborarea cu medicii de familie şi
ameliorarea cadrului legislativ (barem de investigaţii şi medicamente, tarife
pentru consultaţii). Din păcate, nu avem în România un registru naţional al
bolnavilor cu BCR aflaţi în predializă, dar avem Registrul renal român pentru
bolnavii dializaţi pentru care avem date precise.
Diagnostic şi evoluţie
Pentru diagnosticul bolii cronice de rinichi
sunt necesare două consultaţii la interval de trei luni, cu determinarea
creatininei serice şi estimarea RFG (eRFG < 60 ml/min), determinări ale
albuminei şi creatininei urinare în urina spontan emisă şi calcularea
raportului albumină/creatinină urinară (RAC = 30 mg/g).
BCR
evoluează cu pierderea treptată şi definitivă a funcţiilor renale, spre terapia
de substituţie a funcţiilor renale sau deces. Riscul de deces este foarte mare:
doar unul din cinci pacienţi cu BCR ajunge în stadiul terminal al bolii şi are şansa
de a beneficia de terapia de substituţie a funcţiei renale; patru decedează
(majoritatea de cauză cardiovasculară). Intervenţiile terapeutice pot limita
progresia BCR, apariţia complicaţiilor, diminuarea riscului cardiovascular sau
acutizarea bolii.
Ghidul
pentru evaluarea şi managementul BCR (Kidney Disease Improving Global Outcomes
– KDIGO 2012) propune un model nou pentru definirea şi stratificarea riscului
bolii cronice de rinichi, coroborând nivelul RFG cu magnitudinea albuminuriei
(categoriile de albuminurie: A1, A2, A3). Noutăţile pe care le aduce KDIGO 2012
sunt: subîmpărţirea stadiului 3 în două stadii (3a şi 3b), ceea ce ameliorează relevanţa
clinică a stadializării; introducerea raportului albumină/creatinină urinară,
determinat din urina spontană, drept criteriu de diagnostic şi de stratificare
a riscului; definirea categoriilor de risc – de mortalitate, morbiditate
cardiovasculară şi progresie spre necesitatea de tratament substitutiv renal
(TSFR) – foarte utile pentru elaborarea programelor terapeutice.
Tratament
Deşi
în România aproximativ 2,3 milioane de persoane au boală cronică de rinichi,
numai 45.240 (2%) se regăsesc în raportările medicilor de familie (Cepoi,
2011), majoritatea probabil în stadiul 5, când măsurile de profilaxie secundară
sunt foarte limitate. Raportările afecţiunilor cu potenţial evolutiv către BCR
ale medicilor de familie sunt în creştere, dovedind faptul că, în majoritatea
cazurilor, boala cronică de rinichi este ignorată. De aceea, un program de
prevenţie primară şi intervenţie în boala cronică de rinichi, axat pe medicii
de familie, ar fi pe deplin justificat, mai ales că măsurile terapeutice de
reducere a riscurilor – renale şi cardiovasculare – există şi sunt eficiente.
Principalele
măsuri terapeutice ar fi: controlul presiunii arteriale, reducerea proteinuriei
prin mijloace specifice în cazul nefropatiilor cu patogenie imunitară, prin
inhibitori ai enzimei de conversie (IECA) sau blocanţi ai receptorilor de
angiotensină (BRA) la pacienţii cu nefropatie diabetică. Terapia hipolipemiantă
are un rol neclar, iar terapia antiplachetară ar fi utilă atunci când există
comorbidităţi cardiovasculare. Scopul terapiei este de a reduce
morbiditatea/mortalitatea de cauză cardiovasculară sau reducerea numărului de
bolnavi care necesită tratament de substituţie a funcţiei renale. Deoarece nu
există date suficiente pentru a evalua impactul tratamentului asupra morbidităţii
cardiovasculare la această categorie de bolnavi, indicatorul de evaluare a
eficienţei măsurilor de prevenţie secundară este reducerea numărului de bolnavi
care necesită tratament de substituţie a funcţiei renale; eficienţa economică
este evaluată în raport cu acest criteriu.
Opiniile
cu privire la utilitatea programelor de depistare activă şi intervenţie
terapeutică în BCR sunt divergente. Un program de depistare activă şi intervenţie
în boala cronică de rinichi nu ar fi cost-eficient în condiţiile României,
chiar dacă s-ar adresa numai populaţiei cu risc crescut.
Societatea Română de Nefrologie (SRN)
împreună cu Societatea Română de Diabet, Nutriţie şi Boli Metabolice (SRDNBM)
au derulat studiul naţional privind prevalenţa prediabetului, diabetului,
dislipidemiei, supraponderalităţii, obezităţii, hiperuricemiei şi bolii cronice
de rinichi în România – PREDATORR. Studiul s-a încheiat, iar rezultatele sunt
prezentate în cadrul congresului naţional de diabet, la Sibiu, chiar la data
apariţiei acestui articol. Ulterior, va fi posibilă elaborarea unui program de
prevenţie a bolii cronice de rinichi în România.
BCR cu risc înalt include pacienţii cu
albuminurie ca raport albumină/creatinină mai mare de 300 mg/g (deci inclusiv
pe aceia cu nefropatii acute sau cronice), cu sau fără eRFG mai mică de 45
ml/min, la care se înregistrează o creştere apreciabilă a riscului renal şi
cardiovascular şi din acest motiv necesită intervenţie specializată nefrologică.
Obiectivul intervenţiei medicale este reducerea
progresiei declinului funcţiei renale, definit ca scăderea eRFG cu mai mult de
5 ml/min pe an sau mai mult de 10 ml/min în cinci ani şi pregătirea pacientului
pentru iniţierea tratamentului substitutiv renal*. Din punct de
vedere clinic, reducerea morbidităţii/mortalităţii generale sau cardiovasculare,
ca şi a necesarului de tratament substitutiv renal ar fi obiectivele cele mai
importante. Intervenţia ar consta în diagnostic, monitorizare clinică şi de
laborator, tratament patogenic al nefropatiilor glomerulare (imunosupresoare,
corticoizi), tratament pentru reducerea progresiei (antihipertensive,
diuretice, cetoanalogi ai aminoacizilor esenţiali) şi a riscului cardiovascular
(statine, fibraţi), tratament al unor consecinţe ale insuficienţei renale
(anemie, dezechilibrul metabolismelor mineral şi acido-bazic). Consilierea
pacientului pentru alegerea metodei de substituţie a funcţiei renale şi
realizarea căii de abord vascular în timp util constituie intervenţii utile şi
eficiente.
Situaţia din România
Din păcate, în România, nu avem un registru
naţional al bolnavilor cu BCR aflaţi în predializă, dar avem Registrul renal
român al bolnavilor dializaţi, pentru care avem date precise. Din anul 1996,
numărul total al bolnavilor aflaţi în tratament de substituţie a funcţiei
renale la sfârşitul fiecărui an (bolnavi prevalenţi) a crescut continuu, până
la 10.470 în 2012. Ritmul de creştere nu a fost însă constant: perioadei iniţiale
de creştere rapidă (1996–2000; +32,7% anual) i-au urmat perioade de creştere
mai lentă (2001–2003 şi 2004–2006), pentru ca ritmul să crească din nou la 7–8%
anual în perioada 2007–2012 ca urmare a procesului de privatizare a secţiilor
de dializă. Există o relaţie inversă între ritmul anual de creştere şi numărul
total de bolnavi prevalenţi (un indicator al populaţiei cu servicii de dializă):
cu cât acoperirea necesarului de servicii de dializă este mai bună (deci numărul
bolnavilor trataţi este mai mare), cu atât ritmul de creştere scade. Tendinţa
ascendentă a ratei de creştere a numărului de bolnavi se va menţine până în
2017–2018, după care va scădea. Pentru anul în curs, rata de creştere prognozată
este de 7–8%. La sfârşitul anului 2013, erau 11.200 de bolnavi dializaţi, iar
la sfârşitul anului 2014 se estimează că vor fi peste 11.400 de bolnavi dializaţi.
Deşi BCR are o evoluţie predictibilă, care
ar permite pregătirea din timp a pacienţilor pentru iniţierea tratamentului
substitutiv renal, lipsesc programele adresate BCR în predializă, inclusiv cele
de educaţie a pacienţilor. De aceea, tratamentul substitutiv renal este
frecvent început neplanificat, iar pacienţii nu pot alege în cunoştinţă de cauză
modalitatea de tratament care le este cel mai bine adaptată. Elaborarea de
programe de îngrijire a bolii cronice de rinichi cu o componentă educaţională
ar avea şi avantajul redresării utilizării dializei peritoneale.
Numărul total al centrelor de dializă a
crescut într-un ritm mai mic (2,5%), dar numărul centrelor private creşte, în
timp ce numărul centrelor publice a scăzut. La sfârşitul anului 2013, existau
147 de centre de dializă, din care 57 publice şi 90 private. Nivelul de dotare
a centrelor private de dializă este la standarde europene, în timp ce
majoritatea centrelor publice de dializă nu au acelaşi nivel de dotare, din
lipsa investiţiilor. Ponderea centrelor publice ca număr de bolnavi trataţi
este în scădere şi se menţine la cel mai jos nivel din 2007 (12%). Deoarece
centrele publice din spitale funcţionează ca suport pentru centrele
ambulatorii, este obligatorie menţinerea unor staţii publice de dializă, cel puţin
în spitalele judeţene. Reducerea ponderii sectorului public sub limita de 12%
ar fi periculoasă.
Transplantul renal are avantaje medicale şi economice faţă de dializă, dar are o
pondere încă mică în România. Deşi în creştere (de la 2% în 2007), numai 8% din
bolnavi încep terapia de substituţie a funcţiilor renale prin transplant renal
în anul 2012. Datele sunt doar estimative, plecând de la raportările centrelor
de dializă (care se referă numai la bolnavii transplantaţi non-preemptiv) şi
ale unuia dintre centrele de transplant, neexistând un registru de transplant
funcţional. Cea mai mare parte a grefelor provine de la donatori cadavru (53%),
ceea ce constituie un progres faţă de anii anteriori, când grefele de la
donatori vii dominau. Necesarul anual este de cel puţin 400 de transplanturi
renale finanţate, pentru ca transplantul să contribuie efectiv la rezolvarea
problemei tratamentului substitutiv renal în România. De asemenea, ar trebui
introdusă raportarea obligatorie către Registrul renal român a bolnavilor
transplantaţi, pentru a avea o evidenţă corectă.
În ultimii cinci ani, ritmul mediu de creştere
a numărului total de bolnavi prevalenţi a fost de 8,9%, dar ponderea bolnavilor
dializaţi peritoneal (DP) a scăzut anual cu 1%, în pofida măsurilor de
stimulare lansate de CNAS. Deoarece tariful pentru un bolnav dializat
peritoneal este mai mic decât cel pentru un bolnav hemodializat (HD), scăderea
ponderii dializei peritoneale are consecinţe economice. Astfel, dacă ar fi fost
respectată proporţia de un bolnav DP pentru cinci bolnavi HD, recomandată de
CNAS, cheltuielile programului ar fi fost numai la nivelul anului 2011, cu 4,43
milioane de euro (5%) mai mici. Practic, mai mult de jumătate din cheltuielile
provenite din creşterea numărului de bolnavi puteau fi acoperite prin alocarea
unui număr adecvat de bolnavi dializei peritoneale.
Pe de altă parte, deoarece transplantul
renal a crescut ca pondere în ultimii ani, un sistem bazat pe dializă
peritoneală şi transplant ar permite tratarea unui număr mai mare de bolnavi cu
aceleaşi cheltuieli, fiind mult mai eficient economic decât sistemul actual,
bazat pe hemodializă şi transplant renal.
*Declinul funcţional
renal „fiziologic“ este de 1 ml/min pe an, după vârsta de 50 de ani. Declinul
variază mult în funcţie de natura bolii renale primare sau de stadiul BCR şi
poate fi influenţat prin terapie.